Lítium
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Általános | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Név, vegyjel, rendszám | lítium, Li, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Latin megnevezés | lithium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elemi sorozat | alkálifémek | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Csoport, periódus, mező | 1, 2, s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Megjelenés | ezüstfehér, szürke 
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomtömeg | 6,938–6,997 g/mol[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronszerkezet | [He] 2s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronok héjanként | 2, 1
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Halmazállapot | szilárd | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sűrűség (szobahőm.) | 0,535 g/cm³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sűrűség (folyadék) az o.p.-on | 0,512 g/cm³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olvadáspont | 453,69 K (180,54 °C, 356,97 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forráspont | 1615 K (1342 °C, 2448 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olvadáshő | 3,00 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Párolgáshő | 147,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moláris hőkapacitás | (25 °C) 24,860 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomi tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristályszerkezet | köbös tércentrált | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidációs szám | 1 (erősen bázikus oxid) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitás | 0,98 (Pauling-skála) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizációs energia | 1.: 520,2 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.: 7298,1 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.: 11815,0 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomsugár | 145 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomsugár (számított) | 167 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalens sugár | 134 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals-sugár | 182 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Egyebek | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mágnesség | paramágneses[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fajlagos ellenállás | (20 °C) 92,8 nΩ·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hőmérséklet-vezetési tényező | (300 K) 84,8 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hőtágulási együttható | (25 °C) 46 µm/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hangsebesség (vékony rúd) | (20 °C) 6000 m/s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young-modulus | 4,9 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nyírási modulus | 4,2 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kompressziós modulus | 11 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs-keménység | 0,6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell-keménység | - HB | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-szám | 7439-93-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fontosabb izotópok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hivatkozások | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A lítium a periódusos rendszer I. főcsoportjába, az alkálifémek közé tartozó kémiai elem. Vegyjele Li, rendszáma 3. Elnevezése a görög λίθος (lithosz, kő) szóból ered. Régies magyar elnevezése lavany.[3] Elemi állapotban lágy, ezüstfehér színű fém. Szabványos hőmérsékleten és nyomáson a lítium a legkisebb atomtömegű fém és a legkisebb sűrűségű szilárd elem. Mint minden alkálifém, erősen reaktív és gyúlékony, emiatt jellemzően ásványi olajba merítve tárolják. Amikor felvágják, a lítium fémesen csillog, de a nedves levegővel érintkezve a felület gyorsan tompa ezüstszürkévé, majd feketévé korrodálódik. Mivel erősen reaktív, a természetben elemi állapotban nem található meg, csak vegyületeiben fordul elő, amelyek általában ionosak. A lítium számos pegmatit ásványban előfordul, de a lítiumion oldhatósága miatt jelen van az óceánokban is, ennek okán gyakorta állítják elő telített sósvízből és agyagból. Az iparban lítium-klorid és kálium-klorid keverékének elektrolízisével különítik el és állítják elő.
A lítium atommagok az instabilitás peremén léteznek, mivel a természetben megtalálható két stabil izotópjában az egy nukleonra jutó kötési energiája a stabil nuklidok között a legalacsonyabbak közé tartozik. Atommagjának viszonylagos instabilitása következtében a periódusos rendszer első 32 eleme közül csak a 26. leggyakoribb a Naprendszerben, annak ellenére, hogy atomtömege rendkívül kicsi.[4] Hasonló okokból kifolyólag a lítiumot szoros szálak fűzik a magfizikához. A lítiumatomok héliummá történő átalakítása (transzmutálása) volt az első teljes egészében ember által kiváltott nukleáris reakció (1932-ben), míg a lítium-6-deuterid fúziós üzemanyagként szolgál a többfázisú termonukleáris fegyverekben.[5]
A lítiumot és vegyületeit számos ipari alkalmazásban használják, beleértve a hőálló üvegeket és kerámiákat, a repülőgépiparban használt ötvözeteket (nagy szilárdság, kis tömeg), a lítiumelemeket és a lítiumion-akkumulátorokat. A teljes lítium termelésnek több, mint a felét ezek az alkalmazások igénylik.
A lítium nyomokban minden élőlényben megtalálható. Az elemnek nincs szerepe semmilyen láthatóan létfontosságú biológiai folyamatban, mivel az állatok és a növények lítiummentes környezetben is egészségesek maradnak. A nem létfontosságú funkciók azonban nem zárhatók ki. A lítiumion (Li+) különféle sói formájában adagolva hasznos hangulatstabilizálónak bizonyult a bipoláris zavarban szenvedők kezelésekor, köszönhetően az ion emberi szervezetben kifejtett neurológiai hatásainak (lásd: lítiumterápia).
Tulajdonságai[szerkesztés]
Fizikai jellemzők[szerkesztés]


A többi alkálifémhez hasonlóan a lítiumnak is egyetlen vegyértékelektronja van, amelynek leadásával könnyen kationt képez.[6] Emiatt jó villamos- és hővezető, valamint nagyon reakcióképes elem, habár az alkálifémek közül a legkevésbé reaktív. Más alkálifémekhez képest kisebb reaktivitása annak köszönhető, hogy a vegyértékelektronja közel helyezkedik el az atommagjához (a fennmaradó két elektron a lítium 1s héján helyezkedik el, és emiatt sokkal alacsonyabb energiájú, így ezek nem vesznek részt a kémiai kötésekben).[6]
A fém lítium elég puha ahhoz, hogy késsel vágható legyen. Amikor felvágják, ezüstfehér színű és fémes csillogású, ám az oxidáció miatt gyorsan elszürkül, elfeketedik.[6] Bár a fémek között az egyik legalacsonyabb olvadáspontú elem (180 °C), olvadás- és forráspontja az alkálifémek közt a legmagasabb.[7]
A lítium sűrűsége nagyon kicsi, mindössze 0,534 g/cm³, a fenyőfáéhoz hasonló. A szobahőmérsékleten szilárd elemek közt a legkisebb sűrűségű, a következő legkönnyebb szilárd elem – a kálium – több, mint 60%-kal sűrűbb (0,862 g/cm³). Ezen túlmenően a héliumot és hidrogént leszámítva könnyebb, mint bármely folyékony elem, sűrűsége csupán ⅔-a a folyékony nitrogénének (0,808 g/cm³).[m 1][8] A lítium úszik a legkönnyebb szénhidrogén olajok felszínén is, és egyike annak a három fémnek, amelyek képesek úszni a vízen (a másik kettő a nátrium és a kálium).
A lítium hőtágulási együtthatója kétszerese az alumíniuménak és négyszerese a vasénak.[9] Normál nyomáson 400 μK alatt, illetve nagyon magas nyomáson (>20 GPa) már valamivel magasabb hőmérsékleten (több mint 9 K) szupravezetővé válik.[10] 70 K alatti hőmérsékleten – a nátriumhoz hasonlóan – diffúzió nélküli fázisváltozáson megy keresztül. 4,2 K hőmérsékleten romboéderes kristályszerkezete van (kilenc rétegű), amely magasabb hőmérsékleten lapközepes köbös ráccsá, majd térközepes köbös ráccsá alakul át. A folyékony hélium hőmérsékletén (4 K) a romboéderes szerkezet a legelterjedtebb.[11] Magas nyomáson több allotrop módosulata is ismert.[12]
A lítium fajlagos hőkapacitása – 3,58 kJ/(kg·K) – a legmagasabb az összes szilárd anyag közül.[13][14] E tulajdonsága miatt a fém lítiumot gyakran használják hűtőfolyadékként különböző hőátadásos folyamatokhoz.[13]
Kémiai jellemzők[szerkesztés]
A lítium azonnal kölcsönhatásba lép a vízzel, de észrevehetően kisebb energiával, mint más alkálifémek. A reakció során hidrogéngáz és vízben oldott lítium-hidroxid keletkezik.[6] A vízzel való heves reakciója miatt a lítiumot általában valamely szénhidrogén, gyakran petrolátum (vazelin) alatt tárolják. Bár a nehezebb alkálifémek sűrűbb anyagokban is tárolhatóak – mint például ásványi olajok – a lítium nem elég sűrű ahhoz, hogy teljesen elmerüljön ezekben a folyadékokban.[15] Nedves levegőn a lítium gyorsan elhomályosul a lítium-hidroxid (LiOH és LiOH·H2O), a lítium-nitrid (Li3N) és a lítium-karbonát (Li2CO3, a LiOH és a CO2 közti másodlagos reakció eredménye) alkotta fekete bevonattól.[16]
Lángba helyezve, a lítium vegyületei markáns bíborvörösre színezik azt, erősen égve azonban a láng ragyogó ezüstszínűvé válik.[17] A lítium száraz levegővel nem lép kölcsönhatásba, de oxigénben meggyullad és elég, ha vízzel vagy vízpárával érintkezik.[18] A lítium szabad levegőn, vagy különösen vízzel érintkezve gyúlékony és robbanásveszélyes, bár kevésbé, mint a többi alkálifém. A lítium–víz reakció normál hőmérsékleten gyors ugyan, de nem erőteljes, mert a reakcióban keletkező hidrogén nem gyullad meg. Az alkálifém-tüzekhez hasonlóan a lítium-tüzet is nehéz eloltani, mert száraz porral oltó készüléket igényel. A lítium az egyetlen fém, amely a nitrogénnel már szobahőmérsékleten egyesül.[19][20]
A lítium erős hasonlóságot mutat a magnéziummal (úgynevezett átlós kapcsolatban vannak), atom- és ionsugaruk közel azonos. A két fém közötti kémiai hasonlóság megmutatkozik a nitridképzésükben (nitrogénnel reagálva); az oxid- (Li2O) és peroxidképzésükben (Li2O2) oxigénben elégetve; sóik hasonló oldhatóságában; valamint nitridjeik és karbonátjaik termikus instabilitásában.[16][21] A fém nagy hőmérsékleten (>500 °C) reakcióba lép a hidrogéngázzal, ezzel lítium-hidridet (LiH) hozva létre.[22]
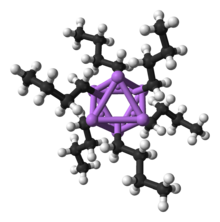
Egyéb ismert biner (kétkomponensű) vegyületei közé tartoznak a halogenidek (LiF, LiCI, LiBr, Lil), valamint a szulfid (Li2S), a szuperoxid (LiO2) és a karbid (Li2C2). Sok más szervetlen vegyülete ismert, amelyben a lítium anionokhoz kötődve változatos sókat képez: borátok, amidok, karbonát, nitrát, vagy bórhidrid (LiBH4). Több szerves lítium reagens is ismert, amelyekben a szénatom és a lítiumatom között közvetlen kötés található, ezzel lényegében karbaniont hozva létre. Ezek rendkívül erős bázisok és nukleofilok. Ezen lítiumorganikus vegyületek többségében a lítiumionok hajlamosak saját maguktól magas szimmetriájú klaszterekbe csoportosulni, ami viszonylag gyakori az alkálifém kationok között.[23] Nagyon kis hőmérsékleten kimutatták a LiHe létezését, amely egy nagyon gyengén kötött van der Waals-vegyület.[24]
Gázhalmazállapotban – bizonyos feltételek mellett – a lítium ferromágnességet mutat.[25]
Izotópjai[szerkesztés]

A természetben előforduló lítiumnak két stabil izotópja van, a 6Li és a 7Li, ezek közül a 7Li a gyakoribb (természetes előfordulása 92,5 %).[6][15][26] Összehasonlítva a szomszédos elemekkel, a héliummal és a berilliummal, mindkét természetes izotóp rendellenesen alacsony egy nukleonra jutó kötési energiával bír, ami azt jelenti, hogy egyedüliként a könnyű elemek közül energia felszabadulás mellett képes a maghasadásra. A két lítium atommagnak alacsonyabb az egy nukleonra jutó kötési energiája, mint bármely más stabil nuklidnak, kivéve a deutériumot és a hélium-3-at.[27] Ennek eredményeként a lítium, bár atomtömege nagyon kicsi, a periódusos rendszer első 32 eleme közül mindössze a 26. leggyakoribb elem a Naprendszerben.[4] Hét radioaktív izotópja ismert, ezek közül a legstabilabb a 8Li, 838 ms, és a 9Li 178,3 ms felezési idővel. Az összes többi radioaktív izotópjának felezési ideje rövidebb, mint 8,6 ms. A legrövidebb életű lítiumizotóp a 4Li, amely protonemisszió révén bomlik, felezési ideje mindössze 7,6·10−23 s.[28]
A 7Li egyike a primordiális elemeknek (vagy még pontosabban a primordiális nuklidoknak) amelyek az ősrobbanás nukleoszintézisében keletkeztek. Kis mennyiségű 6Li és a 7Li a csillagokban is keletkezik, de jelen álláspont szerint az izotópok keletkezésük pillanatában el is égnek.[29] További kis mennyiségű lítium – mind 6Li, mind 7Li – keletkezhet a napszél vagy a kozmikus sugárzás és nehezebb atomok kölcsönhatásából, valamint a fiatal Naprendszer 7Be- és 10Be-izotópjainak radioaktív bomlása révén.[30] Bár lítium a csillagokban is keletkezik a sztelláris nukleoszintézis során, de ez tovább is ég. 7Li széncsillagokban is keletkezhet.[31]
A lítiumizotópok számos természetes folyamatban jelentősen frakcionálódnak,[32] beleértve az ásványképződést (kémiai kicsapás), az anyagcserét és az ioncserét. A lítiumion helyettesíti a magnéziumot és a vasat az oktaéderes helyeken az agyagásványokban. A folyamatban a 6Li könnyebben vesz részt, mint a 7Li, ezért a könnyű izotóp feldúsulásához vezet a hiperfiltrációs és metaszomatózis (kőzet-átalakulás) folyamatokban. Az egzotikus lítium-11-ről ismert, hogy nukleáris haloval rendelkezik. A lézeres izotóp szeparáció néven ismert folyamat lehetővé teszi a lítium izotópjainak különválasztását.[33]
A lítiumizotópok mesterséges különválasztódásának fő okai a nukleárisfegyver-gyártás és az egyéb magfizikai felhasználások. Az ipari és a katonai készletekben felhalmozott könnyű 6Li-izotóp mennyisége olyan nagy, hogy enyhe, de mérhető mértékben megváltozott a 6Li és 7Li aránya még a természetes forrásokban is, mint például a folyókban. Ez odáig vezetett, hogy szokatlan bizonytalanság övezi a lítium standardizált atomtömegét, mivel ez a mennyiség függ a természetben előforduló stabil lítiumizotópok természetes előfordulási arányától.[34]
Előfordulása[szerkesztés]

Csillagászati[szerkesztés]
A modern kozmológiai elméletek szerint a lítium – mindkét stabil izotópja, a lítium-6 és a lítium-7 – egyike annak a három elemnek, amely az ősrobbanásban keletkezett.[35] Bár az ősrobbanás nukleoszintézise során keletkezett lítium mennyisége függ az egy barionra jutó fotonok számától, a lítium gyakorisága elfogadható pontossággal kiszámítható, és ez alapján „kozmológiai lítium eltérés” mutatkozik a Világegyetemben: az idősebb csillagok látszólag kevesebb lítiumot tartalmaznak, mint kellene, míg néhány fiatalabb csillag jóval többet. A lítium hiányát az idősebb csillagokban az okozza, hogy a lítium keveredik a csillag belső régióival, ahol megsemmisül.[36] Továbbá, a lítium termelődik a fiatal csillagokban. Habár 2,4 millió Celsius-fok feletti hőmérsékleten (a legtöbb csillag könnyedén eléri ezt a hőmérsékletet a belsejében), protonnal ütközve a lítium két héliumatommá transzmutálódik, a lítium a vártnál sokkal gyakoribb a kései generációs csillagokban, melynek oka ezidáig nem ismert teljes egészében.[15]
Bár a lítium egyike annak a három elemnek (a hélium és a hidrogén mellett), amely egyidejűleg szintetizálódott az ősrobbanásban, a berilliummal és a bórral egyetemben sokkal kevésbé gyakori, mint a többi szomszédos elem. Ez annak az eredménye, hogy a lítium elpusztításához alacsony hőmérséklet is elegendő, és nincsenek olyan közönséges folyamatok, amelyekben termelődik.[37]
A lítium megtalálható a barna törpékben és bizonyos rendellenes narancs csillagokban. Mivel a lítium jelen van a hidegebb és kisebb tömegű barna törpékben, de elpusztul a meleg vörös törpe csillagokban, a lítium vonalak színkép-spektrumbeli jelenléte lehetővé teszi a „lítiumteszt” elvégzését és így a két objektum megkülönböztetését (mindkettő kisebb, mint a Nap).[15][38][39] Bizonyos narancs csillagok is a szokásosnál nagyobb koncentrációban tartalmaznak lítiumot, ezek – mint például a Centaurus X-4 – általában valamely nagy tömegű neutroncsillag vagy fekete lyuk körül keringenek, amelyek gravitációs vonzása a nehezebb lítiumot a hidrogén-hélium csillag felszínére húzza, így több lítium mutatható ki.[15]
Földi[szerkesztés]
| Ország | Kitermelés | Tartalék[m 2] |
|---|---|---|
| 3200 | 850 000 | |
| 9260 | 970 000 | |
| 160 | 64 000 | |
| 480 | 180 000 | |
| 12 600 | 7 500 000 | |
| 5200 | 3 500 000 | |
| 820 | 10 000 | |
| 470 | 23 000 | |
| Világ összesen | 34 000 | 13 000 000 |
Bár a lítium széles körben elterjedt a Földön, erőteljes reakcióképessége miatt elemi formában nem található meg a természetben.[6] A tengervizek összes lítiumtartalma nagyon nagy, becslések szerint 230 milliárd tonna; az elem koncentrációja viszonylag állandó 0,14–0,25 ppm.[41][42][43] Ennél nagyobb, 7 ppm-et megközelítő koncentrációban fordul elő hidrotermikus források közelében.[42]

Becslések szerint a lítium koncentrációja a földkéregben tömegre vetítve 20–70 ppm közé tehető.[16] A lítium képezi a magmás kőzetek kisebb részét, ezen belül a legnagyobb koncentrációban a gránitban található meg. A gránit pegmatitok a leggazdagabbak lítiumtartalmú ásványokban, ezek közül kereskedelmi szempontból a spodumen és a petalit a legjelentősebb.[16] További fontos lítiumásvány a lepidolit,[44] valamint legújabban a hektorit agyag.[45] Kilogrammonkénti 20 mg-os mennyiségével[46] a lítium a földkéreg 25. leggyakoribb eleme.
A Handbook of Lithium and Natural Calcium (A lítium és a természetes kalcium kézikönyve) szerint a lítium viszonylag ritka elem, és bár számos kőzetben és egyes sós vizekben is megtalálható, ezekben koncentrációja mindig nagyon kicsi. Meglehetősen nagyszámú lítiumtartalmú ásványtelep és sóoldat létezik, de ezek közül csak kevésnek van tényleges vagy potenciális kereskedelmi értéke. Sok lelőhely túl kicsi, mások túl gyenge minőségűek.[47]
A legnagyobb lítiumtartalékok[m 2] egyike a bolíviai Salar de Uyuni terület, amely 5,4 millió tonna ércet rejt. A US Geological Survey 2010-ben úgy becsülte, hogy messze a legnagyobb tartalékok (7,5 millió tonna) Chilében találhatóak,[48] és itt a legnagyobb az éves termelés (8800 tonna) is. A jelentősebb termelők közé tartozik még Ausztrália, Argentína és Kína.[40][49]
2010 júniusában a New York Times napilap arról számolt be, hogy amerikai geológusok talajfelméréseket végeztek kiszáradt sós tavakban Afganisztán nyugati részén, abban a reményben, hogy ott hatalmas lítiumkészletek rejlenek. Pentagoni tisztviselők azt nyilatkozták, hogy „a Ghazni tartományban elvégzett elsődleges elemzés azt mutatta, hogy a potenciális lítiumkészletek a bolíviaival azonos méretűek, melyek ma a világon a legnagyobb ismert lelőhelyek”.[50] Ezek a becslések „elsősorban régi adatokon alapulnak, amelyeket a szovjetek gyűjtöttek össze Afganisztán 1979–1989-es megszállása alatt”. Stephen Peters, a USGS Afghanistan Minerals Project vezetője úgy nyilatkozott, hogy nincs tudomása arról, hogy a USGS részt vett volna bármilyen új ásványkutató felmérésben az elmúlt két évben (2008–2010). „Nincsen tudomásunk semmilyen lítium felfedezésről” – mondta.[51]
Egyes ásványvizekben és gyógyvizekben is nagy mennyiségben található meg ionos formában. Magyar ásványvizek közül a Balfi ásványvíz tartalmazza a legtöbb lítiumot – 0,22 mg/l-t.
Biológiai[szerkesztés]
A lítium nyomokban megtalálható számos növényben, planktonban és a gerinctelenekben, 69–5760 ppb koncentrációban. A gerincesekben lévő lítium mennyisége valamivel alacsonyabb, azt tapasztalták, hogy a gerincesek szinte minden szövetében és testnedvében a lítium koncentrációja 21–763 ppb közé esik.[42] A tengeri élőlények hajlamosabbak a lítium felhalmozására, mint a szárazföldiek.[52] Nem ismert, hogy a lítiumnak van-e élettani szerepe bármely organizmusban,[42] de emlősökön végzett táplálkozástudományi vizsgálatok jelezték egészségügyi fontosságát, ami azt sugallja, hogy a lítium esszenciális nyomelem, az ajánlott napi táplálékbevitel (RDA) 1 mg/nap.[53] Egy Japánban végzett megfigyelésekre hivatkozó, 2011-es tanulmány azt állítja, hogy az ivóvízben előforduló természetes lítium megnövelheti az emberi élettartamot.[54]
Története[szerkesztés]

A petalitot (LiAlSi4O10) a brazil kémikus és államférfi, José Bonifácio de Andrada fedezte fel 1800-ban, a svéd Utö szigeti bányában.[55][56][57] Azonban 1817-ig nem volt ismert, hogy a petalit ércben lítium rejlik, amíg Johan August Arfwedson Jöns Jakob Berzelius vegyész laboratóriumában dolgozva ki nem mutatta az új elemet annak vizsgálata során.[58][59][60] Ez az elem a nátrium- és a kálium-vegyületekhez hasonló vegyületeket képezett, bár karbonátja és hidroxidja vízben kevésbé oldódott, és az oldatuk lúgosabb volt.[61] Berzelius a lúgos anyagot a görög λιθoς (lithosz) szó alapján (jelentése kő) a „lithion / lithina” névvel illette, hogy ezzel utaljon az elem szilárd ásványban történt felfedezésére; szemben a káliummal, amit növényi hamuban fedeztek fel, vagy a nátriummal, amely részben arról volt ismert, hogy bőségesen megtalálható az állati vérben. Az anyagban lévő fémet „lítium”-nak nevezte el.[6][56][60]
Arfwedson később bebizonyította, hogy ugyanez az elem van jelen a spodumen és a lepidolit ásványokban.[56] Christian Gmelin volt az első, aki 1818-ban megfigyelte, hogy a lítiumsók élénkpirosra színezik a lángot.[56] Arfwedson és Gmelin is megpróbálta elkülöníteni a vegytiszta elemet a sóiból, ám ez egyikőjüknek sem sikerült.[56][60][62] Erre 1821-ig nem is került sor, amikor William Thomas Brande lítium-oxid elektrolízisével előállította a tiszta lítiumot. Ezt az eljárást korábban már Sir Humphry Davy is alkalmazta a kálium és a nátrium különválasztása során.[15][62][63][64] Brande ismertetett néhány tiszta lítiumsót, többek közt a lítium-kloridot; valamint úgy becsülte, hogy a „lithia” (lítium-oxid) mintegy 55% fémet tartalmaz, azaz a lítium atomsúlyát 9,8 g/mol körülinek tételezte fel (a mai érték ~6,94 g/mol).[65] Robert Bunsen és Augustus Matthiessen 1855-ben lítium-klorid elektrolízise révén állított elő nagyobb mennyiségű lítiumot.[56] Ennek az eljárásnak a felfedezése vezetett el a továbbiakban a lítium kereskedelmi termeléséhez, amit a német Metallgesellschaft AG indított el 1923-ban. Ebben a folyamatban már lítium-klorid és kálium-klorid folyékony keverékét elektrolizálva állították elő a fémet.[56][66][67]
A lítium előállítása és felhasználása jelentős változásokon ment keresztül a történelem folyamán. A lítium első fontos alkalmazási területe a második világháborúban és nem sokkal utána a hőmérséklettűrő lítium kenőzsírok gyártása volt a repülőgépipar számára. Ezt a felhasználást segítette az a tény, hogy a lítium alapú szappanok más alkáli szappanoknál magasabb olvadáspontúak, és kevésbé korrozívak, mint a kalcium alapú szappanok. A lítiumszappanok és a ráépülő lítiumzsírok iránti szűk piacot erősítette néhány kisebb bányavállalat is, főleg az Amerikai Egyesült Államokban. A lítium iránti kereslet a hidegháború évei alatt drasztikusan megnőtt, ahogy elindult a nukleáris fúziós fegyverek gyártása. A lítium-6 és lítium-7 izotópok neutron besugárzás hatására egyaránt képesek tríciumot termelni, így önmagukban alkalmasak a trícium, valamint lítium-deuterid formájában a hidrogénbombák belsejében használt szilárd fúziós üzemanyag előállítására. Az 1950-es és 1980-as évek közötti időszakban az Egyesült Államok elsődleges lítiumtermelő országgá vált. Végeredményben a felhalmozott készlet mennyisége durván 42 000 tonna lítium-hidroxid volt. A felhalmozott készletben lévő lítium-6 75%-át eltávolították, amely elegendő volt ahhoz, hogy megváltoztassa az elem mérhető atomtömegét számos szabványos vegyületben és természetes forrásban is, amelyek szennyeződtek az izotópszeparáló üzemekből kiengedett lítiumsókkal, amelyek utat találtak a talajvízbe.[34][68]
A lítiumot felhasználták az üveg olvadási hőmérsékletének csökkentésére és az alumínium-oxid olvadási viselkedésének javítására a Hall–Héroult-eljárásban.[69][70] Ez a két felhasználási forma az 1990-es évek közepéig dominált a piacon. A nukleáris fegyverkezési verseny befejeződésével a lítium iránti igény csökkent, és az amerikai Energiaügyi Minisztérium (Department of Energy) készleteinek értékesítése tovább csökkentette az árakat.[68] De az 1990-es évek közepén, több vállalat telített sósvízből (brine) kezdett lítiumot kivonni, ami olcsóbbnak bizonyult, mint a föld alatti és a külszíni bányászat. A bányák többsége bezárt vagy más anyagokra koncentrált, mivel csak a zónás pegmatitok ércét lehetett versenyképes áron kitermelni.
A lítiumion-akkumulátorok használata miatt megnőtt a lítium iránti kereslet, amely 2007-re már meghatározó felhasználási területté vált.[71] A lítiumelemek 2000-es évekbeli felfutásával egyidejűleg új vállalatok bővítették a kitermelést, hogy kielégítsék a növekvő igényeket.[72][73]
Előállítása, kitermelése[szerkesztés]

A második világháború vége óta a lítium kitermelése jelentősen megnövekedett. A lítiumsókat nagyrészt ásványvízforrásokból, sós medencékből és sólerakódásokból vonják ki, de egyes lítiumtartalmú ércek – spodumen, lepidolit, petalit, ambligonit – bányászatával is nyerik őket.[74] A fém lítium előállítható 55% lítium-kloridot és 45% kálium-kloridot tartalmazó keverék elektrolízisével, körülbelül 450 °C hőmérsékleten.[75] Az elektrolízis során az egyes elektródokon lejátszódó reakciók:
A fém piaci árfolyama 1998-ban 21 600 Ft/kg (95 $/kg) volt,[76] ez az érték 2014-re megháromszorozódott.[77] A USGS (United States Geological Survey) becslése szerint a világ lítiumtartalékai 2008-ban 13 millió tonnára rúgtak.[40] Lítiumlelőhelyek találhatók Dél-Amerikában végig az Andok hegyláncai mentén; ennek megfelelően Chile a vezető lítiumtermelő, melyet szorosan követ Argentína. Mindkét országban sós medencékből nyerik ki az elemet, akárcsak az Egyesült Államokban, ahol Nevada bővelkedik lítiumban.[13] A világ ismert lítiumtartalékainak fele azonban Bolíviában, az Andok közép-keleti lejtőin elterülő országban található. Az USGS becslése szerint csak az Uyuni sósivatagban 5,4 millió tonna lítium rejlik.[78][79] 2009-ben Bolívia japán, francia és koreai vállalatokkal kezdett tárgyalásokba a kitermelés megindítása céljából.[78] A nemrégiben felfedezett wyomingi Rock Springs Uplift lelőhelyen a becslések szerint 228 000 tonna lítium található, egy mindössze 64,75 négyzetkilométeres területen. Extrapolálva ezt az értéket, a geológiai képződmény területén akár 18 millió tonna is rejtőzhet.[80]
A lítium potenciális forrásai lehetnek még a geotermikus kutak. A geotermikus folyadék ugyanis oldott ásványi anyagokat (mosadékot) szállít a felszínre,[81] melyből a lítium igazoltan kinyerhető.[82] Mivel a lítium elválasztása egyszerű szűréses technikával történik, a folyamat- és a környezeti költségek gyakorlatilag megegyeznek a már működő geotermikus kútéval, a relatív környezeti hatások tehát pozitívak.[83]
A lítium előállításának potenciális növekedését tekintve megoszlanak a vélemények. Egy 2008-as tanulmány arra a következtetésre jutott, hogy a „reálisan elérhető lítium-karbonát termelés, a jövőbeni hálózatról tölthető hibridautók (PHEV – plug-in-hybrid vehicle) és elektromos járművek globális piaci igényeinek csak egy kis töredékét lesz képes kielégíteni” és hogy „a következő évtizedben a hordozható elektronikai szektor kereslete fogja elnyelni a tervezett termelés-növekedés jelentős részét”, valamint kijelenti, hogy „a lítium-karbonát tömegtermelése nem környezetkímélő, helyrehozhatatlan környezeti károkat okoz a megvédendő ökoszisztémákban, ezért a lítiumion-meghajtás összeegyeztethetetlen a zöld autó (green car) koncepcióval”.[49]
Ugyanakkor egy, a Lawrence Berkeley National Laboratory és a University of California Berkeley által végzett 2011-es tanulmány szerint a lítiumtartalékokra vonatkozó jelenlegi becslések nem lehetnek korlátozó tényezői a nagyüzemi akkumulátor és elektromos jármű gyártásnak; mivel a tanulmány szerint a jelenlegi tartalékokból 1 milliárd 40 kWh-s lítiumalapú akkumulátor épülhet.[84] Egy másik, a University of Michigan és a Ford Motor Company kutatói által végzett 2011-es tanulmány megállapította, hogy a lítiumkészletek 2100-ig elegendőek a globális kereslet kielégítésére, beleértve a hibrid elektromos, hálózatról tölthető (plug-in) hibrid és akkumulátoros-elektromos járművek potenciális széles körű elterjedéséhez szükséges lítiumot is. A tanulmány becslése szerint a globális lítiumtartalékok 39 millió tonnára tehetőek, míg a 90 éves vizsgálati idő alatt a lítium teljes keresete a gazdasági növekedés és az újrahasznosítás arányától függően nem haladja majd meg a 12-20 millió tonnát.[85]
Egészen a 21. század elejéig Dél-Amerika (főleg Chile, Argentína) sótavai jelentették a lítium kinyerésének legfontosabb forrásait. A helyzet azonban megváltozott, miután Ausztrália megnyitotta új és jobb minőséget adó lítiumbányáit.[86]
| Country | Kitermelés | Tartalékok [m 2] | Források |
|---|---|---|---|
| 5700 | 2 000 000 | 9 000 000 | |
| 14 300 | 1 600 000 | 2 000 000+ | |
| - | - | 100 000+ | |
| - | - | 9 000 000 | |
| 200 | 48 000 | 200 000 | |
| 480 | 180 000 | 2 000 000 | |
| 12 000 | 7 500 000 | 7 500 000+ | |
| - | - | 1 000 000 | |
| - | - | 200 000 | |
| 2000 | 3 200 000 | 7 000 000 | |
| 200 | 60 000 | N/A | |
| - | - | 1 000 000 | |
| - | - | 1 000 000 | |
| ? | 38 000 | 6 900 000 | |
| 900 | 23 000 | 100 000+ |
Nagy mennyiségű lítium készlettel rendelkezik még Csehország is, kitermelése 2019-től indul és a tervek szerint évi 20 800 tonna lítiumot fognak előállítani. A becsült lítium készletük 1,3 millió, ami a globális szinthez képest 3%-ot jelent.[88]
Felhasználása[szerkesztés]

Kerámia és üveg[szerkesztés]
A lítium-oxid széles körben használt folyasztószer a szilícium-dioxid feldolgozásához, amely csökkenti az anyag olvadáspontját és viszkozitását, így jobb fizikai tulajdonságokkal – többek között alacsony hőtágulási együtthatójú – bíró kerámiamázak készíthetők.[90] A lítium-oxid a tűzálló edények egyik összetevője; világszerte önmagában ez a legnagyobb felhasználási területe a lítiumvegyületeknek.[89] Erre a célra általában lítium-karbonátot (Li2CO3) használnak, amely hevítve oxiddá alakul.[91]

Elektromosság és elektronika[szerkesztés]
A 20. század végén a lítium nagy elektrokémiai potenciáljának köszönhetően fontos összetevőjévé vált a szárazelemek elektrolitjának és egyik elektródjának. Mivel atomtömege kicsi, a lítium nagy töltés/tömeg és teljesítmény/tömeg aránnyal rendelkezik. Egy tipikus lítiumion-akkumulátor mintegy 3 V-ot állít elő cellánként, szemben a savas ólomakkumulátorral (2,1 V) vagy szén-cink szárazelemekkel (1,5 V). Az újratölthető és nagy energiasűrűségű lítiumion-akkumulátorok nem keverendőek össze a lítiumelemekkel, amelyek anódja lítium vagy lítiumvegyület, és nem tölthetőek újra (eldobhatóak).[92][93] A további, újratölthető lítium tartalmú akkumulátorok közé tartoznak még a lítiumion polimer akkumulátor, a lítium–vas-foszfát akkumulátor és a nanoszál akkumulátor.
Kenőzsír[szerkesztés]
A lítium harmadik legnagyobb felhasználási területe a kenőzsírgyártás. A lítium-hidroxid erős bázis, zsír jelenlétében hevítve lítium-sztearát szappanná alakul át. A lítiumszappannak megvan az a képessége, hogy besűríti az olajokat, így általános célú, magas hőmérsékleten is alkalmas kenőzsírokat állítanak elő belőle.[13][94][95]
Kohászat[szerkesztés]
Amikor folyasztószerként hegesztéshez vagy forrasztáshoz használják, a lítium elősegíti a fémek összehegedését, és megakadályozza az oxidképződést azáltal, hogy elnyeli a szennyeződéseket. Jó minőségű folyasztószerként nagyon fontos a kerámiák, zománcok és üvegek előállításához is. Alumíniummal, kadmiummal, rézzel és mangánnal alkotott ötvözeteit nagy teljesítményű repülőgép-alkatrészek (Al–Li ötvözetek) elkészítéséhez használják fel.[96]
Levegőtisztítás[szerkesztés]
A lítium-klorid és a lítium-bromid higroszkópos tulajdonságú, ezért gázáramok kiszárítására (a nedvességtartalmuk megkötésére) használják.[13] A lítium-hidroxid és a lítium-peroxid sókat leggyakrabban zárt térben, mint például űrhajók és tengeralattjárók fedélzetén használják fel a szén-dioxid eltávolítására és a levegő tisztítására. A lítium-hidroxid megköti a levegőben lévő szén-dioxidot és lítium-karbonátot képez, amely kis súlya miatt előnyösebb az alkáli-hidroxidokkal szemben. A lítium-peroxid (Li2O2) nedvesség jelenlétében nemcsak reagál a szén-dioxiddal és lítium-karbonátot képez, hanem oxigént is felszabadít.[97][98] A végbemenő reakció a következő:
- .
Néhány fent említett vegyületet – valamint a lítium-perklorátot is – oxigéngyertyákban alkalmazzák, hogy a tengeralattjárókat oxigénnel lássák el. Ezek kis mennyiségben bórt, magnéziumot, alumíniumot, szilíciumot, titánt, mangánt és vasat tartalmazhatnak.[99]

Pirotechnika[szerkesztés]
A lítium vegyületeit pirotechnikai színezékként és oxidálószerként használják a piros tűzijátékokban és jelzőfáklyákban.[13][100]
Optika[szerkesztés]
A mesterségesen növesztett lítium-fluorid kristályok tiszták és átlátszóak, ezért gyakran használják speciális IR, UV és VUV (vákuum UV) optikai feladatokra. A közönségesebb anyagok között az egyik legalacsonyabb törésmutatójú, és fényáteresztő képessége a legtávolabb nyúlik a mély UV–A sugárzási tartományba.[101] A finoman eloszlatott lítium-fluorid port termolumineszcens doziméterekben (TLD) használják: ha egy ilyen mintát sugárzás ér, a kristályhibák felhalmozódnak; melegítés hatására a hibák kékes fény kíséretében eltűnnek, amely fény intenzitása az elnyelt sugárdózis mértékétől függ. A kibocsátott fény vizsgálatával lehetőség nyílik az elnyelt dózis meghatározására.[102] A lítium-fluoridot időnként teleszkópok gyűjtőlencséiben is alkalmazzák.[13][103]
A lítium-niobát (LiNbO3) és a lítium-tantalát (LiTaO3) úgynevezett nemlineáris kristályok, amelyeket előszeretettel alkalmaznak a nemlienáris optikában és a terahertzes technológiában. Széles körben felhasználják őket a telekommunikációs termékekben, mint például a mobiltelefonok és optikai modulátorok kristályoszcillátoraiban. A mobiltelefonbeli lítium alkalmazások részaránya több mint 60%.[104]
Szerves- és polimerkémia[szerkesztés]
A szerves lítiumvegyületeket (lítiumorganikus vegyületek) széles körben használják polimerek és finomvegyszerek előállítására. A polimer- (műanyag-) iparban, amely ezen anyagok legnagyobb felhasználója, az alkil-lítium-vegyületeket katalizátorként/iniciátorként[105] használják a funkciós csoport nélküli alkének anionos polimerizálása során.[106][107][108] A finomvegyszerek termelésében a szerves lítiumvegyületek erősen bázikus tulajdonságát használják ki a szén-szén kötések kialakításához. A szerves lítiumvegyületeket fém lítiumból és alkil-halogenidekből állítják elő.[109]
Sok más lítiumvegyületet reagensként használnak szerves vegyületek előállítására. A népszerű vegyületek közé tartozik a lítium-alumínium-hidrid (Li[AIH4]) és a lítium-trietil-bórhidrid (LiBH(C2H5)3).
Hadiipar[szerkesztés]

A fémes lítiumot és komplex hidridjeit, mint például a Li[AlH4]-t, rakéta-hajtóanyagok nagy energiájú adalékaként alkalmazzák.[15] A lítium-alumínium-hidrid önmagában is használható szilárd üzemanyagként.[110]
A Mark 50 Torpedo kémiai energiát tároló meghajtórendszere (SCEPS) egy kis tartálynyi kén-hexafluorid gázt permetez szilárd lítiumtömbre. A reakció hőt termel, amelyet gőz termelésére használnak fel, a gőz pedig egy zárt Rankine-ciklus révén hajtja meg a torpedót.[111]
A lítium-6 tartalmú lítium-hidridet használják a hidrogénbombákban, amelyben egy atombomba körül helyezik el.[112]
Nukleáris[szerkesztés]
A lítium-6 értékes neutronelnyelő anyag a magfúzióban, és kiindulóanyag a trícium termeléshez. A természetes lítium mintegy 7,5%-os arányban tartalmaz lítium-6 izotópot, amelyet izotópszétválasztás révén nagy mennyiségben állítottak elő nukleáris fegyverek gyártására.[113] A lítium-7-et atomreaktorok hűtőfolyadékában is alkalmazzák.[114]

Lítium-deuterid volt a korai hidrogénbomba változatok választott fúziós üzemanyaga. Amikor neutronokkal bombázzák, a lítium-6 és a lítium-7 egyaránt tríciumot produkál. Ez a reakció – amely csak részben volt ismert az első hidrogénbomba tesztek során – volt a felelős a Castle Bravo atomrobbantás vártnál nagyobb energiahozamáért. A trícium viszonylag könnyen előidézhető magreakció során egyesül a deutériummal. Habár a részletek még mindig titkosak, úgy tűnik, a lítium-6-deuterid még mindig fontos szerepet játszik a modern nukleáris fegyverekben mint fúziós üzemanyag.[115]
A lítium-7 izotópban erősen dúsított lítium-fluorid képezi a folyékony sóolvadékos reaktorok LiF–BeF2 sókeverékének egyik alapvető komponensét. A lítium-fluorid kémiailag rendkívül stabil, és a LiF–BeF2 keverékek alacsony olvadásponttal rendelkeznek. Ezen kívül a 7Li, a Be és a F azon kevés nuklidok egyike, amelyek termikus neutronbefogási keresztmetszete elég kicsi ahhoz, hogy ne mérgezze a fissziós reaktorokban lejátszódó hasadási reakciókat.[m 3][116]
A kísérleti stádiumban levő magfúziós erőművekben a mágnesesen zárt, deutérium és trícium üzemanyagú reaktorokban lítiumot alkalmaznának a trícium előállítására. A természetben megtalálható trícium rendkívül ritka, ezért azt mesterségesen kell előállítani a reagáló plazmát körülölelő lítiumtartalmú „köpenyben”, ahol a plazmában lejátszódó deutérium–trícium reakció neutronjai a lítiumot további trícium keletkezése közben hasítják:
A lítiumot alfa-részecske vagy hélium atommag forrásként is használják. Amikor a 7Li-t felgyorsított protonokkal bombázzák, 8Be keletkezik, amely két alfa-részecskévé hasad el. Ezt a reakciót végezte el 1932-ben Cockroft és Walton, és ez volt az első teljesen mesterséges magreakció.[117][118] (Nukleáris reakciókat és ember irányította nukleáris transzmutációt 1917-ben is megvalósítottak már, de csak természetes radioaktív forrásból származó alfa-részecskékkel).
A lítium-7-et használó reaktorok nagy nyomáson melegítenek vizet, amely hő aztán korrózióra hajlamos hőcserélőkön adódik le. Ezekben a reaktorokban a lítiumra azért van szükség, hogy ellensúlyozza a neutronelnyelőként vízhez adott bórsav maró hatását.[119]

Gyógyászat[szerkesztés]
A lítium hatékony gyógyszer a bipoláris zavarban szenvedők számára.[120] Erre a célra különböző lítiumsókat, leggyakrabban a lítium-karbonátot (Li2CO3) és a lítium-citrátot (Li3C6H5O7) alkalmazzák. A lítiumsók hasznosak lehetnek a kapcsolódó betegségek, úgymint a szkizoaffektív zavar és a ciklikus depresszió kezelésében is. A lítiumról feltételezik, hogy lelassítja az Alzheimer-kór és a demencia kialakulását, így az ennek kockázatával élők számára védő hatású lehet.[121]
Ezeknek a sóknak az aktív része a lítiumion: Li+.[120] A sók ugyanakkor növelhetik az Ebstein-anomália kialakulásának kockázatát olyan csecsemőknél, akik édesanyja lítiumot kapott a terhesség első trimeszterében.[122]
Biztonság[szerkesztés]
A lítium maró hatású, ezért kezelése különleges odafigyelést igényel a bőrrel való érintkezés megelőzése érdekében. A lítiumpor vagy lítiumvegyületek (amelyek gyakran lúgosak) belégzése kezdetben irritálja az orrot és a torkot, míg nagyobb mennyiségben már folyadékfelhalmozódást okozhat a tüdőben, amely tüdőödémához vezet. A fém kezelése már önmagában is veszélyes, mert nedvességgel érintkezve maró lítium-hidroxid keletkezik. Levegőnek (és különösen nedvességnek kitéve) más alkálifémekhez hasonlóan, az elemi lítium is erősen gyúlékony és kismértékben robbanásveszélyes. Ezért a lítiumot levegőtől elzárva, nem-reakcióképes vegyületekben, például könnyűbenzinben (nafta) tárolják.[123]
- Törvényi szabályozása
Néhány jogrendszer korlátozza a lítiumelemek eladását, amelyek a lítium legkönnyebben elérhető forrásai az átlag fogyasztó számára. A lítiumelemek bizonyos típusainak szállítása megtiltható egyes közlekedési eszközökön (különösen a repülőgépeken), mert a legtöbb lítiumelem rövidre zárva nagyon gyorsan lemerül, ami túlmelegedéshez és esetleges robbanáshoz vezet. A legtöbb fogyasztókhoz kerülő termék beépített túlmelegedés elleni védelemmel van ellátva, vagy már eleve a kialakítása megakadályozza a zárlati áramok folyását. A belső rövidzárlat kialakulásának lehetősége is ismert, ez gyártási hibák vagy az elemek sérülésének következtében alakulhat ki, és spontán túlmelegedéshez vezet.[124][125]
Megjegyzések[szerkesztés]
- ↑ Az összes gáz-halmazállapotú elem sűrűsége elérhető az Airliquide.com Archiválva 2014. február 13-i dátummal a Wayback Machine-ben weboldalon.
- ↑ a b c Függelék. A USGS definíciója alapján; a tartalék magában foglalja a jelenleg gazdaságosan kitermelhető (tartalék), a gazdaságosság határán lévő (marginális tartalék) és a jelenleg még gazdaságtalanul kitermelhető (szubekonomikus tartalék) érckészletek egy részét is.
- ↑ A berilliumnak és a fluornak csak egy izotópja fordul elő: 9Be, illetve 19F. E két izotópon kívül – leszámítva az aktinoidákat – csak a 7Li, valamint a 2H, 11B, 15N, 209Bi, a C és az O stabil izotópjainak elég kicsi a termikus neutronbefogási keresztmetszete ahhoz, hogy a sóolvadékos tenyésztőreaktorok üzemanyagának fő komponensei lehessenek.
Jegyzetek[szerkesztés]
- ↑ Current Table of Standard Atomic Weights in Order of Atomic Number. Commission on Isotopic Abundances and Atomic Weights – Commission II.I of the International Union of Pure and Applied Chemistry, 2013. (Hozzáférés: 2013. október 13.)
- ↑ Magnetic susceptibility of the elements and inorganic compounds, Handbook of Chemistry and Physics 81st edition, CRC press.
- ↑ Szőkefalvi-Nagy Zoltán; Szabadváry Ferenc: A magyar kémiai szaknyelv kialakulása. A kémia története Magyarországon. Akadémiai Kiadó, 1972. (Hozzáférés: 2015. július 4.)
- ↑ a b Számadatok: Lodders, Katharina (2003. július 10.). „Solar System Abundances and Condensation Temperatures of the Elements” (PDF). The Astrophysical Journal 591 (2), 1220–1247. o, Kiadó: The American Astronomical Society. [2015. november 7-i dátummal az eredetiből archiválva]. DOI:10.1086/375492. (Hozzáférés: 2014. június 29.) Grafikusan ábrázolva File:SolarSystemAbundances.jpg
- ↑ Nuclear Weapon Design Archiválva 2016. január 12-i dátummal a Wayback Machine-ben. Federation of American Scientists (1998-10-21). fas.org
- ↑ a b c d e f g Krebs, Robert E.. The History and Use of Our Earth's Chemical Elements: A Reference Guide. Westport, Conn.: Greenwood Press (2006). ISBN 0-313-33438-2
- ↑ szerk.: Lide, D. R.: CRC Handbook of Chemistry and Physics, 86th, Boca Raton (FL): CRC Press (2005). ISBN 0-8493-0486-5
- ↑ Nitrogen, N2, Physical properties, safety, MSDS, enthalpy, material compatibility, gas liquid equilibrium, density, viscosity, inflammability, transport properties. Encyclopedia.airliquide.com. [2011. július 21-i dátummal az eredetiből archiválva]. (Hozzáférés: 2010. szeptember 29.)
- ↑ Coefficients of Linear Expansion. Engineering Toolbox
- ↑ Struzhkin, V. V.; Eremets, M. I.; Gan, W; Mao, H. K.; Hemley, R. J. (2002). „Superconductivity in dense lithium”. Science 298 (5596), 1213–5. o. DOI:10.1126/science.1078535. PMID 12386338.
- ↑ Overhauser, A. W. (1984). „Crystal Structure of Lithium at 4.2 K”. Physical Review Letters 53, 64–65. o. DOI:10.1103/PhysRevLett.53.64.
- ↑ (2004) „Metallic high-pressure modifications of main group elements”. Zeitschrift für Kristallographie 219 (6–2004), 376. o. DOI:10.1524/zkri.219.6.376.34637.
- ↑ a b c d e f g Hammond, C. R.. The Elements, in Handbook of Chemistry and Physics 81st edition. CRC press (2000). ISBN 0-8493-0481-4
- ↑ THERMO
- ↑ a b c d e f g Emsley, John. Nature's Building Blocks. Oxford: Oxford University Press (2001). ISBN 0-19-850341-5
- ↑ a b c d Kamienski, McDonald, Daniel P.; Stark, Marshall W.; Papcun, John R., Conrad W.. Lithium and lithium compounds, Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc.. DOI: 10.1002/0471238961.1209200811011309.a01.pub2 (2004)
- ↑ Náray-Szabó István. Kémia. Műszaki Könyvkiadó (1973. április 26.)
- ↑ (1861) „XXIV.—On chemical analysis by spectrum-observations”. Quarterly Journal of the Chemical Society of London 13 (3), 270. o. DOI:10.1039/QJ8611300270.
- ↑ Krebs, Robert E.. The history and use of our earth's chemical elements: a reference guide. Greenwood Publishing Group, 47. o. (2006). ISBN 0-313-33438-2
- ↑ (1994. január 1.) „Geochemistry international” 31 (1–4), 115. o.
- ↑ Greenwood, N.N.. Az elemek kémiája, 1., Budapest: Nemzeti Tankönyvkiadó, 104–105. o. (1999). ISBN 963-18-9144-5
- ↑ Beckford, Floyd: University of Lyon course online (powerpoint) slideshow. [2005. november 4-i dátummal az eredetiből archiválva]. (Hozzáférés: 2008. július 27.) „definitions:Slides 8–10 (Chapter 14)”
- ↑ Sapse, Anne-Marie and von R. Schleyer, Paul. Lithium chemistry: a theoretical and experimental overview. Wiley-IEEE, 3–40. o. (1995). ISBN 0-471-54930-4
- ↑ (2013. április 8.) „APS Physics” 6, 42. o.
- ↑ http://newsoffice.mit.edu/2009/magnetic-gas-0918
- ↑ Isotopes of Lithium. Berkeley National Laboratory, The Isotopes Project. [2008. május 13-i dátummal az eredetiből archiválva]. (Hozzáférés: 2008. április 21.)
- ↑ A File:Binding energy curve - common isotopes.svg grafikusan ábrázolja a stabil nuklidok kötési energiáit; a számadatok a képfájl vitalapján találhatóak.
- ↑ Sonzogni, Alejandro: Interactive Chart of Nuclides. Brookhaven National Laboratory. [2018. december 20-i dátummal az eredetiből archiválva]. (Hozzáférés: 2008. június 6.)
- ↑ Asplund, M. (2006). „Lithium Isotopic Abundances in Metal-poor Halo Stars”. The Astrophysical Journal 644, 229. o. DOI:10.1086/503538.
- ↑ (2006) „Li and B isotopic variations in an Allende CAI: Evidence for the in situ decay of short-lived 10Be and for the possible presence of the short−lived nuclide 7Be in the early solar system”. Geochimica et Cosmochimica Acta 70 (1), 224–245. o. [2010. július 18-i dátummal az eredetiből archiválva]. DOI:10.1016/j.gca.2005.08.016. (Hozzáférés: 2014. február 16.)
- ↑ (2000) „Episodic lithium production by extra-mixing in red giants”. Astronomy and Astrophysics 358, L49–L52. o.
- ↑ (2004) „Lithium isotopic signatures of peridotite xenoliths and isotopic fractionation at high temperature between olivine and pyroxenes”. Chemical Geology 212 (1–2), 163–177. o. DOI:10.1016/j.chemgeo.2004.08.009.
- ↑ Duarte, F. J. Tunable Laser Applications. CRC Press, 330. o. (2009). ISBN 1-4200-6009-0
- ↑ a b (2002) „Isotope-abundance variations of selected elements (IUPAC Technical Report)”. Pure and Applied Chemistry 74 (10), 1987. o. DOI:10.1351/pac200274101987.
- ↑ (1985) „Big bang nucleosynthesis – Theories and observations”. IN: Annual review of astronomy and astrophysics. Volume 23 (A86-14507 04–90). Palo Alto 23, 319. o. DOI:10.1146/annurev.aa.23.090185.001535.
- ↑ Cain, Fraser. „Why Old Stars Seem to Lack Lithium”, 2006. augusztus 16.
- ↑ Element Abundances. [2006. szeptember 1-i dátummal az eredetiből archiválva]. (Hozzáférés: 2009. november 17.)
- ↑ Cain, Fraser: Brown Dwarf. Universe Today. [2011. február 25-i dátummal az eredetiből archiválva]. (Hozzáférés: 2009. november 17.)
- ↑ Reid, Neill: L Dwarf Classification, 2002. március 10. [2013. május 21-i dátummal az eredetiből archiválva]. (Hozzáférés: 2013. március 6.)
- ↑ a b c U.S. Geological Survey, 2012, commodity summaries 2011: U.S. Geological Survey
- ↑ Lithium Occurrence. Institute of Ocean Energy, Saga University, Japan. [2009. május 2-i dátummal az eredetiből archiválva]. (Hozzáférés: 2009. március 13.)
- ↑ a b c d Some Facts about Lithium. ENC Labs. [2011. július 10-i dátummal az eredetiből archiválva]. (Hozzáférés: 2010. október 15.)
- ↑ Extraction of metals from sea water. Springer Berlin Heidelberg, 1984
- ↑ Atkins, Peter. Shriver & Atkins' Inorganic Chemistry, 5, W. H. Freeman and Company, 296. o. (2010). ISBN 0199236178
- ↑ Moores, S. (2007. június 1.). „Between a rock and a salt lake”. Industrial Minerals 477, 58. o.
- ↑ Taylor, S. R.; McLennan, S. M.;. The continental crust: Its composition and evolution. Oxford: Blackwell Sci. Publ., 330. o. (1985. április 26.)
- ↑ Garrett, Donald. Handbook of Lithium and Natural Calcium. Academic Press (2004) hivatkozva: The Trouble with Lithium 2. Meridian International Research, 2008
- ↑ Clarke, G.M. and Harben, P.W.. Lithium Availability Wall Map (2009) hivatkozva: International Lithium Alliance. [2012. október 20-i dátummal az eredetiből archiválva].
- ↑ a b The Trouble with Lithium 2 (PDF). Meridian International Research, 2008. (Hozzáférés: 2010. szeptember 29.)
- ↑ Risen, James. „U.S. Identifies Vast Riches of Minerals in Afghanistan”, The New York Times, 2010. június 13. (Hozzáférés: 2010. június 13.)
- ↑ „Taleban zones mineral riches may rival Saudi Arabia says Pentagon”, The Times, 2010. június 15.
- ↑ (1984) „Bioaccumulation of lithium by marine organisms in European, American, and Asian coastal zones: microanalytic study using secondary ion emission”. Comptes rendus de l'Academie des sciences. Serie III, Sciences de la vie 299 (18), 719–24. o. PMID 6440674.
- ↑ (2002) „Lithium: Occurrence, dietary intakes, nutritional essentiality”. Journal of the American College of Nutrition 21 (1), 14–21. o. DOI:10.1080/07315724.2002.10719188. PMID 11838882.
- ↑ (2011) „Low-dose lithium uptake promotes longevity in humans and metazoans”. European Journal of Nutrition 50 (5), 387–9. o. DOI:10.1007/s00394-011-0171-x. PMID 21301855.
- ↑ Petalite Mineral Information. Mindat.org. (Hozzáférés: 2009. augusztus 10.)
- ↑ a b c d e f g Lithium:Historical information. (Hozzáférés: 2009. augusztus 10.)
- ↑ Weeks, Mary. Discovery of the Elements. Whitefish, Montana, United States: Kessinger Publishing, 124. o. (2003). ISBN 0-7661-3872-0. Hozzáférés ideje: 2009. augusztus 10.
- ↑ Johan August Arfwedson. Periodic Table Live!. [2010. október 7-i dátummal az eredetiből archiválva]. (Hozzáférés: 2009. augusztus 10.)
- ↑ Johan Arfwedson. [2008. június 5-i dátummal az eredetiből archiválva]. (Hozzáférés: 2009. augusztus 10.)
- ↑ a b c van der Krogt, Peter: Lithium. Elementymology & Elements Multidict. (Hozzáférés: 2010. október 5.)
- ↑ Clark, Jim: Compounds of the Group 1 Elements, 2005. (Hozzáférés: 2009. augusztus 10.)
- ↑ a b Enghag, Per. Encyclopedia of the Elements: Technical Data – History –Processing – Applications. Wiley, 287–300. o. (2004). ISBN 978-3-527-30666-4
- ↑ Various authors (1818). „The Quarterly journal of science and the arts” (PDF). The Quarterly Journal of Science and the Arts 5, 338. o, Kiadó: Royal Institution of Great Britain. (Hozzáférés: 2010. október 5.)
- ↑ Timeline science and engineering. DiracDelta Science & Engineering Encyclopedia. [2008. december 5-i dátummal az eredetiből archiválva]. (Hozzáférés: 2008. szeptember 18.)
- ↑ A manual of chemistry. Long, 191. o. (1821). Hozzáférés ideje: 2010. október 8.
- ↑ Green, Thomas: Analysis of the Element Lithium. echeat, 2006. június 11.
- ↑ Handbook of Lithium and Natural Calcium Chloride, 99. o. (2004. április 5.). ISBN 9780080472904
- ↑ a b Ober, Joyce A.: Commodity Report 1994: Lithium. United States Geological Survey, 1994. (Hozzáférés: 2010. november 3.)
- ↑ (2003) „Lithium und seine Verbindungen – Industrielle, medizinische und wissenschaftliche Bedeutung”. Chemie in unserer Zeit 37 (4), 258. o. DOI:10.1002/ciuz.200300264.
- ↑ (1985) „Lithium – wie es nicht im Lehrbuch steht”. Chemie in unserer Zeit 19 (5), 167. o. DOI:10.1002/ciuz.19850190505.
- ↑ Ober, Joyce A.: Minerals Yearbook 2007 : Lithium. United States Geological Survey, 1994. (Hozzáférés: 2010. november 3.)
- ↑ Kogel, Jessica Elzea. Lithium, Industrial minerals & rocks: commodities, markets, and uses. Littleton, Colo.: Society for Mining, Metallurgy, and Exploration, 599. o. (2006). ISBN 978-0-87335-233-8
- ↑ McKetta, John J.. Encyclopedia of Chemical Processing and Design: Volume 28 – Lactic Acid to Magnesium Supply-Demand Relationships. M. Dekker (2007. július 18.). ISBN 978-0-8247-2478-8. Hozzáférés ideje: 2010. szeptember 29.
- ↑ szerk.: Alexandre Chagnes, Jolanta Swiatowska: Lithium Process Chemistry: Resources, Exraction, Batteries, and Recycling, 81–82. o. (2015)
- ↑ Greenwood, N.N.. Az elemek kémiája, 1., Budapest: Nemzeti Tankönyvkiadó, 73. o. (1999). ISBN 963-18-9144-5
- ↑ Ober, Joyce A: Lithium (PDF) pp. 77–78. United States Geological Survey. (Hozzáférés: 2007. augusztus 19.)
- ↑ TőzsdeFórum: Erre a fémre érdemes lesz figyelni, 2014. január 3. [2015. szeptember 12-i dátummal az eredetiből archiválva]. (Hozzáférés: 2014. február 12.)
- ↑ a b Romero, Simon. „In Bolivia, a Tight Grip on the Next Big Resource”, New York Times, 2009. február 2.
- ↑ USGS Mineral Commodities Summaries 2009. USGS
- ↑ Money Game Contributors: New Wyoming Lithium Deposit. Business Insider, 2013. április 26. (Hozzáférés: 2013. május 1.)
- ↑ Parker, Ann. Mining Geothermal Resources Archiválva 2017. május 2-i dátummal a Wayback Machine-ben. Lawrence Livermore National Laboratory
- ↑ Patel, P. (2011-11-16) Startup to Capture Lithium from Geothermal Plants. technologyreview.com
- ↑ Wald, M. (2011-09-28) Start-Up in California Plans to Capture Lithium, and Market Share. The New York Times
- ↑ Study finds resource constraints should not be a limiting factor for large-scale EV battery production. Green Car Congress, 2011. június 17. (Hozzáférés: 2011. június 17.)
- ↑ University of Michigan and Ford researchers see plentiful lithium resources for electric vehicles. Green Car Congress, 2011. augusztus 3. (Hozzáférés: 2011. augusztus 11.)
- ↑ http://www.origo.hu/gazdasag/20180123-kina-bevasarolja-magat-vilag-legfontosabb-litiumbanyai.html
- ↑ Lithium Statistics and Information, U.S. Geological Survey, 2017, <http://minerals.usgs.gov/minerals/pubs/commodity/lithium/>
- ↑ PORTFOLIO.HU - Online gazdasági újság. www.portfolio.hu. (Hozzáférés: 2018. március 6.)
- ↑ a b USGS. „Lithium” (PDF) (Hozzáférés: 2012. november 3.)
- ↑ Worldwide demand by sector. [2014. szeptember 7-i dátummal az eredetiből archiválva]. (Hozzáférés: 2014. február 16.)
- ↑ Some Compounds of the Group 1 Elements. chemguide.co.uk , 2005. (Hozzáférés: 2013. augusztus 8.)
- ↑ Disposable Batteries - Choosing between Alkaline and Lithium Disposable Batteries. Batteryreview.org. (Hozzáférés: 2013. október 10.)
- ↑ Battery Anodes > Batteries & Fuel Cells > Research > The Energy Materials Center at Cornell. Emc2.cornell.edu. (Hozzáférés: 2013. október 10.)
- ↑ Totten, George E.; Westbrook, Steven R. and Shah, Rajesh J.. Fuels and lubricants handbook: technology, properties, performance, and testing, Volume 1. ASTM International, 559. o. (2003). ISBN 0-8031-2096-6
- ↑ Rand, Salvatore J.. Significance of tests for petroleum products. ASTM International, 150–152. o. (2003). ISBN 0-8031-2097-4
- ↑ Aluminum and aluminum alloys. ASM International, 121–. o. (1993). ISBN 978-0-87170-496-2. Hozzáférés ideje: 2011. május 16.
- ↑ Mulloth, L.M. and Finn, J.E.. Air Quality Systems for Related Enclosed Spaces: Spacecraft Air, The Handbook of Environmental Chemistry, 383–404. o.. DOI: 10.1007/b107253 (2005)
- ↑ Application of lithium chemicals for air regeneration of manned spacecraft. Lithium Corporation of America & Aeropspace Medical Research Laboratories, 1965. [2012. október 7-i dátummal az eredetiből archiválva]. (Hozzáférés: 2014. február 16.)
- ↑ Lithium Perchlorate Oxygen Candle. Pyrochemical Source of Pure Oxygen - I&EC Product Research and Development (ACS Publications). Pubs.acs.org, 2002. május 1. (Hozzáférés: 2013. október 10.)
- ↑ Wiberg, Egon; Wiberg, Nils and Holleman, Arnold Frederick Inorganic chemistry, Academic Press (2001) ISBN 0-12-352651-5, p. 1089
- ↑ Hobbs, Philip C. D.. Building Electro-Optical Systems: Making It All Work. John Wiley and Sons, 149. o. (2009). ISBN 0-470-40229-6
- ↑ Point Defects in Lithium Fluoride Films Induced by Gamma Irradiation. World Scientific, 819. o. (2002). ISBN 981-238-180-5
- ↑ (1962) „Infrared Spectroscopy of Planets and Stars”. Applied Optics 1 (2), 105. o. DOI:10.1364/AO.1.000105.
- ↑ You’ve got the power: the evolution of batteries and the future of fuel cells (PDF). Toshiba. [2011. július 17-i dátummal az eredetiből archiválva]. (Hozzáférés: 2009. május 17.)
- ↑ Organometallics. IHS Chemicals, 2012. február 1.
- ↑ Yurkovetskii, A. V. (2005). „Polymerization of 1,2-dimethylenecyclobutane by organolithium initiators”. Russian Chemical Bulletin 37 (9), 1782–1784. o. DOI:10.1007/BF00962487.
- ↑ Quirk, Roderic P. (1986). „Functionalization of polymeric organolithium compounds. Amination of poly(styryl)lithium”. Macromolecules 19 (5), 1291. o. DOI:10.1021/ma00159a001.
- ↑ Stone, F. G. A.; West, Robert. Advances in organometallic chemistry. Academic Press, 55. o. (1980). ISBN 0-12-031118-6
- ↑ Bansal, Raj K.. Synthetic approaches in organic chemistry, 192. o. (1996). ISBN 0-7637-0665-5
- ↑ LiAl-hidrid. [2003. június 28-i dátummal az eredetiből archiválva]. (Hozzáférés: 2014. február 16.)
- ↑ Hughes, T.G.; Smith, R.B. and Kiely, D.H. (1983). „Stored Chemical Energy Propulsion System for Underwater Applications”. Journal of Energy 7 (2), 128–133. o. DOI:10.2514/3.62644.
- ↑ Emsley, John. Nature's Building Blocks (2011)
- ↑ Makhijani, Arjun and Yih, Katherine. Nuclear Wastelands: A Global Guide to Nuclear Weapons Production and Its Health and Environmental Effects. MIT Press, 59–60. o. (2000). ISBN 0-262-63204-7
- ↑ National Research Council (U.S.). Committee on Separations Technology and Transmutation Systems. Nuclear wastes: technologies for separations and transmutation. National Academies Press, 278. o. (1996). ISBN 0-309-05226-2
- ↑ Barnaby, Frank. How nuclear weapons spread: nuclear-weapon proliferation in the 1990s. Routledge, 39. o. (1993). ISBN 0-415-07674-9
- ↑ (1974) „The chemistry and thermodynamics of molten salt reactor fuels”. Journal of Nuclear Materials 51, 149. o. DOI:10.1016/0022-3115(74)90124-X.
- ↑ Agarwal, Arun. Nobel Prize Winners in Physics. APH Publishing, 139. o. (2008). ISBN 81-7648-743-0
- ↑ "'Splitting the Atom': Cockcroft and Walton, 1932: 9. Rays or Particles?" Archiválva 2012. szeptember 2-i dátummal a Wayback Machine-ben Department of Physics,University of Cambridge
- ↑ MATTHEW L. WALD. „Report Says a Shortage of Nuclear Ingredient Looms”, New York Times, 2013. október 8.
- ↑ a b Kean, Sam. The Disappearing Spoon (2011)
- ↑ Allan H. Young (2011). „More good news about the magic ion: lithium may prevent dementia”. The British Journal of Psychiatry 198, 336–337. o. DOI:10.1192/bjp.bp.110.082875.
- ↑ Yacobi S, Ornoy A (2008). „Is lithium a real teratogen? What can we conclude from the prospective versus retrospective studies? A review”. Isr J Psychiatry Relat Sci 45 (2), 95–106. o. PMID 18982835.
- ↑ Furr, A. K.. CRC handbook of laboratory safety. Boca Raton: CRC Press, 244–246. o. (2000). ISBN 978-0-8493-2523-6
- ↑ Bro, Per and Levy, Samuel C.. Battery hazards and accident prevention. New York: Plenum Press, 15–16. o. (1994). ISBN 978-0-306-44758-7
- ↑ TSA: Safe Travel with Batteries and Devices. Tsa.gov, 2008. január 1. [2012. január 4-i dátummal az eredetiből archiválva].
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben a Lithium című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
További információk[szerkesztés]
- Lítium, a jövő olaja - Képriport a lítium kitermeléséről és jövőjéről (index.hu).
- Lítium a The Periodic Table of Videos c. műsorban (Nottinghami Egyetem).
- Nemzetközi Lítium Szövetség
- USGS: Lítium statisztikák és információ
- Lithium Supply & Markets 2009 IM Conference 2009 Sustainable lithium supplies through 2020 in the face of sustainable market growth
- University of Southampton, Mountbatten Centre for International Studies, Nuclear History Working Paper No5.
- a magyar Wikipédia lítiumot tartalmazó vegyületeinek listája külső keresővel
- a magyar Wikipédia biner lítiumvegyületeinek listája külső keresővel








