Xenon
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Általános | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Név, vegyjel, rendszám | xenon, Xe, 54 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Latin megnevezés | xenon | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elemi sorozat | nemesgázok | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Csoport, periódus, mező | 18, 5, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Megjelenés | színtelen
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomtömeg | 131,293(6) g/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronszerkezet | [Kr] 4d10 5s2 5p6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronok héjanként | 2, 8, 18, 18, 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Halmazállapot | gáz | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sűrűség | (0 °C, 101,325 kPa) 5,894 g/l | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hármaspont | 161,36 K, 81 500 Pa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olvadáspont | 161,4 K (-111,7 °C, -169,1 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forráspont | 165,03 K (-108,12 °C, -162,62 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olvadáshő | 2,27 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Párolgáshő | 12,64 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moláris hőkapacitás | (25 °C) 20,786 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritikus nyomás | 5,84 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritikus hőmérséklet | 289,8 K (16,6 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomi tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristályszerkezet | köbös lapcentrált | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidációs szám | 0, +2, +4, +6 (ritkán több mint 0) (gyengén savas oxid) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitás | 2,6 (Pauling-skála) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizációs energia | 1.: 1170,4 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.: 2046,4 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.: 3099,4 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomsugár (számított) | 108 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalens sugár | 130 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals-sugár | 216 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Egyebek | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mágnesség | nem mágneses | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hőmérséklet-vezetési tényező | (300 K) 5,65 mW/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hangsebesség | (liquid) 1090 m/s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-szám | 7440-63-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-kód | N01AX15, V09EX02, V09EX03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fontosabb izotópok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hivatkozások | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A xenon (INN) egy kémiai elem, vegyjele Xe, rendszáma 54. Színtelen, szagtalan, nehéz nemesgáz, előfordul kis mennyiségben a Föld atmoszférájában is[1] (9·10−5 térfogatszázalék, 4·10−5 tömegszázalék). Bár kémiailag általában közömbös, ismert néhány reakciója, például melynek során xenon-hexafluoroplatinát, az elsőként előállított nemesgázvegyület keletkezik.[2][3][4]
A természetben előforduló xenonnak kilenc stabil izotópja van. Ezen felül további 40 nem stabil, radioaktív izotópja létezik. A xenon izotópjainak aránya fontos eszköz a Naprendszer történetének vizsgálatakor.[5] A xenon-135 maghasadás következtében jön létre, és az atomreaktorokban neutronelnyelőként viselkedik.[6]
A xenont ívlámpákban[7] és vakukban,[8] illetve általános érzéstelenítőként is alkalmazzák.[9] Az első excimerlézerek xenon dimer molekulát (Xe2) használtak aktív közegként,[10] az első lézerekben pedig xenon villanólámpákat használtak pumpálásra.[11] A xenont a feltételezett gyengén kölcsönható nehéz elemi részecskék (WIMP-ek) felkutatásában is alkalmazzák,[12] valamint ezt használják az űreszközök ionhajtóművének hajtóanyagaként.[13]
Története[szerkesztés]

A xenont William Ramsay és Morris Travers fedezte fel 1898. július 12-én Angliában, nem sokkal azután, hogy felfedezték a kriptont és a neont. A cseppfolyósított levegő elpárologtatása után visszamaradt anyagban találták meg.[14][15] Ramsay azt javasolta, hogy az idegen, külföldi vagy vendég jelentésű, görög eredetű xenos semleges nemű változata után xenonnak (ξένον) nevezzék el az új elemet.[16][17] 1902-ben Ramsey úgy becsülte, a xenon alkotja a Föld atmoszférájának húszmilliomod részét.[18]
Az 1930-as években Harold Edgerton mérnök elkezdte felkutatni a villódzó fény technológiáját, ami a gyors fényképezéshez elengedhetetlen volt. Így jutott el a xenonvaku feltalálásáig, amiben úgy hoz létre fényt, hogy egy xenongázzal töltött csövön keresztül elektromosságot vezet keresztül. Ezzel a technológiával 1934-ben Edgerton már egy mikromásodperces hosszúságú villanást is képes volt előállítani.[7][19][20]
1939-ben ifjabb Albert R. Behnke elkezdte a mélytengeri búvároknál a merüléssel összefüggésben kialakuló „részegség” okait kutatni. Alanyain úgy kísérletezett, hogy különböző levegőkeverékeket kellett belélegezniük, és felfedezte, hogy ez okozza a búvárok mélységérzetének változását. Eredményeiből azt a következtetést vonta le, hogy a xenongázt lehet érzéstelenítőként alkalmazni. Bár Oroszországban Lazarev már 1941-ben tanulmányozta a xenon érzéstelenítő hatásait, először a nemesgáz ilyen hatását 1946-ban J. H. Lawrence egyik tanulmánya erősítette meg. Ő egereken végzett kísérleteket. A xenont műtéti érzéstelenítőként először 1951-ben Stuart C. Cullen alkalmazta, aki ennek segítségével két páciensen sikeresen műtétet hajtott végre.[21]
1960-ban John H. Reynolds felfedezte, hogy több meteorit esetében izotópanomália mutatható ki, mivel túl sok xenon-129-et tartalmaznak. Mindebből arra következtetett, hogy ez a 129I radioaktív bomlásterméke lehet. Ezt az izotópot a kozmikus sugárzás által kiváltott hasadás és a maghasadás következtében időben lassan jött létre, nagy mennyiségben azonban csak egy szupernóva felrobbanásakor jöhet létre. Mivel a 129I felezési ideje kozmikus egységekben mérve rövid – csupán 16 millió év –, ebből az következik, hogy rövid idő telt el a robbanás és a meteoritok megszilárdulása között. A két esemény (a szupernóva-robbanás és a gázfelhő megszilárdulása) között eltelt idő azt bizonyítja, hogy ezek a Naprendszer történetének kezdetekor történtek, mivel a 129I-izotóp valószínűleg a Naprendszer kialakulása előtt nem sokkal létrejött, és a napgáz felhőjét egy másik izotópforrás telítette be.[22][23]
Hosszú ideig úgy gondolták, hogy a xenon és a hozzá hasonló többi nemesgáz kémiailag közömbös, és nem alkotnak vegyületeket. Azonban Neil Bartlett mialatt a University of British Columbia oktatója volt, felfedezte, hogy a platina-hexafluorid (PtF6) olyan erős oxidálószer, hogy oxidálni képes az oxigén gázt (O2), dioxigenil-hexafluoroplatinát képződése (O+2[PtF6]−) közben.[24] Mivel az O2 és a xenon első ionizációs energiája majdnem megegyezik, Bartlett felismerte, hogy a platina-hexafluorid képes lehet a xenont is oxidálni. 1962. március 23-án elegyítette a két gázt, és létrehozta az első ismert, nemesgáztartalmú vegyületet, a xenon-hexafluoroplatinátot.[25][4] Bartlett úgy gondolta, hogy ennek képlete Xe+[PtF6]− lehet, de későbbi munkák kimutatták, hogy valószínűleg különböző xenontartalmú sók keveréke lehetett.[26][27][28] Azóta számos más xenonvegyületet fedeztek fel,[29] és több más nemesgáznak – így például az argonnak, a radonnak és a kriptonnak – is kimutatták már vegyületeit. Ezek közé tartozik az argon-fluorohidrid (HArF),[30] a kripton-difluorid (KrF2),[31][32] és a radon-difluorid.[33]
Előfordulása[szerkesztés]
A xenon a Föld légkörében nyomgáznak számít, aránya 0,087±0,001 ppm (μl/l), vagy nagyjából 1:11 500 000 arányban fordul elő,[34] és megtalálták forrásokból kijövő gázok között is. A xenon néhány radioaktív változata, mint például a 133Xe és a 135Xe úgy jön létre, hogy neutronnal besugározzák a reaktorban lévő hasadóanyagot.[2]
A xenont általában a levegő oxigénre és nitrogénre történő szétválasztásának melléktermékeként állítják elő. Miután a forráspontok eltérését kihasználva külön edényekben összegyűjtötték a nitrogént és a folyékony oxigént, az utóbbiban kis mennyiségű kriptont és xenont lehet találni. Egy újabb, hasonló hátterű szétválasztás során az oxigént fel lehet úgy dúsítani, hogy 0,1–0,2% kripton/xenon együttes koncentrációt lehessen kimutatni. Ezt szilikagél vagy desztilláció segítségével ki lehet nyerni a folyadékból. Végül a kripton/xenon keveréket egy újabb desztillációval lehet részeire szedni.[35][36] A levegőből egy liter xenon kinyeréséhez 220 wattóra energiára van szükség.[37] A világ xenontermelését 1998-ban 5000–7000 m³-re becsülték.[38] Alacsony koncentrációjának köszönhetően a xenon sokkal drágább, mint a nála könnyebb nemesgázok. 1999-ben Európában 1 liter xenon ára 10, míg a kriptoné 1, a neoné pedig 0,2 euró volt.[38]
A xenon a Nap, a Föld atmoszférájában valamint az aszteroidákban és az üstökösökben viszonylag ritka. A Mars légrétegében a xenon koncentrációja hasonlít a földi értékhez, 0,08 milliomod rész,[39] azonban itt nagyobb a 129Xe aránya mint akár a Földön akár a Napnál. Mivel ez az izotóp radioaktív bomlás eredményeképpen jön létre, az eredmény arra utalhat, hogy a Mars a kialakulását követő első 100 millió év során elvesztette légkörének jelentős részét.[40][41] Ezzel ellentétben a Jupiter légkörének kimagaslóan nagy a xenontartalma, 2,6-szor annyi, mint a Napé.[42] A magas koncentráció oka egyelőre ismeretlen, de lehet, hogy a korai és gyors bolygóképződés lehetett, melynek során sok apró, csillagászati mérték alatti test jött létre. Ez még azelőtt történhetett, hogy Naprendszerünk protoplanetáris korongja elkezdett volna fölmelegedni.[43] (Máskülönben nem lehetett volna xenont észlelni a bolygóképződés korabeli jégben.) A Naprendszerben a xenon összes izotópjának a Naprendszer teljes tömegéhez viszonyított aránya 1,56·10−8.[44] Az alacsony földi xenonszint részben talán azzal is lehet magyarázható, hogy a kvarcban a xenon kovalens kötéssel kapcsolódik az oxigénhez, és emiatt távozik kevesebb xenon a légkörbe.[45]
A többi, kisebb tömegű nemesgázzal ellentétben a csillagokban lejátszódó megszokott nukleoszintézis során xenon nem jön létre. Az 56-os rendszámú vasnál nehezebb atomok fúziós előállításához olyan sok energia szükséges, hogy abból a csillag nem jut energiához, ha xenont hoz létre.[46] Ezzel ellentétben szupernóva-robbanás után nagy mennyiségben lehet xenont mérni.[47]
Jellemzői[szerkesztés]
Egy xenonatomnak 54 protonja van. Standard hőmérsékleten és nyomáson a közönséges xenongáz sűrűsége 5,761 kg/m³, ami nagyjából négy és félszerese a földi légkör felszíni 1,217 kg/m³-es sűrűségének.[48] Folyadékként sűrűsége elérheti a 3,100 g/ml értéket is. A legmagasabb ez az érték a hármaspontjánál.[49] Hasonló körülmények között a szilárd xenon sűrűsége – 3,64 g/cm³ – nagyobb, mint a gránit 2,75 g/cm³-es átlagos sűrűsége.[49] Több gigapascal nyomás alkalmazásával a xenon fémes fázisba kényszerül.[50]
A szilárd xenon lapcentrált köbös rácsa nyomás hatására szoros illeszkedésű hexagonális kristályokká alakul, és 140 GPa környékén fémes jellegűvé kezd válni anélkül, hogy a hexagonális fázis térfogata észrevehetően megváltozna. 155 GPa nyomás alatt a xenon teljesen fémessé válik. A fémes xenon égkék színű, mivel elnyeli a vörös fényt, és a átengedi a látható fény más frekvenciájú sugarait. Ez a viselkedés a fémek esetén szokatlan, és az a magyarázata, hogy a fémes xenon elektronsávjai között viszonylag kicsi a távolság.[51][52]
Tulajdonságai[szerkesztés]
A xenonnak nincs szabad vegyértékelektronja ezért nemesgáznak vagy a technikában inert gáznak hívják,ennek ellenére a xenonnak legalább 80 vegyülete ismert. Egy gázzal töltött csőben a xenon kék fénnyel sugároz, a gáz részecskéinek elektromos gerjesztése következtében.
Forráspontja nagy atomtömege ellenére is nagyon alacsony (150 K alatt van).[53]
Vegyületei[szerkesztés]
Neil Bartlett 1962-es felfedezése után, mely szerint a xenon képes kémiai vegyületeket képezni, nagy számú xenonvegyületet fedeztek fel és írtak le. Csaknem minden ismert xenonvegyületben előfordul a nagy elektronegativitású fluor- vagy oxigénatom.[54]
Halogenidek[szerkesztés]
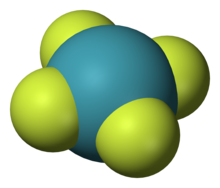

A xenonnak három fluoridja ismert: XeF2, XeF4 és XeF6. Csaknem minden xenon vegyület szintézise fluoridokból indul ki.
A szilárd, kristályos difluorid XeF2 fluor és xenongáz keverékéből képződik ultraibolya fény hatására.[55] A reakcióhoz normál napfény is elegendő.[56] A XeF2 nagy hőmérsékleten, hosszú ideig tartó melegítésével NiF2 katalizátor jelenlétében XeF6 keletkezik.[57] XeF6 NaF jelenlétében végzett hőbontása során nagy tisztaságú XeF4 jön létre.[58]
A xenon-fluoridok fluoridion akceptorként és donorként viselkednek, így például XeF+ és Xe2F3+ kationokat, valamint XeF5−, XeF7− és XeF82− anionokat tartalmazó sókat képezhetnek. A zöld színű, paramágneses Xe2+ a XeF2 xenongázzal történő redukciója során keletkezik.[54]
A XeF2 átmenetifém-ionokkal koordinációs komplexek képzésére is képes. Eddig több mint 30 ilyen komplexet állítottak elő és jellemeztek.[57]
Míg a xenon fluoridjai jól leírt vegyületek, a többi halogenid – a XeCl2 kivételével – nem ismert. A beszámolók szerint a xenon-diklorid endoterm, színtelen, kristályos vegyület, ami 80 °C-on elemeire bomlik. Xenon, fluor és szilícium- vagy szén-tetraklorid keverékének nagyfrekvenciás besugárzásával állítható elő.[59] Kétségek merültek fel azonban azzal kapcsolatban, hogy a XeCl2 valódi vegyület-e, vagy csak egy van der Waals-molekula, mely gyengén kötött Xe-atomokat és Cl2-molekulákat tartalmaz.[60] Elméleti számítások alapján a XeCl2 lineáris molekula kevésbé stabil, mint a van der Waals komplex.[61]
Oxidok és oxohalogenidek[szerkesztés]
A xenonnak három oxidja ismert: a xenon-trioxid (XeO3) és a xenon-tetroxid (XeO4), melyek rendkívül robbanásveszélyes, erélyes oxidálószerek, valamint a négyes koordinációs számmal jellemzett xenon-dioxid, melyről 2011-ben számoltak be.[62] A XeO2 xenon-tetrafluorid jégre történő kiöntésekor keletkezik. Kristályszerkezete olyan, hogy lehetővé teheti a szilícium helyettesítését a szilikát ásványokban.[63] A XeOO+ kationt azonosították szilárd argonban infravörös spektroszkópia segítségével.[64]
A xenon közvetlenül nem reagál oxigénnel, a trioxid a XeF6 hidrolízise során keletkezik:[65]
- XeF6 + 3 H2O → XeO3 + 6 HF
A XeO3 gyenge sav, lúgokban instabil xenát sók keletkezése közben oldódik, ezekben HXeO−4 anion található. Ezek az instabil sók könnyen diszproporcionálódnak xenon gázzá és perxenát sókká, melyek XeO4−6 aniont tartalmaznak.[66]
Bárium-perxenátból tömény kénsavval reagáltatva előállítható a gázállapotú xenon-tetroxid:[59]
- Ba2XeO6 + 2 H2SO4 → 2 BaSO4 + 2 H2O + XeO4
A bomlás megakadályozására az így előállított xenon-tetroxidot gyorsan lehűtik, a kapott halványsárga szilárd anyag −35,9 °C feletti hőmérsékleten robbanásszerűen xenon és oxigén gázra bomlik.
Számos xenon-oxifluorid ismert,[67] ezek közé tartozik a XeOF2, a XeOF4, a XeO2F2 és a XeO3F2. XeOF2 OF2 és xenon gáz alacsony hőmérsékleten végrehajtott reakciójában keletkezik. Előállítható XeF4 részleges hidrolízisével is. −20 °C-on XeF2 és XeO2F2 képződése közben diszproporcionálódik.[68] XeOF4 a XeF6 részleges hidrolízise során [69] vagy XeF6 és nátrium-perxenát (Na4XeO6) reakciójában keletkezik. Az utóbbi reakcióban kis mennyiségben XeO3F2 is képződik. A XeOF4 CsF-dal reagálva XeOF−5 aniont képez,[68][70] míg a XeOF3-ból alkálifém-fluoridokkal – KF, RbF és CsF – reagálva XeOF−4 anion keletkezik.[71]
Felhasználási területek[szerkesztés]
Ezt a gázt a legszélesebb körben xenonlámpa töltőgázaként alkalmazzák. Ilyen berendezést tartalmaznak többek között egyes vakuk és stroboszkópok. A xenonívlámpák színhőmérséklete megközelítőleg azonos a déli napéval, ezért napszimulátorokban, és például IMAX filmvetítő rendszerekben is használatosak. Az újfajta ionhajtóművek előszeretettel használják üzemanyagként.
Jegyzetek[szerkesztés]
- ↑ Staff: Xenon. Columbia Electronic Encyclopedia. Columbia University Press, 2007. (Hozzáférés: 2007. október 23.)
- ↑ a b Husted, Robert; Boorman, Mollie: Xenon. Los Alamos National Laboratory, Chemical Division, 2003. december 15. [2010. november 22-i dátummal az eredetiből archiválva]. (Hozzáférés: 2007. szeptember 26.)
- ↑ Rabinovich, Viktor Abramovich. Thermophysical properties of neon, argon, krypton, and xenon, English-language, Washington, DC: Hemisphere Publishing Corp. (1988). ISBN 0195218337. Hozzáférés ideje: 2009. április 2.–National Standard Reference Data Service of the USSR. Volume 10.
- ↑ a b Freemantel, Michael: Chemistry at its Most Beautiful (PDF). Chemical & Engineering News, 2003. augusztus 25. (Hozzáférés: 2007. szeptember 13.)
- ↑ Kaneoka, Ichiro (1998). „Xenon's Inside Story”. Science 280 (5365), 851–852. o. DOI:10.1126/science.280.5365.851b. (Hozzáférés: 2007. október 10.)
- ↑ Stacey, Weston M.. Nuclear Reactor Physics. Wiley-VCH, 213. o. (2007). ISBN 3527406794
- ↑ a b Burke, James. Twin Tracks: The Unexpected Origins of the Modern World. Oxford University Press, 33. o. (2003). ISBN 0743226194
- ↑ Mellor, David. Sound Person's Guide to Video. Focal Press, 186. o. (2000). ISBN 0240515951
- ↑ Sanders, Robert D.; Ma, Daqing; Maze, Mervyn (2005). „Xenon: elemental anaesthesia in clinical practice”. British Medical Bulletin 71 (1), 115–135. o. DOI:10.1093/bmb/ldh034. PMID 15728132. (Hozzáférés: 2007. október 2.)
- ↑ Basov, N. G., Danilychev, V. A.; Popov, Yu. M. (1971). „Stimulated Emission in the Vacuum Ultraviolet Region”. Soviet Journal of Quantum Electronics 1 (1), 18–22. o. [2020. május 16-i dátummal az eredetiből archiválva]. DOI:10.1070/QE1971v001n01ABEH003011. (Hozzáférés: 2009. június 5.)
- ↑ Toyserkani, E., Khajepour, A.; Corbin, S.. Laser Cladding. CRC Press, 48. o. (2004). ISBN 0849321727
- ↑ Ball, Philip: Xenon outs WIMPs. Nature, 2002. május 1. (Hozzáférés: 2007. október 8.)
- ↑ Saccoccia, G., del Amo, J. G.; Estublier, D.. „Ion engine gets SMART-1 to the Moon”, ESA, 2006. augusztus 31. (Hozzáférés: 2007. október 1.)
- ↑ W. Ramsay and M. W. Travers (1898). „On the extraction from air of the companions of argon, and neon”. Report of the Meeting of the British Association for the Advancement of Science, 828. o.
- ↑ Gagnon, Steve: It's Elemental - Xenon. Thomas Jefferson National Accelerator Facility. (Hozzáférés: 2007. június 16.)
- ↑ Anonymous.szerk.: Daniel Coit Gilman, Harry Thurston Peck, Frank Moore Colby: The New International Encyclopædia. Dodd, Mead and Company, 906. o. (1904)
- ↑ Staff. The Merriam-Webster New Book of Word Histories. Merriam-Webster, Inc., 513. o. (1991). ISBN 0877796033
- ↑ Ramsay, William (1902). „An Attempt to Estimate the Relative Amounts of Krypton and of Xenon in Atmospheric Air”. Proceedings of the Royal Society of London 71, 421–426. o. DOI:10.1098/rspl.1902.0121. (Hozzáférés: 2007. október 2.)
- ↑ Anonymous: History. Millisecond Cinematography. [2006. augusztus 22-i dátummal az eredetiből archiválva]. (Hozzáférés: 2007. november 7.)
- ↑ Paschotta, Rüdiger: Lamp-pumped lasers. Encyclopedia of Laser Physics and Technology. RP Photonics, 2007. november 1. (Hozzáférés: 2007. november 7.)
- ↑ Marx, Thomas; Schmidt, Michael; Schirmer, Uwe; Reinelt, Helmut (2000). „Xenon anesthesia” (PDF). Journal of the Royal Society of Medicine 93, 513–517. o. (Hozzáférés: 2007. október 2.)
- ↑ Clayton, Donald D.. Principles of Stellar Evolution and Nucleosynthesis. University of Chicago Press, 75 edition=2nd. o. (1983). ISBN 0226109534
- ↑ Bolt, B. A.; Packard, R. E.; Price, P. B.: John H. Reynolds, Physics: Berkeley. The University of California, Berkeley, 2007. (Hozzáférés: 2007. október 1.)
- ↑ {{cite journal title=Dioxygenyl hexafluoroplatinate (V), O+2[PtF6]− | author=Bartlett, Neil; Lohmann, D. H. | journal=Proceedings of the Chemical Society | publisher=Chemical Society | location=London | issue=3 | page=115 | month=March | year=1962 | doi = 10.1039/PS9620000097}}
- ↑ Bartlett, N. (1962. June). „Xenon hexafluoroplatinate (V) Xe+[PtF6]‒”. Proceedings of the Chemical Society, London (6), 218. o, Kiadó: Chemical Society. DOI:10.1039/PS9620000197.
- ↑ Graham, L., Graudejus, O.; Jha N.K.; Bartlett, N. (2000). „Concerning the nature of XePtF6”. Coordination Chemistry Reviews 197, 321–334. o. DOI:10.1016/S0010-8545(99)00190-3.
- ↑ p. 392, §11.4, Inorganic Chemistry, translated by Mary Eagleson and William Brewer, edited by Bernhard J. Aylett, San Diego: Academic Press, 2001, ISBN 0-12-352651-5; translation of Lehrbuch der Anorganischen Chemie, originally founded by A. F. Holleman, continued by Egon Wiberg, edited by Nils Wiberg, Berlin: de Gruyter, 1995, 34th edition, ISBN 3-11-012641-9.
- ↑ Steel, Joanna: Biography of Neil Bartlett. College of Chemistry, University of California, Berkeley, 2007. [2007. július 8-i dátummal az eredetiből archiválva]. (Hozzáférés: 2007. október 25.)
- ↑ Bartlett, Neil (2003. szeptember 9.). „The Noble Gases”. Chemical & Engineering News 81 (36), Kiadó: American Chemical Society. (Hozzáférés: 2007. október 1.)
- ↑ Khriachtchev, Leonid, Pettersson, Mika; Runeberg, Nino; Lundell, Jan; Räsänen, Markku (2000. augusztus 24.). „A stable argon compound”. Nature 406, 874–876. o. DOI:10.1038/35022551. (Hozzáférés: 2008. június 4.)
- ↑ Lynch, C. T.; Summitt, R.; Sliker, A.. CRC Handbook of Materials Science. CRC Press (1980). ISBN 0-87819-231-X
- ↑ D. R. MacKenzie (1963. szeptember 20.). „Krypton Difluoride: Preparation and Handling”. Science 141 (3586), 1171. o. DOI:10.1126/science.141.3586.1171. PMID 17751791.
- ↑ Paul R. Fields, Lawrence Stein, and Moshe H. Zirin (1962). „Radon Fluoride”. Journal of the American Chemical Society 84 (21), 4164–4165. o. DOI:10.1021/ja00880a048.
- ↑ Hwang, Shuen-Cheng, Robert D. Lein, Daniel A. Morgan. Noble Gases, Kirk-Othmer Encyclopedia of Chemical Technology, 5th, Wiley. DOI: 10.1002/0471238961.0701190508230114.a01 (2005). ISBN 047148511X
- ↑ Kerry, Frank G.. Industrial Gas Handbook: Gas Separation and Purification. CRC Press, 101–103. o. (2007). ISBN 0849390052
- ↑ Xenon - Xe. CFC StarTec LLC, 1998. augusztus 10. [2020. június 12-i dátummal az eredetiből archiválva]. (Hozzáférés: 2007. szeptember 7.)
- ↑ Singh, Sanjay: Xenon: A modern anaesthetic. Indian Express Newspapers Limited, 2005. május 15. [2007. augusztus 13-i dátummal az eredetiből archiválva]. (Hozzáférés: 2007. október 10.)
- ↑ a b Häussinger, Peter, Glatthaar, Reinhard; Rhode, Wilhelm;Kick, Helmut; Benkmann, Christian; Weber, Josef; Wunschel, Hans-Jörg; Stenke, Viktor; Leicht, Edith; Stenger, Hermann. Noble Gases, Ullmann's Encyclopedia of Industrial Chemistry, 6th, Wiley. DOI: 10.1002/14356007.a17_485 (2001). ISBN 3527201653
- ↑ Williams, David R.: Mars Fact Sheet. NASA, 2004. szeptember 1. (Hozzáférés: 2007. október 10.)
- ↑ Schilling, James: Why is the Martian atmosphere so thin and mainly carbon dioxide?. Mars Global Circulation Model Group. [2010. május 28-i dátummal az eredetiből archiválva]. (Hozzáférés: 2007. október 10.)
- ↑ Zahnle, Kevin J. (1993). „Xenological constraints on the impact erosion of the early Martian atmosphere”. Journal of Geophysical Research 98 (E6), 10,899–10,913. o. [2011. április 19-i dátummal az eredetiből archiválva]. DOI:10.1029/92JE02941. (Hozzáférés: 2007. október 10.)
- ↑ Mahaffy, P. R., Niemann, H. B.; Alpert, A.; Atreya, S. K.; Demick, J.; Donahue, T. M.; Harpold, D. N.; Owen, T. C. (2000). „Noble gas abundance and isotope ratios in the atmosphere of Jupiter from the Galileo Probe Mass Spectrometer”. Journal of Geophysical Research 105 (E6), 15061–15072. o. DOI:10.1029/1999JE001224. (Hozzáférés: 2007. október 1.)
- ↑ Owen, Tobias, Mahaffy, Paul; Niemann, H. B.; Atreya, Sushil; Donahue, Thomas; Bar-Nun, Akiva; de Pater, Imke (1999). „A low-temperature origin for the planetesimals that formed Jupiter”. Nature 402 (6759), 269–270. o. DOI:10.1038/46232. (Hozzáférés: 2007. február 4.)
- ↑ Arnett, David. Supernovae and Nucleosynthesis. Princeton, New Jersey: Princeton University Press (1996). ISBN 0-691-01147-8
- ↑ Sanloup, Chrystèle, et al.. „Retention of Xenon in Quartz and Earth's Missing Xenon”. Science 310 (5751), 1174–1177. o. DOI:10.1126/science.1119070. PMID 16293758. (Hozzáférés: 2007. október 8.)
- ↑ Clayton, Donald D.. Principles of Stellar Evolution and Nucleosynthesis. University of Chicago Press (1983). ISBN 0226109534
- ↑ Heymann, D.; Dziczkaniec, M. (Hiba: Érvénytelen idő.). „Xenon from intermediate zones of supernovae”. Proceedings 10th Lunar and Planetary Science Conference: 1943–1959, Houston, Texas: Pergamon Press, Inc.. Hozzáférés: 2007. október 2.
- ↑ Williams, David R.: Earth Fact Sheet. NASA, 2007. április 19. (Hozzáférés: 2007. október 4.)
- ↑ a b Aprile, Elena, Bolotnikov, Aleksey E.; Doke, Tadayoshi. Noble Gas Detectors. Wiley-VCH, 8–9. o. (2006). ISBN 3527609636
- ↑ Caldwell, W. A., Nguyen, J.; Pfrommer, B.; Louie, S.; Jeanloz, R. (1997). „Structure, bonding and geochemistry of xenon at high pressures”. Science 277, 930–933. o. DOI:10.1126/science.277.5328.930.
- ↑ Fontes, E.: Golden Anniversary for Founder of High-pressure Program at CHESS. Cornell University. (Hozzáférés: 2009. május 30.)
- ↑ Eremets, Mikhail I.; Gregoryanz, Eugene A.; Struzhkin, Victor V.; Mao, Ho-Kwang; Hemley, Russell J.; Mulders, Norbert; Zimmerman, Neil M. (2000). „Electrical Conductivity of Xenon at Megabar Pressures”. Physical Review Letters 85 (13), 2797–2800. o. DOI:10.1103/PhysRevLett.85.2797. PMID 10991236.
- ↑ O. SŠifner, J. Klomfar: Thermodinamic Propertes of Xenon from the Triple Point to 800 K with Pressures up to 350 MPa. nist.gov, 2008. [2012. szeptember 20-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. június 2.)
- ↑ a b Harding, Charlie; Johnson, David Arthur; Janes, Rob. Elements of the p block. Great Britain: Royal Society of Chemistry, 93–94. o. (2002). ISBN 0854046909
- ↑ Weeks, James L.; Chernick, Cedric; Matheson, Max S. (1962). „Photochemical Preparation of Xenon Difluoride”. Journal of the American Chemical Society 84, 4612. o. DOI:10.1021/ja00882a063.
- ↑ Streng, L. V.; Streng, A. G. (1965). „Formation of Xenon Difluoride from Xenon and Oxygen Difluoride or Fluorine in Pyrex Glass at Room Temperature”. Inorganic Chemistry 4 (9), 1370–1371. o. DOI:10.1021/ic50031a035.
- ↑ a b Tramšek, Melita; Žemva, Boris (2006. december 5.). „Synthesis, Properties and Chemistry of Xenon(II) Fluoride” (PDF). Acta Chimica Slovenica 53 (2), 105–116. o. [2013. május 12-i dátummal az eredetiből archiválva]. DOI:10.1002/chin.200721209. (Hozzáférés: 2009. július 18.)
- ↑ Ogrin, Tomaz; Bohinc, Matej; Silvnik, Joze (1973). „Melting-point determinations of xenon difluoride-xenon tetrafluoride mixtures”. Journal of Chemical and Engineering Data 18 (4), 402. o. DOI:10.1021/je60059a014.
- ↑ a b Scott, Thomas; Eagleson, Mary. Xenon Compounds, Concise encyclopedia chemistry. Walter de Gruyter (1994). ISBN 3110114518
- ↑ Proserpio, Davide M.; Hoffmann, Roald; Janda, Kenneth C. (1991). „The xenon-chlorine conundrum: van der Waals complex or linear molecule?”. Journal of the American Chemical Society 113, 7184. o. DOI:10.1021/ja00019a014.
- ↑ Richardson, Nancy A.; Hall, Michael B. (1993). „The potential energy surface of xenon dichloride”. The Journal of Physical Chemistry 97, 10952. o. DOI:10.1021/j100144a009.
- ↑ Brock, D.S..; Schrobilgen, G.J. (2011). „Synthesis of the missing oxide of xenon, XeO2, and its implications for earth's missing xenon”. Journal of the American Chemical Society 133 (16), 110222081739042. o. DOI:10.1021/ja110618g. PMID 21341650.
- ↑ (2011) „Chemistry: Where did the xenon go?”. Nature 471 (7337), 138–138. o. DOI:10.1038/471138d.
- ↑ Zhou, M.; Zhao, Y.; Gong, Y.; Li, J. (2006). „Formation and Characterization of the XeOO+ Cation in Solid Argon”. Journal of the American Chemical Society 128, 2504–2505. o. DOI:10.1021/ja055650n.
- ↑ Holloway, John H., Hope, Eric G..szerk.: A. G. Sykes: Advances in Inorganic Chemistry Press. Academic, 65. o. (1998). ISBN 012023646X
- ↑ Henderson, W.. Main group chemistry. Great Britain: Royal Society of Chemistry, 152–153. o. (2000). ISBN 0854046178
- ↑ szerk.: Náray-Szabó Gábor: Kémia. Budapest: Akadémiai Kiadó, 360. o. (2006). ISBN 963 05 8240 6
- ↑ a b Mackay, Kenneth Malcolm; Mackay, Rosemary Ann; Henderson, W.. Introduction to modern inorganic chemistry, 6th, CRC Press, 497–501. o. (2002). ISBN 0748764208
- ↑ Smith, D. F. (1963). „Xenon Oxyfluoride”. Science 140, 899. o. DOI:10.1126/science.140.3569.899.
- ↑ K. O. Christe, D. A. Dixon, J. C. P. Sanders, G. J. Schrobilgen, S. S. Tsai, W. W. Wilson (1995). „On the Structure of the [XeOF5]− Anion and of Heptacoordinated Complex Fluorides Containing One or Two Highly Repulsive Ligands or Sterically Active Free Valence Electron Pairs”. Inorg. Chem. 34 (7), 1868–1874. o. DOI:10.1021/ic00111a039.
- ↑ K. O. Christe, C. J. Schack, D. Pilipovich (1972). „Chlorine trifluoride oxide. V. Complex formation with Lewis acids and bases”. Inorg. Chem. 11 (9), 2205–2208. o. DOI:10.1021/ic50115a044.
További információk[szerkesztés]
- a magyar Wikipédia xenont tartalmazó vegyületeinek listája külső keresővel


