Kanyaró
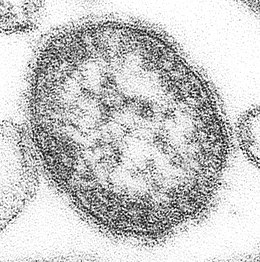
| Kanyaróvírus | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| Vírusbesorolás | ||||||||||
| ||||||||||
| Hivatkozások | ||||||||||
A Wikimédia Commons tartalmaz Kanyaróvírus témájú médiaállományokat és Kanyaróvírus témájú kategóriát. |
A kanyaró (latinul morbilli) vírus által okozott, veszélyes emberi megbetegedés. Habár népiesen vörös himlőként is emlegetik,[1] nincs köze a rózsahimlőhöz (Rubeola), a bárányhimlőhöz (Varicella) vagy a fekete himlőhöz (variola). A vírus a beteg ember váladékaival ürül, s cseppfertőzéssel terjed. A fertőződés után 9–11 nap múlva hirtelen fellépő nátha, láz, köhögés és kötőhártya-gyulladás jelentkezik, valamint a szájüregi nyálkahártyán cseresznyepiros foltok,[2] az úgynevezett Koplik-foltok jelennek meg. Később kiütések alakulnak ki a bőrön, egyúttal a láz csökken.
A betegség súlyos komplikációkkal járhat: felléphet középfül- és tüdőgyulladás, valamint különböző mechanizmusokkal kialakulhat agyvelőgyulladás (akár 15 évvel a fertőződés után is), továbbá felléphetnek egyéb bakteriális fertőzések.
A fertőzés lezajlása után egész életen át tartó immunitás alakul ki a kórokozóval szemben.
A betegség megelőzésére Magyarországon kötelező a védőoltás: a morbilli–mumps–rubeola (MMR) vakcinát a gyermekek először 15 hónaposan, majd az általános iskola VI. osztályában újra megkapják. Az oltóanyag "élő", attenuált (tehát legyengített) kanyaró-, mumpsz- és rubeola- (rózsahimlő) vírusokat tartalmaz.
Tudománytörténet[szerkesztés]
Az első adatok a kanyaróról a 7. századból származnak Al-Yehudi zsidó orvostól. Az első részletes leírást Muhammad ibn Zakarijja r-Rázi (Rhazes) perzsa orvos adta, aki szerint a kanyaró félelmetesebb betegség, mint a himlő.[3]
A középkorban sok és nagy kanyarójárvány volt, sok halottal. Amerika felfedezése után az indiánok nagy része belehalt az olyan, számukra új betegségekbe, mint a fekete himlő, kanyaró, szamárköhögés vagy tífusz. Ennek az volt az oka, hogy szervezetük egészen addig nem találkozott ezekkel a betegségekkel, ezért nem alakult ki bennük az immunitás.[4] Így kanyaró tombolt Santo Domingóban (1519), Guatemalában (1523) és Mexikóban (1531). 1529-ben Hondurasban és Közép-Amerikában a kanyaró a himlőt túlélő őslakosság kétharmadának életét követelte.[5]

A kanyaró a 19. században is sok halálos áldozatot szedett ott, ahol addig nem ismerték (és nem ismerte az ott lakók immunrendszere sem a kanyaróvírust). Így 1848-ban Hawaii 148 000 lakosa közül 40 000-en haltak meg kanyaróban, 1874-ben pedig a Fidzsi-szigetek lakóinak egynegyede esett a kanyaró áldozatául.[6]
Peter Panum dán orvos 1846-ban megállapította, hogy 1781 óta, vagyis az azt megelőző 65 évben a Färöer-szigeteken nem volt jelen a betegség. Ekkor a 7864 lakos közül 6100-an betegedtek meg kanyaróban. 99,5% betegedett meg azok közül, akik még nem éltek 1781-ben, ellenben mind a 98, 65 évnél idősebb lakos immunisnak bizonyult.[7]
Thomas Sydenhams angol lelkész a 17. században a kanyarót meg tudta különböztetni a skarláttól, és más lázzal járó fertőző betegségektől egy nagy járvány idején.[8]
1882-ben nagy feltűnést jelentett Antoine Louis Gustave Béclère műve, amiben az immunizálás céljából mesterségesen kiváltott kanyarófertőzésről írt. A 19. század francia kutatóorvosai véglegesen elkülönítették a betegséget más bőrkiütésekkel járó betegségektől. 1911-ben sikerült először majmokat kanyaróval megfertőzni. Enders és Peebles 1954-ben izolálta a vírust,[9] lehetővé téve az oltóanyag kifejlesztését. Az első oltóanyagot 1958-ban sikerült előállítani, ami a Maurice Hilleman vezette fejlesztésnek köszönhetően 1963-tól kezdve hozzáférhetővé vált széles körű orvosi használatra.
Elterjedtsége[szerkesztés]
| WHO-Region | 1980 | 1990 | 2000 | 2005 |
|---|---|---|---|---|
| Afrika | 1 240 993 | 481 204 | 520.102 | 316.224 |
| Amerika | 257 790 | 218 579 | 1 755 | 19 |
| Közel-Kelet | 341 624 | 59 058 | 38 592 | 15 069 |
| Európa | 851 849 | 234 827 | 37 421 | 37 332 |
| Délkelet-Ázsia | 199 535 | 224 925 | 61 975 | 83 627 |
| Nyugat-Óceánia | 1 319 640 | 155 490 | 176 493 | 128 016 |
| Összesen | 4 211 431 | 1 374 083 | 836 338 | 580 287 |
A kanyaróvírus világszerte elterjedt, de a betegség előfordulásának aránya nagy mértékben változó; különösen gyakoriak a járványok a fejlődő országokban. Ott a kanyaró az egyik leggyakoribb fertőző betegség, ami nagyban hozzájárul a megbetegedésekhez és a halálozáshoz.[11][12] A WHO becslése szerint 2000-ben 30-40 millióan betegedtek meg kanyaróban, és az ugyanebben az évben védőoltással megelőzhető gyermekkori betegségben meghalt 1,7 millió gyerek majdnem felének haláláért a kanyaró volt a felelős.[13] A bejelentett esetek száma ennél sokkal kisebb, ahogy a táblázat mutatja.
Az oltási kampányoknak köszönhetően ugyanakkor a vírus egyes területekről, például Amerikából majdhogynem eltűnt. Ennek a sikernek többek között az az oka, hogy a kanyaróvírus egyedüli gazdája az ember. 2001-ben a WHO és az UNICEF közös tervükben célként tűzték ki, hogy 2005-re oltási kampányokkal felére csökkentik a kanyaró miatti gyermekhalálozást. A különböző tudósítások szerint ezt a célt nagyjából el is érték, bár a pontos adatok hiányoznak. 1999 és 2003 között világszerte 39%-kal sikerült csökkenteni a halálozási arányokat, habár Afrikában és Délkelet-Ázsiában még mindig sokan halnak bele a betegségbe.[14] 2005-ben a WHO World Health Assemblyje egy új tervet fogalmazott meg, amiben a halálozási számok 90%-os csökkentését tűzték ki célul. A terv határideje 2010 volt.[15]
2009-ben az amerikai CDC (Centers for Disease Control and Prevention) jelentésében egy izraeli járványról számolt be, amiben több, mint 900-an betegedtek meg, ebből 700 Jeruzsálemben és Beit Shemeshben.[16] Dél-Afrikában 2009 óta tart a kanyarójárvány.[17]
Európában a bejelentett kanyaróbetegek száma 1990 és 2004 között nagy mértékben csökkent.[15] Az esetek aránya az átoltottságtól függően országonként nagy mértékben változó. Míg a skandináv országokban nagyon ritka (Finnországban 1996 óta négy, import eset),[18] addig Közép- és Kelet-Európában néha helyi járványok alakulnak ki a hiányos átoltottság miatt. Magyarország ebből a szempontból jól védettnek tekinthető, viszont Ukrajnában és Romániában előfordulnak járványok.[19] A legtöbb országban a kanyaró bejelentésköteles; ennek ellenére a legtöbb esetet nem jelentik, így a tényleges betegszám jóval nagyobb lehet a valódinál.
Az amerikai kontinens majdnem minden országa 1994-re bevezette a gyerekek kanyaró elleni védőoltását. Ennek eredményeképpen a megbetegedések száma évi 250 ezerről körülbelül 100-ra esett vissza, a betegség lényegében eltűnt a kontinensről. Néha nagyobb arányban is megjelenik a kanyaró, de szinte minden ilyen eset behurcolt kanyaróra vezethető vissza.[15][20] Amerika a legjobb példa arra, hogy a kanyaró oltásokkal leküzdhető.[21] 2011-től mindazonáltal az oltásellenesség következtében az USA-ban ismét emelkedni kezdett az esetek száma. 2013-ban 186 esetet regisztráltak, 2014 júniusának első hetében 65-öt, 2014 első félévében pedig 402-t.[22] 2014-ben összesen 667 kanyarós esetet regisztráltak, míg 2019 első négy hónapja során 695 kanyarós esetet jelentettek be, amely az ország 22 tagállamában jelentkezett.[23]
Oltásellenes mozgalmak és hatásaik[szerkesztés]
Andrew Wakefield brit orvos, egy 1998-as, a Lancet című tekintélyes orvosi folyóiratban megjelent tanulmányában azt állította, hogy a gyermekeknél tapasztalható autizmus és a védőoltások között kapcsolat van, mert a betegség megjelenése vagy súlyosbodása olykor az egyes védőoltások beadása után történik.[24][25] Szerinte az autizmust a tartósítószerként alkalmazott tiomerzál (etil-higany) okozza. Vizsgálatait megpróbálták megismételni, de az eredményeket nem sikerült reprodukálni, a feltevést nem lehetett igazolni, sőt a Public Library of Science folyóirat egy 2008-as tanulmányában cáfolták is azt.[26][27] Később az is kiderült, hogy Wakefield meghamisította az eredményeket, és vizsgálatait etikátlanul végezte.[28][29] Mindennek eredményeképpen 2010-ben a Lancet visszavonta az 1998-ban megjelent cikket, s a brit Orvosi Kamara is kizárta Wakefieldet tagjai sorából.[30] Bár az 1998 és 2004 között (illetve azóta) született eredmények tükrében gyakorlatilag kizárható, hogy bármilyen összefüggés lenne az oltások és az autizmus között, a cikk médiavisszhangjának köszönhetően sok szülő mégis úgy döntött (és teszi ma is), hogy az autizmus miatti félelemből nem adatja be gyerekének az MMR-oltást.[31] Emiatt jelentősen csökkent az átoltottság az Amerikai Egyesült Államokban, az Egyesült Királyságban és más európai országokban is.[32] A kanyaró pl. 14 év után újra megjelent Nagy-Britanniában, ahol 2008-ban ezren kapták el a betegséget, valamint 2015 februárjában Berlinben egy másfél éves kisgyermek betegedett meg és halt bele a kanyaró fertőzésbe.[33][34] A témában készült egy dokumentum film-sorozat is Vaxxed címmel, amelyben több szülő mesél a tapasztalataikról.
2019 áprilisában büntetés terhe mellett rendelték el a védőoltás kötelező beadását Brooklynban az ortodox zsidó negyedben kitört kanyarójárvány megfékezésére.[35] Az újabb járványok miatt egyre több helyen szigorítják az oltási kötelezettséget, a kanyaró ellen is.[19]
Kórokozója[szerkesztés]
Tulajdonságok[szerkesztés]
A kanyaróvírus kizárólag az emberben előforduló, 120–140 nanométeres egy szálú (-) RNS virus a Paramyxoviridae családból.
A vírus burka haemagglutinint (H-protein), fúziós proteint (F-protein) és mátrixproteint (M-protein) tartalmaz. A H- és az F-proteinek teszik lehetővé, hogy a vírus a gazdasejthez kapcsolódjon. A CD46 és a CD150 receptorok segítségével hatol be a sejtbe. Az oltás által indukált antitestek a felszíni fehérjék ellen irányulnak, különösen a H-protein ellen.[36]
A WHO eddig nyolc törzset (A-H) és 23 genotípust tart nyilván.[37] A genom mutációs rátája viszonylag alacsony, így nyomon követhetők a globális fertőzési utak.[38] Közép-Európában a C2, D6 és a D7 genotípus a leggyakoribb. A 2006-2007-es svájci és alsó-bajorországi kanyaró azonban D5 típusú volt, ami típusa alapján Thaiföldről vagy Kambodzsából származott.[39] Emellett a genotipus is stabil, ami lehetővé teszi a hatékony oltóanyagok előállítását.
A vírus érzékeny a külső hatásokkal szemben, a magas hőmérséklettel, az ultraibolya sugárzással, a zsíroldó- és a fertőtlenítőszerekkel szemben. Levegőn két órán át marad fertőzőképes.
A fertőzés módja és kivédése[szerkesztés]
A kanyaróvírus közvetlen kapcsolattal vagy cseppfertőzéssel terjed. A beteg a bőrkiütések előtt három-öt nappal már fertőzőképes, és az marad a bőrkiütések elmúlása utáni negyedik napig. A légutak nyálkahártyáján át vagy a szem kötőhártyáján keresztül jut a szervezetbe. A vírusnak rövid ideig való kitettség is könnyen fertőzéshez vezethet, fertőzési indexe 0,95. A vírusok a helyi nyirokcsomókban szaporodnak, és 48 óra után az érhálózaton át eljutnak a többi nyirokszervbe. 5–7 nap múlva a vírusok újra felszaporodnak a vérben, és megfertőzik a bőrt és a légutakat. Ekkor jelennek meg a bőrkiütések, kezdődik a köhögés és a bronchitis. A T-limfociták fertőzöttsége és a citokinek megnövekedett mennyisége legyengíti a szervezet ellenállóképességét. Ebben a négy-hat hétben a beteg másodlagos fertőzéseket is szenvedhet.[40]
A kiütések megjelenése előtt főleg a sejtes immunitás védekezik a kanyaró ellen. Azok a legyengült immunrendszerű betegek, akiknél a sejtes immunitás gyengült le, nagyobb eséllyel kapják el a kanyarót, ami súlyosabb lefolyást vehet. Azok a legyengült immunrendszerű betegek azonban, akiknél a humorális immunrendszer gyengült le, nincsenek nagyobb veszélyben, mint azok, akik egyébként egészségesek. A kiütések kialakulásában fontos szerepet játszanak a kis kapillárisokban lejátszódó immunreakciók. Legyengült immunrendszerű betegekben a kiütések el is maradhatnak, a többi súlyos tünet megjelenése mellett. A kiütések megjelenésével együtt kezdenek termelődni az antitestek, először az IgM, később az IgG típusúak.[40]
Lefolyása[szerkesztés]
Típusos lefolyás[szerkesztés]
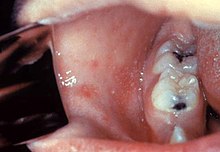

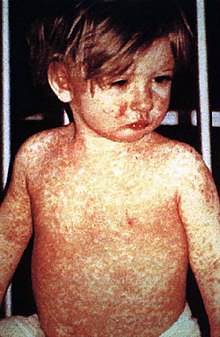
A típusos kanyaró lefolyása jellegzetesen két fázisú. A 10-14 napos lappangási idő után kezdődik a felső, néha a középső légutak nyálkahártyáinak gyulladásával, vagy kötőhártya-gyulladással. Ezekhez járulhat még az akár 41 °C-os láz, rosszullét, nyak- és fejfájás. A szájüreg nyálkahártyáján az elülső őrlőfogak környékén kis fehér foltocskák jelenhetnek meg elvörösödött háttér előtt, megelőlegezve a testszerte megjelenő kiütéseket. Ezek a foltok egyértelműen kanyaróra utalnak, de csak ritkán figyelhetők meg, ezért egyes szerzők inkább atípusosnak tartják.[41]
A betegség 12-13. napján kezdődik a kiütéses fázis. Először többnyire a lágy szájpad nyálkahártyája vörösödik el. A 14-15. naptól a fül mögül indul a nagy foltokból részben összefolyó vöröses kiütés, ami 4-5 napig megmarad. Emellett gyakori a nyirokcsomók megduzzadása is. Felnőtteken a betegség gyakran súlyosabb, mint gyerekeken.
A betegség lázgörbéje gyakran két csúcsú. A láz a csúcsot először a kezdeti, majd a késő kiütéses szakaszban éri el; a kettő között rövid időre el is múlhat a láz. Ha nincsenek komplikációk, akkor gyors gyógyulás, és élethossziglani immunitás következik.[42][43]
Nem típusos lefolyás[szerkesztés]
A nem típusos kanyaró különféleképpen jelentkezhet. Anyatejes csecsemők, vagy azok a betegek, akik antitesteket kaptak, a kanyaró enyhébb változatában betegednek meg.
Immunhiányos betegeknél a lefolyás nagy mértékben eltérhet a típusostól, például a kiütések elmaradásában. Az immunhiány okai lehetnek a sejtes immunitás veleszületett hiányosságai, a HIV-fertőzés, vagy a rosszindulatú daganatok. Ezen kívül a szervátültetettek is ide sorolhatók, akik bár nem betegek, de immunrendszerüket mesterségesen le kell gyengíteni ahhoz, hogy a beültetett szerv ne lökődjön ki. Náluk a kanyaró súlyosabb, és hosszabb lefolyású, ráadásul több, súlyosabb komplikáció léphet fel, és a halálozási arány is nagyobb.
Az Amerikai Egyesült Államokban és Kanadában az 1960-as években formalinnal inaktivált vírust használtak az oltásokban. Az ezzel oltott betegeknél a vad típusú kanyaróvírus a betegség súlyosabb formáját váltotta ki, kifejezett tünetekkel, a típusos sorrendtől eltérve, a tüdőt körülvevő folyadék felgyűlésével, májgyulladással és a végtagok ödémájával. A tünetek súlyossága ellenére a prognózis jó volt, és a betegek teljesen meggyógyultak.[42]
Komplikációk[szerkesztés]
Míg a betegek többsége semmilyen komplikációt nem tapasztal, addig az esetek 20–30%-ában különböző komplikációk lépnek fel. A leggyakoribb komplikációk a hasmenés (8%), a középfülgyulladás (7%), és a tüdőgyulladás (6%).[3] Emellett még sok más komplikáció is jelentkezhet.
Különböző adatok vannak a kanyarós betegek halálozási arányára. A Robert-Koch-Institut szerint 1:10.000 és 1:20.000 közötti,[44] a Centers for Disease Control and Prevention 1:500 és 1:1000 közé teszi.[45] A fejlődő országokban ez sokkal nagyobb, akár 25% is lehet.[15] Többnyire az agy vagy a tüdő gyulladása vezet halálhoz.
Tüdőgyulladás[szerkesztés]
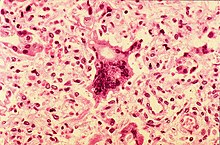
A kanyaró által okozott tüdőgyulladás a hörgőcskékben megy végbe, és légzészavart okoz. Vizsgálatához röntgenfelvétel szükséges.
A vírus közvetlenül károsítja a légzőrendszer hámját, pusztítja a hámsejtek csillóit. Ezzel a baktériumok is könnyebben megfertőzik a beteget. A légzőrendszer legyengülése miatt azonban enélkül is bekövetkezhet a bakteriális fertőzés és a tüdőgyulladás.
A kanyaró által okozott tüdőgyulladásban ritkábban többmagvú óriássejtek is létrejöhetnek a léghólyagocskák falában. Ez általában kanyaróra, vagy szamárköhögésre utal, de influenza vagy diftéria is okozhatja. Ez a forma az egyébként is legyengült betegeknél jelentkezik, és rossz a prognózisa.
Agyvelő- és agyhártyagyulladás[szerkesztés]
Az agy és az agyhártya gyulladása kanyarós betegeknél viszonylag ritka, az esetek 0,1%-ában jelentkezik, viszont 15–20%-ban halálos. További 20–40%-ban maradandó károsodásokat okoz.[44]
Az agyvelőgyulladás a kiütések megjelenésétől számított harmadik-tizenegyedik napon kezdődhet. Hat éven felülieknél gyakoribb, mint kisgyerekeknél. Lázzal, fejfájással, nyakmerevséggel, hányással kezdődik. Tudatzavar is kialakulhat, a beteg kómába is eshet. A súlyosabb formák epilepsziás rohamokban, és más agyi zavarokban nyilvánulnak meg. Az agy-gerincvelői folyadék sejtszaporulatot és megnövekedett fehérjekoncentrációt mutat.
Immunhiányos gyerekeknél a kanyaró által okozott agyvelőgyulladás különösen súlyos formája jelentkezhet. Ez a MIBE (measles inclusion-body encephalitis). A kanyaró után egy éven belül jelenik meg, nehezen kezelhető görcsrohamokban nyilvánul meg, és rendszerint néhány hónapon belül halált okoz.[46] A diagnózist az agyból vett mintával lehet megerősíteni. Még az oltásban levő vírus is okozhatja.[47] Ezért immunhiány esetén nem szabad kanyaró ellen oltani.
Dawson-kór[szerkesztés]
A kanyaró késői komplikációi közé tartozik a Dawson-kór, azaz a szubakut szklerotizáló pánenkefalitisz vagy SSPE (subacute sclerosing panencephalitis). Az agy általános gyulladása, a myelinhüvelyek pusztulása jellemzi. Súlyos károsodásokat okoz, és ha nem ismerik fel idejében, mindig halálhoz vezet. Okai nem ismertek, de úgy látszik, hogy a mutálódott felszíni fehérjék, különösen az M-protein válthatja ki.[43][48]
A kanyaró után hónapokkal, vagy évekkel később is felléphet. A leghosszabb lappangási idő tíz év, az átlagos hét év. A lefolyás során egyre súlyosabbá válik, a betegség progresszív. Általában egy-három évig tart; ettől csak az esetek 10%-a tér el.
Három fázisa különíthető el. Az elsőt pszichés károsodások és demencia, a másodikat izomgörcsök és epilepsziás rohamok jellemzik. A harmadik szakaszban a nagyagy súlyosan károsodott. Az EEG jellegzetes mintázatot mutat; ez döntő fontosságú a betegség diagnosztizálásában.
A betegség halálos kimenetele csak az 1. fázisban előzhető meg. Megszüntetésére nincs lehetőség, de interferonnal kombinált antivírus-készítmények (pl. Ribavirin) segítségével a tünetek csökkenthetők. A gyógyszert a betegnek élete végéig szednie kell. A 2. fázis közepétől kezdve a kór minden esetben halállal végződik.
Előfordulását régebben egy millióból 5-10 esetre tették. Az újabb adatok szerint gyakorisága 1:10.000.[44][49] Az abszolút gyakoriság a kanyaró elleni védőoltások hatására az 1980-as évek óta nagy mértékben csökkent.
Az SSPE többnyire azoknál lép fel, akik kétéves koruk előtt estek át kanyarón. Mivel a gyerekek egyéves koruk előtt nem olthatók, ezért csak az átoltott környezet védheti meg őket.
További komplikációk[szerkesztés]
A kezdeti szakaszban felléphet gégegyulladás, ami rekedtséget és a nyálkahártyák duzzanatával együtt légszomjat okoz.
A szaruhártya gyulladása látótérkiesést okozhat, ahol a kieső foltok kör alakúak. A fejlődő országokban a gyerekek megvakulásának a kanyaró az egyik fő oka, különösen, ha A-vitaminhiánnyal kombinálódik.
A kanyaró járhat ezen kívül még vakbélgyulladással, vagy a nyirokcsomók általános gyulladásával. Ritkán előfordulhat szívizomgyulladás, vesegyulladás, vagy a vérlemezkék számának erőteljes csökkenése.[43]
Törölheti az immunrendszer memóriáját, mellyel azt születéskori állapotába helyezi vissza; kivéve a kanyarót magát.
Felismerése[szerkesztés]
A tünetek alapján végzett diagnózis az atipikus lefolyású esetek miatt nem tekinthető biztosnak, ugyanis így a nem tipikus esetek nem ismerhetők fel, ezért éppen a legsúlyosabb kanyaróbetegek maradhatnának ellátatlanul.[44] A biztosabb felismerés érdekében kiegészítő vizsgálatokra van szükség. Járvány esetén azonban sokszor mégis a tünetek alapján állapítják meg a betegséget, különösen a tapasztalt diagnoszták.[50][51]
A legbiztosabb diagnózist a szérumvizsgálat nyújtja. A szérumban keresik mind az IgM, mind az IgG antitesteket. Az IgM antitestek megnövekedett száma csak valószínűsíti a betegséget, de még nem bizonyítja. Az IgM mennyisége csak a kiütések megjelenésétől kezdve nő meg; a kiütések megjelenése utáni harmadik naptól már biztosan kimutatható. A megnövekedett mennyiség a kiütések megjelenése utáni negyedik-hatodik hétig megmarad. A betegség az első napjaiban nem mutatható ki így, és a szerzett immunitás hamis pozitív eredményt adhat. Ha azonban a kanyaró elleni IgG-antitestek koncentrációja egy hét alatt a négyszeresére nő, akkor az egy friss fertőzésre utal. Ez a vizsgálat azonban csak a kiütések megjelenése utáni hetedik naptól fejezhető be.[43][44][52]
A kórokozó direkt kimutatása nehezebb, de bizonyos esetekben van értelme. A vírus RNS-ének elemzésével meg lehet állapítani a típusát, ami a fertőzések nyomon követéséhez hasznos. Társuló agyvelő- vagy agyhártyagyulladás esetén érdemes a vírust az agy-gerincvelői folyadékban keresni. Az RNS instabilitása miatt a nyomok hiánya nem zárja ki, hogy a kísérő betegséget a kanyaróvírus okozta. SSPE esetén sem direkt mutatják ki a vírust, hanem közvetve, az IgM-antitestek alapján.
A speciális vírusdiagnosztika mellett a vérvizsgálat a fehérvérsejtek számának csökkenését mutatja ki, különösen a limfociták, és az eozinofil granulociták száma csökken, és megritkulnak a vérlemezkék is. Az agy fertőzöttsége esetén az agy-gerincvelői folyadékban megnő a fehérjék és a limfociták koncentrációja.
A differenciáldiagnosztika szempontjából leginkább a skarlát és a rózsahimlő jöhet még szóba. Skarlát esetén a kis pontokból álló kiütések a hónalj vagy a csípő környékéről indulnak el, és felfelé terjednek, kihagyva az áll-száj háromszöget. Emellett tipikus a nyelv elszíneződése és a pharingitis. A rózsahimlő többnyire enyhébb lefolyású, mint a kanyaró, mérsékelt lázzal, és gyenge, össze nem folyó kiütésekkel a nyakon és a mellen. Jellemző a nyaki nyirokcsomók gyulladása. Emellett számításba kell még venni a Pfeiffer-féle mirigylázat, a toxoplazmózist, a Kawasaki-szindrómát, a mycoplasma fertőzést, és a gyógyszerallergiát. A speciális antitestek kimutatásával mindezeket ki lehet zárni.
Kezelése[szerkesztés]
Speciálisan kanyaró elleni kezelés nem létezik. A betegség akut szakaszában ágynyugalom, láz- és köhögéscsillapítás, sok folyadék fogyasztása javasolt. Tüneti kezelésként fájdalomcsillapítókat és köhögés elleni szereket írnak fel. A láz miatti megnövekedett folyadékveszteséget fokozott folyadékbevitellel kell fedezni. A baktériumos felülfertőzéseket, a középfül- és tüdőgyulladást antibiotikumokkal lehet kezelni.
A fejlődő országokban végzett tanulmányok szerint az A-vitamin adása segít a komplikációk elkerülésében és a halálozás csökkentésében.[53] A WHO ajánlja az A-vitamin pótlását azokon a vidékeken, ahol gyakori az A-vitaminhiány. A fejlett országokban azonban nem végeztek hasonló felméréseket.[54]
A Ribavirin vírusellenes szer in vitro hatékonynak bizonyult a kanyaróvírus ellen. Néhány egyedi esetben segített a kanyarófertőzés ellen, a klinikai tanulmányok azonban hiányoznak.[54][55]
Az aktív vagy passzív immunizálás segíthet mérsékelni vagy elkerülni a betegséget. A betegnek nem szabad közösségbe mennie, amíg meg nem gyógyul (karantén).
A betegség több országban bejelentésköteles.
Megelőzése[szerkesztés]
Karantén[szerkesztés]
A fertőzött gyerek egészen addig nem mehet közösségbe, amíg fertőz, és amíg meg nem gyógyul. Közösségen leginkább olyan intézményeket kell érteni, amik gyerekekkel foglalkoznak, például bölcsődék, óvodák, iskolák, napközik, táborok, otthonok. Hasonló rendelkezések vonatkoznak az ilyen intézmények dolgozóira is. Sok országban van ilyen szabályozás.
Oltás[szerkesztés]
A kanyaró elleni oltóanyagot a mumpsz és a rózsahimlő elleni oltóanyaggal kombinálva adják be; ez az úgynevezett MMR-vakcina. Az oltóanyag gyengített vírust tartalmaz, ami az esetek 95%-ában elégséges védelmet ad. A másik oltásra azért van szükség, mert emellett a hatásfok mellett még kialakulhatnak helyi járványok. A második oltás után a gyerekek 99%-ában alakul ki élethossziglani védettség, ami már elég a helyi járványok megakadályozására. A két oltás között legalább négy hét szünetet kell tartani. A védettség megállapítható a kanyaró elleni IgG jelenlétéből. Az MMR-vakcina tovább kombinálható más oltóanyagokkal.
Az oltás ellenjavallatai: akut betegségek; HIV-pozitív állapot, leukémia, és más immunhiányok; terhesség, zselatinallergia, alacsony vérlemezkeszám. Ha egy ilyen állapotú ember elkapja a kanyarót, akkor antitesteket adnak be neki.[54]
Általában nem oltanak egy évesnél fiatalabb csecsemőt. Ha viszont a gyereket intézetben kell elhelyezni, akkor az oltás beadható tizenkét hónapos kora előtt, de meg kell várni a kilenc hónapos kort, mivel az anyai antitestek leküzdhetik az oltásban levő vírust. Az oltást akkor is ajánlják, ha a gyerek már átesett természetes fertőzésen, mivel szérumvizsgálat hiányában az anamnézis megbízhatatlan. A második oltás előtt lehetséges szérumvizsgálatot végezni, és megfelelő ellenanyag-koncentráció esetén lemondani a második oltásról, de az ajánlások a második oltás rutinszerű beadását javasolják.
Ha az átoltottság elér egy bizonyos arányt, akkor a nyájimmunitás alapján az oltás nemcsak azokat védi, akik be vannak oltva, hanem azokat is, akik nem olthatók, vagy nem akarják magukat beoltani. Így az oltás nemcsak magánérdek, de közérdek is.
Az oltás kockázatai[szerkesztés]
| Tünet, vagy betegség | Komplikációs arány kanyaróban |
Komplikációs arány MMR-oltás után |
|---|---|---|
| Kiütés | 98% | 5%, enyhe |
| Láz | 98% | 3-15% |
| A vérlemezkeszám leesése | 1/3000 | 1/30 000-1/50 000 |
| Agyvelőgyulladás | 1/1000 | < 1/1 000 000 (bizonytalan) |
| Letalitás | 1/1000-1/20 000 | 0 |
Az oltás leggyakoribb kísérő jelenségei: láz, levertség, fejfájás, és helyi oltásreakció bőrpírral, duzzanattal és fájdalommal. Ezek enyhe tünetek. Ritkák az olyan súlyosabb reakciók, mint az allergia. A vérlemezkeszám leesése, és az agyvelőgyulladás nagyon ritka, és vitatott, hogy valóban oltási kanyaró okozta-e az ismert eseteket.[54] Lázgörcsök jelentkezhetnek; ijesztő, de hosszú távon nyom nélkül elmúlnak.[57]
Mivel az oltóanyag fertőzőképes vírusokat tartalmaz, fennáll az oltási kanyaró veszélye. Ez a kanyaró a tipikus tünetekkel jelentkezik, és enyhe lefolyású. Ezekben az esetekben átfertőzéstől nem kell tartani.[44]
A további mellékhatások vitatottak. Jelen ismereteink szerint nem lehet kizárni az asztmát, az allergiákat, és a cukorbetegséget. A Crohn-betegséget kizárták, mint lehetséges mellékhatást.[58] Andrew Wakefield angol sebész szerint az MMR-vakcina higanytartalma miatt felelőssé tehető az autizmus elterjedéséért. Habár Wakefield feltételezését kutatásokkal cáfolták,[59][60][61] és az újabb MMR-oltóanyagok nem tartalmaznak higanyt, a hisztériát nem lehetett megállítani. Az autizmustól félő szülők gyerekeiket természetes fertőzéssel akarják immunizálni, ezért oltatlan gyerekeiket kanyarós gyerekek közé viszik, remélve, hogy elkapják a fertőzést.[62]
Bár a kanyaró elleni oltóanyagot a szakértők biztonságosnak és szükségesnek tartják, több publikáció szerint a mellékhatásokra nem fordítottak elég figyelmet, és a vizsgálatok egy része nem volt megfelelő.[59]
Profilaxis[szerkesztés]
Az immunhiányos betegeket nem lehet oltani. Ha elkapják a kanyarót, akkor, ha három napon belül emberi antitesteket kapnak a betegség ellen, akkor a kanyaró kitörése megakadályozható, vagy enyhe lefolyásúvá tehető. Az egészséges immunrendszerű betegek aktív oltóanyagot kapnak. Ezzel az oltással a kanyaró további terjedését előzik meg.[44]
Kanyaró és terhesség[szerkesztés]
Jelenleg nem ismerjük a terhesség alatti kanyaró hatását. Az anyánál a betegség megnövelheti a komplikációk esélyét; koraszüléshez vagy vetéléshez vezethet. Nem mindig kapja el az anya betegségét az újszülött születés közben; ha mégis, akkor súlyos komplikációktól kell tartani.[43]
A terhességük alatt kanyaróban megbetegedett nőket megfigyelés alatt tartják. Prenatális diagnosztikát ilyenkor nem szoktak végezni. A kezelés általában tüneti, de az anya immunglobulint is kaphat. Az MMR-oltás terhesség alatt ellenjavallt. Az oltás után három hónapig védekezni kell a teherbe esés ellen, de az oltásra hivatkozva nem lehet terhességmegszakítást kérni.
Áltudományos nézetek a kanyaróval kapcsolatban[szerkesztés]
Bár tudományosan teljes mértékben bizonyított, hogy a kanyaróvírus okozza ezt az erősen fertőző betegséget, mégis vannak olyanok, akik megkérdőjelezik magát a tényt. Egy német biológus, Dr. Stefan Lanka azt állítja, hogy a vírus nem is létezik, és a kanyaró valójában pszichoszomatikus eredetű betegség. Lanka egy jól ismert oltásellenes aktivista Németországban, aki többek között azt is vitatja, hogy az AIDS okozója a HIV vírus.[63] Saját kutatásokat nem folytat, azonban 2011-ben a saját honlapján közzétett egy felhívást, amelyben 100 ezer eurót ajánlott fel annak, aki tudományosan be tudja bizonyítani, hogy a kanyarót vírus okozza, és meg tudja határozni a vírus méretét is.[64] Amikor egy német orvos, David Barden különböző orvosi kutatásokból származó tudományos bizonyítékok sokaságát tárta elé válaszul, Lanka nem fogadta el a bizonyítékokat, így Barden beperelte őt. A per azzal az ítélettel végződött, hogy Lankának meg kell fizetnie a felhívásban szereplő 100 ezer eurós összeget.[65][66]
Az ügy igen nagy nemzetközi visszhangot kapott, amely sokakat arra késztetett, hogy megszólaljanak az ügyben. Megtette ezt többek között a nemzetközi hírű szkeptikus, a tudomány alapú orvoslás ismert szóvivője, Dr. Steven Novella klinikai neurológus is, aki Lankát egyszerűen „hóbortosnak” titulálta.[67]
Jegyzetek[szerkesztés]
- ↑ Kanyaró szócikk - A Pallas nagy lexikona. Magyar Elektronikus Könyvtár. (Hozzáférés: 2015. március 31.)
- ↑ Házi Gyermekorvosok Országos Egyesülete - Kanyaró Archiválva 2017. március 9-i dátummal a Wayback Machine-ben, hgye.hu
- ↑ a b Measles. In: Epidemiology & Prevention of Vaccine-Preventable Diseases – „The Pink Book“, 9te Edition, Public Health Foundation, S. 131-144 PDF, 830 kB
- ↑ Bianchine PJ, Russo TA.: The role of epidemic infectious diseases in the discovery of America. Allergy Proc. 1992 Sep-Oct;13(5):225-32. PMID 1483570
- ↑ Roy Porter: Die Kunst des Heilens: Eine medizinische Geschichte der Menschheit. Heidelberg, Berlin (Spektrum) 2003 (ISBN 3-8274-1454-7) S. 166
- ↑ ebd. S. 24
- ↑ Peter L. Panum: Observations Made During the Epidemic of Measles on the Faroe Islands in the Year 1846 American Public Health Association, New York 1940;(ders. Beobachtungen über das Maserncontagium, in: Archiv für Pathologische Anatomie und Physiologie und für Klinische Medizin, Berlin, Bd. 1, 1847, S. 492-512
- ↑ J.-Ch. Sournia, J. Poulet, M: Martiny (Hrsg.): Illustrierte Geschichte der Medizin. Directmedia, Berlin 2004
- ↑ Enders JF, Peebles TC.: Propagation in tissue cultures of cytopathogenic agents from patients with measles. Proc Soc Exp Biol Med. 2:277-86. (1954) PMID 13177653
- ↑ WHO: Global summary on measles Archiválva 2013. augusztus 14-i dátummal a Wayback Machine-ben, 2006
- ↑ Áttekintés: Measles History, Website des Center for Disease Control and Prevention (CDC) Archiv-Version
- ↑ Moss WJ :Measles Still Has a Devastating Impact in Unvaccinated Populations[halott link] PLoS Medicine Vol. 4, No. 1. PMID 17199409
- ↑ WHO-UNICEF joint statement on strategies to reduce measles mortality worldwide. Weekly epidemiological record 27, 77:221–228 (2002) PMID 12125242 PDF, 158 kB
- ↑ Muller CP, Kremer JR, Best JM, Dourado I, Triki H, Reef S; WHO Steering Committee for Measles and Rubella.: Reducing global disease burden of measles and rubella: report of the WHO Steering Committee on research related to measles and rubella vaccines and vaccination, 2005. Vaccine. 2007 Jan 2;25(1):1-9. PMID 17262908
- ↑ a b c d Barinaga Jorge, Skolnik Paul: Epidemiology and transmission of measles. Review, UpToDate v15.1, 2007
- ↑ Medical News Today: CDC Urges Travelers To Israel To Protect Themselves From Measles. [2010. december 27-i dátummal az eredetiből archiválva]. (Hozzáférés: 2010. július 7.)
- ↑ Webseite des National Institute for Communicable Diseases[halott link]
- ↑ Robert Koch-Institut: Epidemiologisches Bulletin 05/2003 PDF, 98 KB Archiválva 2010. december 21-i dátummal a Wayback Machine-ben
- ↑ a b https://medikidskozpont.hu/nem-fenyeget-kanyarojarvany-magyarorszagon/
- ↑ De Quadros CA, Izurieta H, Carrasco P, Brana M, Tambini G: Progress toward measles eradication in the region of the Americas. J Infect Dis. 2003 May 15;187 Suppl 1:S102-10. PMID 12721900
- ↑ de Quadros CA.: Can measles be eradicated globally? Bull World Health Organ. 2004 Feb;82(2):134-8. PMID 15042236
- ↑ http://www.cdc.gov/mmwr/preview/mmwrhtml/mm6323md.htm#tab2
- ↑ US measles outbreak is largest since disease was declared eliminated in 2000. edition.cnn.com. (Hozzáférés: 2019. április 25.)
- ↑ (angolul) Autizmus és homeopátia Archiválva 2008. szeptember 5-i dátummal a Wayback Machine-ben
- ↑ Smits, Tinus. Autizmus. Remedium. ISBN 978-963-87863-0-2
- ↑ Nincs összefüggés az autizmus és a védőoltás között (Index, 2008. szeptember 5.)
- ↑ [http://briandeer.com/mmr/lancet-summary.htm Exposed: Andrew Wakefield and the MMR-autism fraud]. briandeer.com. (Hozzáférés: 2015. március 31.)
- ↑ http://www.timesonline.co.uk/tol/life_and_style/health/article5683643.ece
- ↑ https://web.archive.org/web/20100202030927/ca.news.yahoo.com/s/afp/100129/world/britain_health_vaccination_children_social
- ↑ Nem okoz autizmust a védőoltás. index.hu, 2011. január 6. (Hozzáférés: 2015. március 31.)
- ↑ Kovács Emese: Andrew Wakefield és a nagy autizmusoltás-kamu. Divany.hu, 2014. november 12. (Hozzáférés: 2015. március 31.)
- ↑ Ha te nem oltasz, az én gyerekem is veszélyezteted. Divany.hu, 2014. január 29. (Hozzáférés: 2015. március 31.)
- ↑ Meghalt egy kanyarós kisgyerek Berlinben. index.hu, 2015. február 23. (Hozzáférés: 2015. március 31.)
- ↑ Disneylandből jön a kanyaró. Népszabadság Online, 2015. január 24. (Hozzáférés: 2015. március 31.)
- ↑ bbc.com
- ↑ Yanagi Y, Takeda M, Ohno S, Seki F: Measles virus receptors and tropism. Archiválva 2007. október 18-i dátummal a Wayback Machine-ben Jpn J Infect Dis. 2006 Feb;59(1):1-5. PMID 16495625
- ↑ WHO: Nomenclature for describing the genetic characteristics of wild-type measles viruses (update). WER 2001; 32: 242–247 and 33: 249–251 PMID 11515240 PDF, 137 kB
- ↑ Bellini WJ, Rota PA.: Genetic diversity of wild-type measles viruses: implications for global measles elimination programs. Emerg Infect Dis. 1998 4(1):29-35. PMID 9452396
- ↑ Robert Koch-Institut: Epidemiologisches Bulletin 37/2007 Archiválva 2009. február 6-i dátummal a Wayback Machine-ben
- ↑ a b Köhler et al.: Medizinische Mikrobiologie, S. 641-644.
- ↑ Cherry JD: Textbook of pediatric infectious diseases, 5. Auflage, Philadelphia (WB. Saunders) 2004, S. 2292–2293
- ↑ a b Harrisons Innere Medizin (2005), S. 1232–1235.
- ↑ a b c d e Barinaga Jorge, Skolnik Paul: Clinical presentation and diagnosis of measles. Review, UpToDate v15.1, 2007
- ↑ a b c d e f g h Kanyaró. A Robert-Koch-Institut tanácsadója a fertőző betegségekről orvosoknak. [2010. december 20-i dátummal az eredetiből archiválva]. (Hozzáférés: 2010. július 9.)
- ↑ Website des CDC: Overview of Measles Disease
- ↑ Freeman AF et al.: A new complication of stem cell transplantation: measles inclusion body encephalitis. Pediatrics. 2004 114(5):e657-60. PMID 15520095. ISSN 0031-4005 PDF, 157 kB
- ↑ Bitnun A et al.: Measles inclusion-body encephalitis caused by the vaccine strain of measles virus. Clin Infect Dis. 1999 29(4):855-61. PMID 10589903. ISSN 1058-4838
- ↑ Hotta H, Jiang DP, Nagano-Fujii M: SSPE virus and pathogenesis. Nippon Rinsho. 2007 Aug;65(8):1475–80. PMID 17695286
- ↑ Bellini WJ et al.: Subacute sclerosing panencephalitis: more cases of this fatal disease are prevented by measles immunization than was previously recognized. J Infect Dis. 2005 192(10):1686–93. PMID 16235165
- ↑ Ferson MJ, Young LC, Robertson PW, Whybin LR.: Difficulties in clinical diagnosis of measles: proposal for modified clinical case definition. Med J Aust. 1995 Oct 2;163(7):364-6. PMID 7565261
- ↑ Oliveira SA et al.: Assessment of the performance of a definition of a suspected measles case: implications for measles surveillance. Rev Panam Salud Publica. 2006 Apr;19(4):229-35. PMID 16723063
- ↑ Bellini, WJ, Helfand, RF: The challenges and strategies for laboratory diagnosis of measles in an international setting. J Infect Dis 2003; 187 Suppl 1:S283 PMID 12721927
- ↑ Huiming Y, Chaomin W, Meng M: Vitamin A for treating measles in children. Cochrane Database Syst Rev. 2005 Oct 19;(4):CD001479. PMID 16235283
- ↑ a b c d e Bekhor David, Barinaga Jorge, Skolnik Paul: Prevention and treatment of measles. Review, UpToDate v15.1, 2007
- ↑ Forni, AL, Schluger, NW, Roberts, RB. Severe measles pneumonitis in adults: Evaluation of clinical characteristics and therapy with intravenous ribavirin. Clin Infect Dis 1994; 19:454. PMID 7811865
- ↑ Chen RT: Vaccine risks: real perceived and unknown. Vaccine 17/1999. S. 41–46 PMID 10559533
- ↑ Vestergaard M et al.: MMR vaccination and febrile seizures: evaluation of susceptible subgroups and long-term prognosis. JAMA. 2004 Jul 21;292(3):351-7. 15265850 PMID 15265850
- ↑ Kulcsár Anita a kizárt mellékhatásokról. Szent László Kórház[halott link]
- ↑ a b Demicheli V, Jefferson T, Rivetti A, Price D: Vaccines for measles, mumps and rubella in children. Cochrane Database Syst Rev. 2005 Oct 19;(4):CD004407. Review. PMID 16235361
- ↑ Madsen KM, Hviid A, Vestergaard M, Schendel D, Wohlfahrt J, Thorsen P, Olsen J, Melbye M: A population-based study of measles, mumps, and rubella vaccination and autism. N Engl J Med. 2002 Nov 7;347(19):1477–82. PMID 12421889
- ↑ T Jefferson: Unintended events following immunization with MMR: a systematic review. Vaccine. 2003 Sep 8;21(25-26), S. 3954-60 PMID 12922131
- ↑ http://www.guardian.co.uk/lifeandstyle/2001/jul/26/healthandwellbeing.health
- ↑ Stefan Lanka: HIV; Reality or artefact? (német nyelven). Virusmyth.com, 1995. április 1. (Hozzáférés: 2015. március 31.)
- ↑ Das Masern-Virus 100.000 € Belohnung! WANTeD Der Durchmesser (német nyelven), 2011. november 24. [2015. április 2-i dátummal az eredetiből archiválva]. (Hozzáférés: 2015. március 31.)
- ↑ 100 ezer eurót fizethet a német oltástagadó. index.hu, 2015. március 13. (Hozzáférés: 2015. március 31.)
- ↑ 30 milliót bukhat egy fogadáson az oltásellenes biológus. Hír24.hu, 2015. március 13. [2015. április 2-i dátummal az eredetiből archiválva]. (Hozzáférés: 2015. március 31.)
- ↑ Steven Novella: Yes, Dr. Lanka, Measles is Real (angol nyelven). NeuroLogica Blog, 2015. március 13. (Hozzáférés: 2015. március 31.)
Források[szerkesztés]
- Gergely Lajos (szerk.): Orvosi mikrobiológia. (2., átd. kiadás.) Alliter Kiadói és Oktatásfejlesztő Alapítvány, Budapest, 2003. ISBN 963-202-766-3.
- Az Országos Epidemiológiai Központ tájékoztatója a védőoltásokról (2007): https://web.archive.org/web/20080607055428/http://www.egeszsegkalauz.hu/oltasi-naptar-2007.xhtml
- https://web.archive.org/web/20170913231352/https://munkahet.hu/hirek/eletmod-egeszseg/a-kanyaro-tunetei-kezelese-vedooltas
- Kanyaró gyermekkorban (tünetek, okai, kezelése). Archiválva 2018. szeptember 2-i dátummal a Wayback Machine-ben
| Az itt található információk kizárólag tájékoztató jellegűek, nem minősülnek orvosi szakvéleménynek, nem pótolják az orvosi kivizsgálást és kezelést. A cikk tartalmát a Wikipédia önkéntes szerkesztői alakítják ki, és bármikor módosulhat. |

