Szerves kémia
| Kémia |
|---|
| elméleti kémia |
| fizikai kémia |
| szervetlen kémia |
| szerves kémia |
| analitikai kémia |
| egyéb |
| A kémia személyes- és történelmi vonatkozásai |
|
|
A szerves kémia a kémia azon ága, mely a szerves vegyületeket tanulmányozza. Szerves vegyületek építik fel az élő szervezeteket, de számos mesterséges vegyület (pl.: műanyagok, szintetikus gyógyszerek) is van köztük. Legnagyobb mennyiségben a fotoszintetizáló élőlények (pl. zöld növények, kékbaktériumok, sárgásmoszatok stb.) állítanak elő szerves vegyületeket szén-dioxidból és vízből, valamint ásványi sókból. Ezek ún. fotoautotróf szervezetek. A zöld növények és a már említett egyéb autotróf szervezetek előállítanak szénhidrátokat (glükóz, fruktóz, cukor, keményítő, cellulóz élesztő), zsírokat, olajokat, vitaminokat, fehérjéket, nukleinsavakat színanyagokat, illatanyagokat stb.
A legegyszerűbb szerves vegyületek azonban a szénhidrogének, amelyek a kőolaj, földgáz, metán-hidrát összetevői. Kisebb mennyiségben a kemoautotróf szervezetek, pl. metanogének, kénoxidáló baktériumok, nitrifikáló baktériumok is kötnek meg szén-dioxidot. Az élővilág szerves vegyületei tehát végső soron az autotróf élőlények anyagcseréje során megkötött szén-dioxidból származnak, a többi élőlény (heterotrófok) ezeket felhasználva építi fel saját szerves vegyületeit. A szerves kémia elnevezés onnan ered, hogy sokáig azt hitték, csak az élő szervezet képes előállítani az őket felépítő szénvegyületeket. Ezt az álláspontot (vis vitalis elmélet) Friedrich Wöhler cáfolta meg, amikor 1828-ban szervetlen anyagból kiindulva karbamidot, szerves szénvegyületet állított elő. Tehát az ember is képes mesterséges szerves anyagok előállítására, akár szervetlen anyagokból is. Az évek folyamán a tudományos kutatás rengeteg olyan szénvegyületet hozott létre mesterségesen, életfolyamatok közreműködése nélkül, amelyek tulajdonságaikat tekintve az életfolyamattal kapcsolatos (valódi) szerves vegyületekkel megegyeznek, vagy legalábbis azokkal nagy hasonlóságot mutatnak. Habár ezek közül számosnak nincs biológiai funkciója, mégis a szerves vegyületek között vannak számontartva.
A 2000-es évek elején már 10–15·106 számú természetes és szintetikus szerves vegyület volt ismert, és ez a szám évente kb. 300 000-rel nőtt.[1]
Története[szerkesztés]

A tizenkilencedik század elején, a modern kémia hajnalán a vegyészek úgy látták, hogy az élőlényekből származott anyagok szerkezete túlságosan bonyolult és csakis életfolyamatok útján jöhetnének létre úgynevezett vis vitalis, vagyis életerő segítségével. Ezeket 1806-ban Jöns Jakob Berzelius svéd kémikus szerves anyagoknak nevezte el.[2]
Szerves kémia csak akkor ébredezett, amikor valaki ki tudta mutatni, hogy ezeket az anyagokat szervetlen anyagokhoz hasonlóan lehet kezelni és ezeket is elő lehet állítani életfolyamat közreműködése nélkül. 1816 táján Chevreuil (Michel) kezdte tanulmányozni a különféle zsírokból származó szappanokat. Elválasztotta ezekből a különböző savalkotórészeket, és megfigyelte, hogy ezek különböző vegyületek. Ezzel azt bizonyította, hogy kémiai változás igenis létrehozható szerves származású zsírokból életfolyamat közreműködése nélkül.
A vis vitalis elmélet teljes megcáfolása csak akkor történt, amikor Wöhler karbamidot (a vizelet egyik komponense) állított elő, és 1828-ban azt írta közleményében, hogy a folyamatban a vesének semmi szerepe nem volt. Eredetileg nem is karbamidot akart előállítani, hanem ammónium-cianátot, de sikertelenül, mert cianátokat próbált reagáltatni ammónia oldattal. Ezt követően ciánsavra váltott, és a lombik fenekén összegyűlt fehér por analíziséből kiderült, hogy karbamid volt. Az ammónium-cianát vizes oldatának bepárlása útján való karbamid előállítást Wöhler-szintézisnek nevezik.
A következő nagy lépés 1856-ban történt, amikor Perkin (William, Henry) egy szerves festéket állított elő (szintén véletlenül), melyet Perkin-lilának (mauvein) neveztek el. 1874-ben a DDT laboratóriumi előállítása Zeidler (Othmer) munkája folyamán megint fontos lépést jelentett, még ha a vegyület rovarirtó tulajdonságait csak sokkal később vették is észre.
A szerves kémia története a kőolaj felfedezésével folytatódik, annak frakcionált desztilláció útján való párlatokra osztásával és további részrebontásával finomdesztilláció, extrakció vagy fagyasztás igénybevételével. A különböző vegyülettípusok vagy egyedi vegyületek kémiailag más vegyülettípusokká vagy vegyületekké történő átalakítása (konverziója) hozta létre a kőolajkémiát és a petrolkémiai ipart is. Az utóbbi sikeresen kapcsolódott a mesterséges gumi, a különböző szerves ragasztószerek, műanyagok és a kőolajtermékek tulajdonságmódosító adalékanyagainak gyártásához.
A gyógyszeripar a 19. század utolsó évtizedében született meg, amikor a Bayer gyár elkezdte az acetilszalicilsav (aszpirin) gyártását.
A biokémia, az élő szervezetek vegyületei szerkezeti összetételeinek és egymással való kölcsönhatásainak in vitro (kémcsőben) vagy magában az élő szervezetben való tanulmányozása csak a 20. században jött létre.
Szerves vegyületek[szerkesztés]
A szerves vegyületek molekulákból felépülő, széntartalmú vegyületek.
A molekulákban a szénatomok többnyire szénatomláncokat képeznek, úgy, hogy egyes, kettős vagy hármas kovalens kötéssel kapcsolódnak egymáshoz. Vannak azonban egy szénatomos szerves vegyületek is, pl. a metán vagy a Wöhler-kísérletben előállított karbamid.
A szénatom négy vegyértékű, tehát négy kovalens kötést hoz létre másik szénatommal, hidrogénatommal vagy más, nemfémes elem atomjával. Elektronegativitása optimális a kovalens kötések kialakításához.
A szerves vegyületeket felépítő elemeket organogén elemeknek nevezik: C, H, N, O, halogének (F, Cl, Br, I), S, P.
Vannak azonban szervetlen szénvegyületek is. Ide sorolják a szén oxidjait, a karbidokat, a karbonátokat, a hidrogén-cianidot és a fém-cianidokat (pl. kálium-cianid).[1]
Szénatomláncok[szerkesztés]
Csak a szénatomok képesek egymáshoz kapcsolódva stabil atomláncokat létrehozni.
A szénnel „rokon” szilícium hidrogénnel alkotott vegyülete, a szilícium-hidrid, vagy más néven szilán (SiH4), mely a metán analógja, rendkívül instabil, még alacsony hőmérsékleten is öngyulladó. Erős redukálószer. A szilánok, SinH2n+2, az alkánok analógjai, de sokkal kevésbé stabilak azoknál. Csak a kis szilíciumatom-számú homológok állíthatók elő számottevő mennyiségben (Si6H14-ig). Kettős vagy hármas kötésű homológok nem léteznek.
A szénláncokban a kovalens kötések irányítottak, azaz meghatározott szöget zárnak be, és a kötéstávolság is jól meghatározott értékű. Ebből kifolyólag a molekuláknak sajátos alakja van.
1. Telített láncok[szerkesztés]
Az ún. telített szénláncok a legegyszerűbb szénatomláncok.
A telített szénláncokban a szénatomok sp3 hibridállapotban vannak, és egyszeres kovalens kötéssel kapcsolódnak egymáshoz.
Felépítésüket egy telített szénlánc, illetve egyszerűbb képviselője, a négy szénatomból álló bután és a belőle levezethető karbonsav, a butánsav (vajsav) szerkezetével ideálisan lehet szemléltetni.
 |
 |
 |
 |
 |
 |
A legegyszerűbb szénhidrogén, a metán esetén a kötésszög 109°28’, a kötéstávolság 108,70 pm. A többi szénláncban ezek az értékek kisebb eltérést mutatnak, amint azt az etán szerkezete ábrázolja:
 |
 |
 |
Konformáció[szerkesztés]
Az egyszeres kovalens kötéssel kapcsolódó szénatomok az egyszeres kötés tengelye körül egymáshoz képest elfordulhatnak, így a molekula különböző alakokat vehet fel.
Például az etán konformációi: különböző 3D szerkezetei, melyek csak az egyszeres kötés körüli elforgás mértékében különböznek egymástól:
 |
 |
 |
2. Telítetlen láncok[szerkesztés]
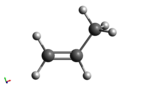
Az ún. telítetlen szénláncokban a szénatomok egy része (legalább két-két szénatom) sp2 vagy sp hibridállapotban van, és kettős vagy hármas kötéssel kapcsolódik egymáshoz.
Ezek szerkezete az etén, propén, illetve acetilén szerkezetével, illetve molekulamodelljével szemléltethető:
 |
 |
 |
 |
 |
A telített és telítetlen szénláncok osztályozása[szerkesztés]
- egyenes láncok: pl. a már említett bután. Az egyenes láncú butánt normál-butánnak (n-bután) nevezik.
- elágazó láncok: a bután elágazó láncú izomerje a 2-metilpropán (izobután).
 |
 |
- A bután és a 2-metilpropán (izobután) azonos számú szén- és hidrogénatomot tartalmaz, ezért ezek egymásnak láncizomerjei.
- gyűrűs láncok: például a ciklohexán
 |
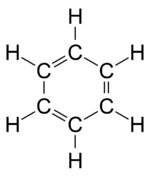
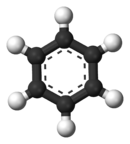
3. Aromás gyűrű[szerkesztés]
A legegyszerűbb aromás gyűrű a benzolgyűrű, melynek szénatomjai sp2 hibridállapotban vannak, és 6 atomból álló szabályos hatszög alakú, zárt láncot – gyűrűt – képeznek. A benzol többféleképpen ábrázolható. Az első, legegyszerűbb ábrázolásmód a Kekulé-féle képlet. A benzol modern képlete jobban leírja a molekula aromás jellegét, ennek ellenére továbbra is használják a Kekulé-féle képletet is, mert egyes reakciói, pl. az addíciós reakciók, ezzel a képlettel jobban magyarázhatók.
A benzolban a C−C kötéstávolság 0,140 nm, a kötésszög 120°. A benzol-homológoknál ez eltérő értékeket mutat.
A szénatom jellegzetes tulajdonságai miatt rengeteg lehetséges szerves vegyület létezik, sokkal több, mint szervetlen.
A szerves vegyületek jellemzői[szerkesztés]
Az életfolyamatok szervetlen anyagokra is támaszkodnak. Például sok enzim működéséhez vas és/vagy réz jelenléte is szükséges igen kis mennyiségben; a csont, a fog és a kagyló pedig részben szerves, részben szervetlen anyagból áll, azt nem is említve, hogy az emésztéshez a HCl vizes oldatára (sósavra) van szükség, és hogy az élőlények testének fő alkotórésze víz. Az előbbi szervetlen sav, és az utóbbi is a szervetlen kémia tárgykörébe tartozik. Azokat a vegyületeket, amelyek életfolyamatokban vesznek részt, a szerves kémiának a biokémia ága tárgyalja.
A szerves vegyületek száma a kutatás és mesterséges előállítás révén igen gyorsan gyarapszik, és számuk többszörösen meghaladja a szervetlen vegyületek számát. Az indoka ennek az, hogy a szilíciumtól eltekintve a szén a periódusos rendszer egyetlen eleme, amelynek atomjai más, magával azonos atomokkal kapcsolódva lánc és gyűrű alakú vegyületek hatalmas tárházát képes létrehozni. Az egyenes vagy elágazó láncok többféle módon egymáshoz is csatlakozhatnak, ami igen bonyolult molekulák létrehozásához vezethet. A szén gyakran nitrogénnel, oxigénnel, különböző halogénekkel, foszfor- vagy kénatomokkal is képez vegyületeket, mely tovább gyarapítja a szerves vegyületek sokszínűségét.
A szenet, egyedülálló vegyületképző tulajdonságai miatt nemcsak változatosság, de sokoldalúság is jellemzi. A vegyületképző tulajdonságok egyike a széles körű izomerek lehetősége, ami azt jelenti, hogy egy bizonyos atomcsoport nemcsak egy meghatározott vegyületet tud képezni, de többet, aszerint hogy az egyes atomok hogyan kapcsolódnak kémiailag egymáshoz, vagy milyen a térbeli elrendezésük. Mindezek miatt a vegyületek alkalmazási területe óriási. A szerves kémia az alapja vagy fontos alkotórésze a műanyagiparnak, gyógyszeriparnak, festékiparnak, robbanóanyag-iparnak, élelmiszeriparnak, kőolajiparnak, petrolkémiának stb.
Néhány kivételtől eltekintve a szerves vegyületek képezik az életfolyamatok alapját is. Helyettesítési reakciók útján különleges hatáskört elvégző vegyületek jöhetnek létre, úgy mint a biológiai rendszerek katalizátorainak (ezek az enzimek) kiterjedt csoportja. Ezeknek a jellegzetes, csaknem ön-propagáló tulajdonsága nélkül életfolyamatokat nehéz lenne elképzelni.
Egyes jelenlegi tárgykörirányzati témák: királis kémia, zöld (környezetvédelmi) kémia, mikrohullám-kémia, fullerének és mikrohullámú spektroszkópia. Ez utóbbi már a szerves vegyületek tucatjait mutatta ki az intersztelláris (csillagok közötti) világűrben. A fullerének szerves vegyületekből előállítható komplex atomcsoportok, melyek csak szénatomokból állnak, vagyis a szén allotrop módosulatainak tekinthetők.
A szerves vegyületek leírása és nómenklatúrája[szerkesztés]
A szerves vegyületek pontos leírásához az egyes atomok egymáshoz való kapcsolódásának és térbeli elrendeződésének ismerete is szükséges.
1. Szerkezeti képlet[szerkesztés]

A molekulaképlet (pl. CH4, C6H12O6) nem elegendő a szerves vegyületek bonyolult összetételének leírására. Ismerni kell az atomok kapcsolódási sorrendjét vagy más néven konstitúcióját, valamint az atomok egymáshoz viszonyított térbeli elrendeződését is.
Azonban a valódi szerkezet általában nagyon bonyolult, leírása sok adatot igényel.
Szerves vegyületek szerkezete szerkezeti képletük segítségével írható le. Ezek nagyon változatosak: pl. konstitúciós képlet, egyszerűsített konstitúciós képlet, az atomok egymáshoz viszonyított térbeli elrendeződését részben tükröző egyszerű konstitúciós képlet. A legegyszerűbbek azonban az úgynevezett vonalképletek, ahol a szénatomok nem a vegyjelükkel vannak jelölve, hanem a vonalak töréspontja feleltethető meg velük. A töréspontok közötti egyenes vonal feleltethető meg az atomok közötti kovalens kötéssel. Kettős és hármas kötés esetén az egyenes vonal is duplázódik vagy triplázódik (ez alatt két vagy három egymással párhuzamos vonalat kell érteni, melyek szorosan egymás mellé vannak rendezve). A szénatomok minden szabad vegyértékét egy hidrogénatom foglalja le, de az egyszerűség és átláthatóság érdekében a szénatomokhoz kapcsolódó hidrogénatomok ritka kivételektől eltekintve nincsenek ábrázolva a vonalképletekben.
A bután molekulaképlete: C4H10.
A következő ábrák a normál bután (n-bután) különböző szerkezeti képleteit mutatják:
A normál bután konformációs képletei:

|
A normál bután konstitúciós izomerje (láncizomer) a 2-metilpropán vagy izobután:
2. A szerves kémia nómenklatúrája[szerkesztés]
A szerves vegyületek nagy száma és változatossága miatt a kémikusok már kezdetben is felismerték, hogy igen fontos a szerves vegyületek elnevezésére egy nemzetközileg elfogadott rendszert felállítani. A genfi nómenklatúra egy nemzetközi gyűléssorozat eredményeképpen jött létre 1892-ben.
Azt is felismerték, hogy bármely rendszer a szerves anyagok számának gyarapodásával el fog avulni, bővítésére és változtatásokra lesz szükség. Végül ezt a feladatot az International Union of Pure and Applied Chemistry, IUPAC (vagyis az Elméleti és Alkalmazott Kémia Nemzetközi Egyesülete) kapta meg.
Annak felismerése eredményeképpen pedig, hogy a biokémia vegyületeinek bonyolultsága még az azelőtt felfedezett vegyületeknél is sokkal bonyolultabb lehet, a IUPAC és az International Union of Biochemistry and Molecular Biology, IUBMB (vagyis a Biokémia és Molekuláris Biológia Nemzetközi Egyesülete) a szerves vegyületek elnevezésére együttesen egy javaslati listát létesített. Az elnevezési, nomenklaturális javaslatokat J.P. Moss[3] összefoglalta, ami számítógépen böngészhető.
Több vegyület esetében a közönséges vagy triviális nevük is használatosak, melyek előnye, hogy általában egyszerűek, rövidek, és elterjedtek.
Fének[szerkesztés]
A szerves vegyületek számának és bonyolultságának növekedésével további egyszerűsítésre lett szükség, és új javaslatok születtek. Az első ilyen javaslat 1951-ben született, amikor egy bonyolult vegyület több ciklikus benzol gyűrűs alkotórészét[pontosabban?] ciklofénnek neveztek. Későbbi javaslatok a módszert kiterjesztették, és hasonló bonyolult vegyületek egyszerűsített, komplex gyűrűcsoportból álló alkotórészeit, amelyek között heterociklusos csoportok is szerepelhetnek, féneknek neveztek, aminek az eredményeképpen a 'fén' az egész osztály neve lett. Ez indította a fén nómenklatúrát.[4]
Szerves vegyületek osztályozása[szerkesztés]
Megkülönböztetnek szénhidrogéneket, valamint funkciós csoportot tartalmazó szerves vegyületeket.
- 1. Szénhidrogének
A szénhidrogének molekuláit csak szén- és hidrogénatomok építik fel.
A szénhidrogének két nagy csoportját különböztetik meg: alifás és aromás szénhidrogének. Az alifás szénhidrogének közé sorolják a telített és telítetlen szénhidrogéneket.
A telített szénhidrogéneknek láncforma szerint két fő csoportja van: nyílt láncú és zárt láncú (gyűrűs) vegyületek. Ha a molekulában mindkettő jelen van, akkor azt a zárt láncúak közé sorolják.
Az alkánok nyílt láncú, telített szénhidrogének, a cikloalkánok zárt láncú (gyűrűs) vegyületek.
A telítetlen szénhidrogéneket felosztják kettős kötést tartalmazó alkénekre (olefinek), gyűrűs (ciklikus) cikloalkénekre, valamint hármas kötéses alkinekre (acetilén szénhidrogének).
Az aromás szénhidrogének (arének) közé sorolják a benzolt és a benzollal rokon vegyületeket.
- 2. Funkciós csoportot tartalmazó szerves vegyületek
A funkciós csoportot tartalmazó szénvegyületekben szénen és hidrogénen kívül más organogén elemek atomjai is előfordulnak: oxigén, nitrogén, kén, halogének. Ezeket heteroatomoknak nevezik. Ebből kifolyólag a funkciós csoportot tartalmazó szerves vegyületeket még heteroatomos szénvegyületeknek is nevezik. Más források a szénhidrogén-származékok megnevezést használják, mert ezek a vegyületek levezethetők az egyszerűbb szénhidrogénekből, ha azok egy vagy több hidrogénatomját egy funkciós csoporttal helyettesítik.
- Funkciós csoportok
- A funkciós csoport olyan heteroatom vagy heteroatomot tartalmazó atomcsoport, melynek jelentős hatása van a vegyület kémiai és fizikai tulajdonságaira. Azok a vegyületek, amelyek ugyanazt a funkciós csoportot tartalmazzák, egymáshoz hasonlóan viselkednek (pl. pH, kémiai reaktivitás, oxidációval szembeni ellenálló képesség stb.).
A szerves vegyületek csoportosítása[szerkesztés]
- 1. Szénhidrogének
- Telített szénhidrogének
- Nyílt láncú szénhidrogének
- Zárt láncú (gyűrűs) szénhidrogének
- Cikloalkánok (Cikloparaffinok)
- Telítetlen szénhidrogének
- Aromás szénhidrogének
- Telített szénhidrogének
- 2. Funkciós csoportot tartalmazó szénvegyületek
- Halogénvegyületek
- Hidroxivegyületek
- Éterek
- Nitrogéntartalmú vegyületek
- Oxovegyületek
- Szénhidrátok (szacharidok)
A szerves vegyületek reakciótípusai[szerkesztés]
A szerves reakciók típusai lehetnek: szubsztitúciós-, addíciós-, eliminációs és átrendeződéses reakciók. A szerves reakciók jellege: több lépéses és összehangolt, azaz ionos-, gyökös- és elektrociklusos reakciók.
- Analízis és szintézis
- A kémiai analízis segítségével meghatározható egy vegyület kémiai összetétele, szerkezete. Ide tartozik a minőségi és mennyiségi analízis. A kémiai analízissel a kémia egyik ága, az analitikai kémia foglalkozik.
- A szerves kémiai analízis segítségével megállapítható a vegyület elemi összetétele, molekulatömege, százalékos összetétele, majd ebből kiszámítható a molekulaképlete vagy más néven összegképlete.
- A szerkezeti képlet megállapítása már bonyolultabb folyamat.
- A kémiai szintézis olyan kémiai folyamat, melynek segítségével több kisebb molekulából, újabb szén−szén vagy szén- és heteroatom közötti kötések kialakításával, egy összetettebb molekula hozható létre. A szintézis a szerves vegyületek egyik előállítási módszere, melynek során új, tudományos, technológiai vagy gyógyászati szempontból érdekes, hasznos vegyületek (pl. polimereket) nyerhetők. Ugyanakkor a kémiai szerkezet bizonyításra is alkalmas.
Jegyzetek[szerkesztés]
- ↑ a b Hans Breuer: Kémia. Atlasz sorozat. Athenaeum 2000 Kiadó Kft., 2003., 265. oldal. ISBN 963-9471-35-6
- ↑ Furka Árpád: Szerves kémia, 17. oldal. Nemzeti Tankönyvkiadó, 1998. ISBN 963-19-2784-9
- ↑ International Union of Pure and Applied Chemistry - Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. http://www.chem.qmul.ac.uk/iupac/ World Wide Web material prepared by G. P. Moss, Department of Chemistry, Queen Mary University of London,Mile End Road, London, E1 4NS, UKg.p.moss@qmul.ac.uk
- ↑ International Union of Pure and Applied Chemistry - Organic Chemistry Division - Commission on nomenclature of organic chemistry http://www.chem.qmul.ac.uk/iupac/phane/ Archiválva 2006. július 3-i dátummal a Wayback Machine-ben Phane Nomenclature Part I: Phane Parent Names IUPAC Recommendations 1998 Prepared for publication by W. H. Powell 1436 Havencrest Ct, Columbus, OH 43220-3841, USA