Hibridizáció

A kémiában a hibridizáció a kémiai kötés leírására szolgáló egyik elmélet, a vegyértékkötés-elmélet módszere: az atompályák keverésével olyan új hibridpályákat hoz létre, melyek alkalmasak az atomok közötti kötés jellemzőinek leírására. A hibridpályák jól használhatók a molekulapályák alakjának magyarázására.
A hibridizáció elméletét Linus Pauling vezette be,[1] hogy megmagyarázza az olyan molekulák szerkezetét, mint például a metán (CH4). Ezt az eljárást eredetileg csak az ilyen egyszerű kémiai rendszerekre fejlesztették ki, de később szélesebb körben is alkalmazni kezdték, és ma a szerves vegyületek szerkezetének leírásában hatékony heurisztikának tekintik.
A hibridizációs elmélet kvantitatív számításokra nem annyira alkalmas, mint a molekulapálya-elmélet. Különösen a d pályák bevonása esetén – például a koordinációs kémia és a fémorganikus kémia területén – lépnek fel nehézségek. Bár a hibridizációs sémák használhatók az átmenetifémek kémiájában, ezek általában nem annyira pontosak.
Fontos megjegyezni, hogy a pályák az elektronok molekulán belüli viselkedésének leírására szolgáló modellek. Az egyszerű hibridizáció esetén ez a közelítés a hidrogén atompályáin alapul. A hibridpályákat ezen atompályák – különböző arányú – keverékének tekintjük. Az egyszerű hibridizációs sémák alapjául azért a hidrogén pályáit választjuk, mert ezek azon kevés pályák közé tartoznak, melyekre a Schrödinger-egyenletnek pontos analitikus megoldása van. A nehezebb atomok, például a szén, nitrogén és oxigén esetén feltételezzük, hogy ezek a pályák valamelyest torzulnak, de nem jelentős mértékben. A hibridizáció elmélete ilyen feltételek esetén használható a leghatékonyabban. Meg kell jegyezni, hogy a molekulák leírásához nincs szükség a hibridizációra, de a szénből, nitrogénből és oxigénből (valamint, bár kisebb mértékben, a kénből és foszforból) álló molekulák esetén a hibridizációs elmélet/modell sokkal egyszerűbbé teszi a leírást.
A hibridizációs elmélet fő felhasználási területe a szerves kémia, azon belül is leginkább a szén, nitrogén és oxigén (kisebb mértékben a foszfor és a kén) atomokra vonatkozóan alkalmazzák. A hibridizáció magyarázata a metán kötéseinek leírásával kezdődik.
sp3 hibridállapot[szerkesztés]
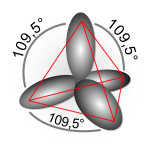
A hibridizáció a kötésben részt vevő atomokat az atom szemszögéből írja le. Egy tetraéderes koordinációjú szénatomnak (mint például a metánban CH4) 4 megfelelő szimmetriájú pályájának kell lennie, mellyel a 4 hidrogénhez kapcsolódik. A metán létezésének problémája a következő: a szén alapállapotú elektronkonfigurációja 1s2 2s2 2px1 2py1, vagy szemléletesebben:
A vegyértékkötés-elmélet azt jósolná – a két félig betöltött p típusú pálya létezése miatt (a px py vagy pz jelöléseknek most nincs jelentősége, mivel nincs semmilyen meghatározott betöltődési sorrendjük) –, hogy a szén két kovalens kötést létesít, azaz CH2 (metilén) keletkezik. A metilén azonban egy rendkívül reakcióképes molekula (lásd még: karbén). Ez az elmélet önmagában tehát nem képes megmagyarázni a CH4 létezését.
Az alapállapotú pályák nem tudnak részt venni a CH4 kötéseiben. Bár a 2s elektronok 2p szintre történő gerjesztése elméletileg lehetővé teszi négy kötés létrehozását, ez azonban azzal járna, hogy a CH4 különböző kötéseinek energiája eltérne a pályák eltérő átfedése miatt. Ezt azonban a kísérleti eredmények nem igazolják: a szénatomról bármely hidrogén egyformán könnyen távolítható el.
Összefoglalásként megállapítható, hogy a CH4 (és sok más molekula) létezésének magyarázatára olyan módszer szükséges, amellyel (átmenetifémek esetén) akár 12 egyforma erősségű (és így azonos hosszúságú) kötés is létrehozható.
A hibridizáció első lépése egy (vagy több) elektron gerjesztése (promóció). A metán szénatomján bemutatva:
A hidrogén magját jelentő proton vonzó hatást fejt ki a szén egyik kisebb energiájú vegyértékelektronjára. Ez a gerjesztő hatás az egyik 2s elektront a 2p pályára mozdítja. Ez azonban növeli a szénatom vegyértékelektronokra ható vonzását, mivel növeli az effektív magtöltést (annak a töltésnek a nagysága, mellyel a mag egy adott elektronra hat = a mag töltése − a maghoz közelebb levő elektronok összes töltése).
Ezeknek az erőknek a kombinációja új matematikai függvényeket hoz létre: ezek a hibrid pályák. A szénatom esetén, amely négy hidrogénnel alakítana ki kötést, négy pálya szükséges. A 2s pálya (az atomtörzs elektronjai szinte soha nem vesznek részt a kötésben) tehát „keveredik” a három 2p pályával, így négy sp3 hibridpálya keletkezik (ejtsd: es-pé-három). Alább látható ennek grafikus összefoglalása.
A CH4 esetén a négy sp3 hibrid pálya a hidrogén 1s pályáival kerül átfedésbe, így négy σ (szigma) kötés (azaz négy egyszeres kovalens kötés) jön létre. A négy kötés hossza és erőssége azonos. Az elmélet megfelel az elvárásoknak.
Egy alternatív nézet: Tekintsük a szenet C4− anionnak. Ebben az esetben a szén minden atompályája be van töltve:
Ha most ezeket a pályákat a 4 hidrogén (4 proton, H+) üres s-pályáival kombináljuk, és megengedjük a 4 hidrogén maximális térbeli elkülönülését (azaz a szénatom körüli tetraéderes elrendeződést), akkor azt látjuk, hogy a p-pályák bármilyen orientációjánál az egyes hidrogéneknek a szén s-pályájával 25%-os, és a 3 p-pályával összesen 75%-os átfedése van (vegyük észre, hogy a százalékok aránya ugyanakkora, mint a megfelelő atompálya karaktere az sp3-hibrid modellben: 25% s- és 75% p-karakter).
A hibridizáció elmélete alapján a metánban a vegyértékelektronok energiájának azonosnak kell lennie, de a fotoelektron-spektrumban[2] két sáv található, az egyik 12,7 eV energiánál (egy elektronpár), és a másik 23 eV-nál (három elektronpár). Ez a nyilvánvaló ellentmondás feloldható, ha feltételezzük, hogy az sp3 pályák és a 4 hidrogén pályájának keveredésekor további pályakeveredés is fellép.
sp2 hibridállapot[szerkesztés]
Más szénalapú vegyületek és egyéb molekulák is a metánhoz hasonlóan írhatók le. Vegyük például az etilént (C2H4). Az etilénben a két szénatom között kettős kötés van, a szerkezete így néz ki:

A szén sp2 hibridizációjú lesz, mivel a hibrid pályák csak σ-kötéseket hoznak létre és egy π-kötés szükséges a két szén közötti kettős kötéshez. A szén–hidrogén kötések mindegyike azonos erősségű és hosszúságú, ami egyezik a kísérleti adatokkal.
Az sp2 hibridállapotban a 2s pálya a három 2p pálya közül csak kettővel keveredik:
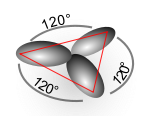
3 sp2 pálya képződik, és marad egy p-pálya. Az etilénben a két szénatom egy σ-kötést létesít az egy-egy sp2 pályájuk átfedése révén, és az egyes szénatomok két-két hidrogénnel kovalenst kötést hoznak létre s–sp2 átfedésekkel, melyek mindegyik 120° szöget zár be egymással. A szénatomok közötti π-kötés, mely a 2p–2p átfedés révén keletkezik, merőleges a molekula síkjára.
A p-karakter nem csak egész szám lehet, például sp2,5 hibridállapotot is leírnak. Ebben az esetben a geometria az ideális hibridállapotú esethez képest valamelyest torzul. A Bent-szabály értelmében például az elektronegatívabb szubsztituens felé irányuló kötésnek általában nagyobb a p-karaktere.
sp hibridállapot[szerkesztés]
Az alkinekhez hasonló hármas kötést tartalmazó vegyületek értelmezése sp hibridizáció útján lehetséges.
Ebben a modellben a 2s pálya a három közül csak egy p-pályával keveredik, így két sp pálya és két változatlan p pálya lesz. Az acetilénben (C2H2) levő kémiai kötés a két szénatom sp–sp pályájának átfedése révén kialakuló σ-kötés, és két további π-kötés, melyeket p–p átfedés hoz létre. Mindkét szén egy-egy hidrogénnel is kötésbe lép egy szigma s–sp átfedéssel, melyek 180° szöget zárnak be.
Hibridizáció és a molekula alakja[szerkesztés]
A hibridizáció a vegyértékelektronpár-taszítási elmélethez hasonlóan segít leírni a molekulák alakját:
- AX1 (pl. LiH): nincs hibridizáció, lineáris molekula
- AX2 (pl. BeCl2): sp hibridizáció; lineáris vagy diagonális alak, a kötésszög cos−1(−1) = 180°
- AX2E (pl. GeF2): hajlított/V-alak, < 120°
- AX3 (pl. BCl3): sp2 hibridizáció; síkháromszög alak; a kötésszög cos−1(−1/2) = 120°
- AX3E (pl. NH3): trigonális piramis, 107°
- AX4 (pl. CCl4): sp3 hibridizáció; tetraéder alak, a kötésszög cos−1(−1/3) ≈ 109,5°
- AX5 (pl. PCl5): sp3d hibridizáció, trigonális bipiramis alak
- AX6 (pl. SF6): sp3d2 hibridizáció, oktaéderes (vagy négyzetes bipiramisos) alak
Ezek akkor igazak, ha a központi atomnak nincsenek nemkötő elektronpárjai. Ha vannak, akkor azokat bele kell számolni Xi-be, de a kötésszögek az erősebb taszító hatás miatt kisebbek lesznek. A vízben H2O például az oxigénatom két hidrogénhez kapcsolódik és van két nemkötő elektronpárja, amit úgy tekinthetünk, mintha az oxigénhez négy „egység” kapcsolódna. A molekula modellje tehát sp3 hibridizációjú AX4, és az elektronok elrendeződése a H2O-ban tetraéderes. Ez egyezik a vízmolekula kísérletileg meghatározott alakjával, V alakú, hajlított szerkezet, a kötésszög 104,5° (a két nemkötő pár nem látható).
Általában ha egy atom s- és p-pályáiból egymással szöget bezáró hi és hj hibridpályák keletkeznek, akkor 1 + ij cos() = 0. A hi pályában a p- és s- pályák aránya i2, a hj hibridpályában pedig j2. Abban a speciális esetben, ha ugyanazon az atomon ekvivalens hibridek vannak, közbezárt szöggel, akkor az egyenlet egyszerűsödik: 1 + 2 cos() = 0. Például a BH3 síkháromszöges geometriájú, a három kötésszög benne 120°, a bóratomon három egyenértékű hibridpálya van , így 1 + 2 cos() = 0 alapján 1 + 2 cos(120°) = 0, ebből a p- és s-pályák arányára 2 = 2 adódik, azaz sp2 hibrid, amint az a fenti lista alapján várható.
A d-pályák részvételével kapcsolatos problémák[szerkesztés]
A hibridizáció elmélete néhány esetben nem működik, főleg a d-pályák kémiai kötésben való részvételének energiaviszonyait nem tudja jól megmagyarázni (lásd fentebb az sp3d és sp3d2 hibridizációt). Ez az alábbi példán mutatható be. Gondoljuk végig, hogy az elmélet hogyan írja le a foszfor-pentaklorid (PCl5) kötéseit. A d-pályák kiterjedése nagy, az atommagtól viszonylag távol helyezkednek el, és nagy az energiájuk. A pályák magtól való radiális távolsága alapján úgy tűnhet, hogy a d-pályák energiaszintje túl magas ahhoz, hogy az s- és p-pályákkal keveredjen (3s: 47 pm; 3p: 55 pm; 3d: 240 pm). Első ránézésre tehát valószínűtlennek látszik, hogy sp3d hibridizáció jöjjön létre.
A pályák méretét (és energiáját) befolyásoló tényezők alaposabb vizsgálata azonban további szempontokat tár fel. Az egyik ilyen tényező a központi atom formális töltése. Nyilvánvaló, hogy a PCl5 molekulában a foszforatomnak elég nagy parciális pozitív töltése van. Ennek következtében a 3d pályák mérete olyan mértékben csökken, ami már elképzelhetővé teszi az s- és p-pályákkal történő hibridizációt. Figyeljük meg azokat az eseteket, amelyekben a d-pályák hibridpályákban való részvételét feltételezik: SF6(kén-hexafluorid), IF7, XeF6; mindegyik molekulában a központi atomot nagy elektronegativitású fluoratomok veszik körül, ami valószínűvé teszi az s-, p- és d-pályák hibridizációját. További vizsgálatok alapján az is ismert, hogy a pályák mérete függ a rajta elhelyezkedő elektronok számától is. A d-pályák elektronjainak párosodása is, bár kisebb mértékben, de csökkenti a pályák méretét.
A molekulapálya-elmélet ugyanakkor sokkal tisztább képet ad ezen molekulák kötésrendszeréről.
A hibridizáció és az MO-elmélet[szerkesztés]
A hibridizáció elmélete fontos része a szerves kémiának. A magasabb szintű szerves kémiai könyvekben a molekulapálya-elmélettel együtt tárgyalják, bár eltérő okokból. Az egyik könyv megjegyzi, hogy a reakciómechanizmus felállításához olykor a kötés klasszikus elképzelése szükséges, amelyben 2 elektron megoszlik két atom között.[3] Azt is említi, hogy a metánban a kötésszöget az MO-elmélet nem képes egyszerűen megmagyarázni. Egy másik könyv az alkének kötésrendszerének tárgyalásánál foglalkozik a hibridizációval,[4] míg egy harmadik könyv[5] a hidrogénmolekula kötését az MO-elmélettel tárgyalja, ugyanakkor a metánét a hibridizációval írja le.
Bár a hibridizáció elmélete, vagy ismertebb nevén a vegyértékkötés-elmélet által használt nyelvezetet és képeket széles körben használják a szintetikus szerves kémiában, a kötésnek ezt a fajta kvalitatív vizsgálatát a kémia többi ágában már nagyrészt felváltotta a molekulapálya-elmélet. A szervetlen kémiai leírásokban például a hibridizáció tanítása már csak a történeti lábjegyzetekben szerepel.[6][7] A hibridizáció egyik jellegzetes hibája, hogy számos molekula fotoelektron-spektrumát rosszul adja meg, olyan alapvető anyagok esetén is, mint például a metán vagy a víz. Pedagógiai szempontból a hibridizáció hajlamos túl nagy hangsúlyt fektetni a kötő elektronok lokalizációjára, és nem használja fel olyan hatékonyan a molekuláris szimmetriát, mint az MO-elmélet.
Jegyzetek[szerkesztés]
- ↑ L. Pauling, J. Am. Chem. Soc. 53 (1931), 1367
- ↑ photo electron spectrum of methane 1 Archiválva 2011. július 20-i dátummal a Wayback Machine-ben photo electron spectrum of methane 2 Archiválva 2009. március 27-i dátummal a Wayback Machine-ben
- ↑ Organic Chemistry. Jonathan Clayden, Nick Greeves, Stuart Warren, and Peter Wothers 2001 ISBN 0-19-850346-6
- ↑ Organic Chemistry, Third Edition Marye Anne Fox James K. Whitesell 2003 ISBN 978-0-7637-3586-9
- ↑ Organic Chemistry 3rd Ed. 2001 Paula Yurkanis Bruice ISBN 0-13-017858-6
- ↑ G. L. Miessler and D. A. Tarr “Inorganic Chemistry” 3rd Ed, Pearson/Prentice Hall publisher, 2003. ISBN 0-13-035471-6.
- ↑ Shriver, D. F.; Atkins, P. W.; Overton, T. L.; Rourke, J. P.; Weller, M. T.; Armstrong, F. A. “Inorganic Chemistry” W. H. Freeman, New York, 2006. ISBN 0-7167-4878-9.
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben az Orbital_hybridisation című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
További információk[szerkesztés]
- Covalent Bonds and Molecular Structure Archiválva 2009. február 10-i dátummal a Wayback Machine-ben
- Hybridisation flash movie
- Hybridised orbital 3D preview program in OpenGL
- Understanding Concepts: Molecular Orbitals Archiválva 2013. április 11-i dátummal az Archive.is-en
- Szerves kémia










