Benzimidazol
| Benzimidazol | |||

| |||
 |
| ||
| IUPAC-név | 1H-benzimidazol | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 51-17-2 | ||
| PubChem | 5798 | ||
| ChemSpider | 5593 | ||
| KEGG | C02009 | ||
| ChEBI | 41275 | ||
| |||
| |||
| InChIKey | HYZJCKYKOHLVJF-UHFFFAOYSA-N | ||
| UNII | E24GX49LD8 | ||
| ChEMBL | 306226 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C7H6N2 | ||
| Moláris tömeg | 118,14 g/mol | ||
| Olvadáspont | 170–172 °C | ||
| Savasság (pKa) | 12,8 (benzimidazol) és 5,6 (konjugált sav)[1] | ||
| Veszélyek | |||
| MSDS | Külső MSDS | ||
| EU osztályozás | ártalmas (Xn) | ||
| R mondatok | R20 R21 R22 R36 R37 R38 | ||
| S mondatok | S26 S36 | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
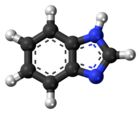
A benzimidazol heterociklusos aromás szerves vegyület. Kétgyűrűs molekula, kondenzált benzol- és imidazolgyűrűből áll. A legjelentősebb természetes benzimidazol-származék az N-ribozil-dimetilbenzimidazol, mely a B12-vitaminban a kobalthoz kapcsolódó axiális ligandum.[2]
A benzimidazol kondenzált gyűrűs nitrogéntartalmú heterociklusos vegyület, N-heterociklusos karbének szénvázaként használják. Az N-heterociklusos karbéneket rendszerint átmenetifém-komplexekben alkalmazzák ligandumként. Ezeket gyakran N,N'-diszubsztituált benzimidazolínium sók 2-es pozícióban bázis hatására bekövetkező deprotonálásával állítják elő.[3][4]
Előállítása[szerkesztés]
A benzimidazol kereskedelmi forgalomban kapható. A szokásos szintézise o-fenilén-diamin és hangyasav kondenzációjával történik,[5] de a megfelelő trimetil-ortoformiát is használható:
- C6H4(NH2)2 + HC(OCH3)3 → C6H4N(NH)CH + 3 CH3OH
A karbonsav változtatásával ez a módszer általánosan használható 2-szubsztituált származékok előállítására.[5] A benzimidazol fungicid sajátosságokkal is rendelkezik. Hatását a gombák mikrotubulusaihoz kapcsolódva fejti ki, megakadályozva a hifanövekedést. Az osztódási orsó mikrotubulusait felépítő fehérjéhez, a tubulinhoz is kötődik,[6] ezáltal blokkolja a sejtmag osztódását.
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Benzimidazole című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások[szerkesztés]
- ↑ Walba, H. & Isensee, R. W. Acidity constants of some arylimidazoles and their cations. J. Org. Chem. 26, 2789-2791 (1961).
- ↑ H. A. Barker, R. D. Smyth, H. Weissbach, J. I. Toohey, J. N. Ladd, and B. E. Volcani (1960. február 1.). „Isolation and Properties of Crystalline Cobamide Coenzymes Containing Benzimidazole or 5,6-Dimethylbenzimidazole”. Journal of Biological Chemistry 235 (2), 480–488. o. [2009. február 11-i dátummal az eredetiből archiválva]. PMID 13796809. (Hozzáférés: 2013. március 20.)
- ↑ R. Jackstell, A. Frisch, M. Beller, D. Rottger, M. Malaun and B. Bildstein (2002). „Efficient telomerization of 1,3-butadiene with alcohols in the presence of in situ generated palladium(0)carbene complexes”. Journal of Molecular Catalysis A: Chemical 185 (1–2), 105–112. o. DOI:10.1016/S1381-1169(02)00068-7.
- ↑ H. V. Huynh, J. H. H. Ho, T. C. Neo and L. L. Koh (2005). „Solvent-controlled selective synthesis of a trans-configured benzimidazoline-2-ylidene palladium(II) complex and investigations of its Heck-type catalytic activity”. Journal of Organometallic Chemistry 690 (16), 3854–3860. o. DOI:10.1016/j.jorganchem.2005.04.053.
- ↑ a b E. C. Wagner and W. H. Millett (1943). „Benzimidazole”. Org. Synth.. ; Coll. Vol. 2: 65.
- ↑ Szentirmai Attila: Mikroszkóppal vizsgálható gombák birodalma (pdf, 26. oldal). (Hozzáférés: 2013. április 20.)
További információk[szerkesztés]
- Grimmett, M. R.. Imidazole and benzimidazole synthesis. Boston: Academic Press (1997). ISBN 0-12-303190-7
Kapcsolódó szócikkek[szerkesztés]
- Benzimidazolin
- Polibenzimidazol, nagyteljesítményű műszál
- Indol, a 3-as helyzetű nitrogén helyett CH csoport tartalmazó vegyület
- Purin, a hattagú gyűrűben további két nitrogénatomot tartalmazó vegyület
- Egyszerű aromás gyűrű
