Adenozin-trifoszfát
| Adenozin-trifoszfát | |||

| |||
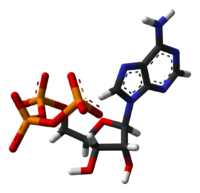
| |||
| IUPAC-név | 5-(6-aminopurin-9-il)-3,4-dihidroxioxolán-2-il-metoxi-hidroxifoszforil-oxi-hidroxifoszforil-oxifoszfonsav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 56-65-5 | ||
| PubChem | 5957 | ||
| ChemSpider | 5742 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C10H16N5O13P3 | ||
| Moláris tömeg | 507,181 g mol-1 | ||
| Olvadáspont | 176 °C (bomlik)[1] | ||
| Savasság (pKa) | 6,5 | ||
| Veszélyek | |||
| EU osztályozás | nincsenek veszélyességi szimbólumok[1] | ||
| R mondatok | nincs[1] | ||
| S mondatok | nincs[1] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Az adenozin-5′-trifoszfát (ATP) egy többfunkciós nukleotid, amely a sejten belüli energiaátvitel legkisebb molekuláris egysége.
Az ATP kémiai energiát szállít a sejten belül az anyagcsere folyamataiban. Emberi szervezetben egyszerre csak kb. 250 g van jelen,[2] de fokozott felhasználását jellemzi az, hogy naponta a testtömegnek megfelelő mennyiség fogy belőle.[3] Ez úgy lehetséges, hogy az ATP folyamatosan újrahasznosul. Jelentős izommunka esetén ez az érték akár fél kilogramm is lehet – percenként.[4] Az energia a foszfátcsoportok közötti kötésekben raktározódik. Egy csoport leszakadásával átlag 30 kJ energia szabadul fel mólonként.
A fotoszintézis és a sejtlégzés folyamataiban energiaforrásként szerepel, és egy sor enzim és sejtfolyamat fogyasztja a bioszintetikus reakciók, a sejtmozgás és a sejtosztódás során.
Az ATP-t a nukleinsavakba is beépítik a polimerázok a DNS-replikáció folyamatában és a transzkripcióban.
A jelátviteli (szignáltranszdukciós) folyamatokban az ATP a kinázok és az adenilát-cikláz enzim szubsztrátja. A kinázok a proteineket és a lipideket foszforilálják. Az adenilát-cikláz pedig egy másodlagos hírvivő molekulát (second messenger), cAMP-t képez az ATP-ből.
A molekula szerkezete egy purinbázisból áll (adenin), amely egy pentóz (ribóz) 1′-es szénatomjához kötődik. A három foszfátcsoport a pentózrész 5′-ös szénatomjához kapcsolódik.
DNS-szintézis közben az ATP-ben a ribóz cukorrész a ribonukleotid-reduktáz enzim hatására először dezoxiribózzá alakul.
Az ATP-t 1929-ben Karl Lohmann fedezte fel, majd 1941-ben Fritz Albert Lipmann feltételezte róla először, hogy ez a fő energiaszállító molekula a sejtekben.
Érdekesség[szerkesztés]
- Szent-Györgyi Albert és munkatársa, Banga Ilona már 1942-ben kidolgozott egy technológiai eljárást viszonylag magas ATP-tartalmú állati takarmány, illetve takarmány-adalékanyag gyártására. Ehhez a vágás előtt legalább három napig pihentetett, de folyamatosan jól tartott vágólovak megdarált, zsírtalanított, legkésőbb 40 percen belül tömény, hideg alkohollal elkevert, majd legvégül légszárazra szárított húsát használták fel. Az eljárás része 6 percnyi, alkoholban való főzés is, ami valamelyest csökkenti a termék ATP-tartalmát, de ennyi hőkezelésre szükség van az anyagban lévő fehérjék denaturálásához. A megfelelő technológiai fegyelem betartásával az így előállítható, fűrészporszerű, világos színű, szagtalan végtermék kilogrammonként 7-8 gramm oldható, kitermelhető ATP-t tartalmaz (vágóállatonként a felhasználható izomhús mennyisége átlagosan kb. 60 kilogramm).[5]
Jegyzetek[szerkesztés]
- ↑ a b c d Biztonsági adatlap (Sigma-Aldrich)
- ↑ 'Nature's Batteries' May Have Helped Power Early Lifeforms. Science Daily, 2010. május 25. [2010. május 27-i dátummal az eredetiből archiválva]. (Hozzáférés: 2014. március 9.) „At any one time, the human body contains just 250g of ATP...”
- ↑ Törnroth-Horsefield S, Neutze R (2008. december 1.). „Opening and closing the metabolite gate”. Proc. Natl. Acad. Sci. U.S.A. 105 (50), 19565–6. o. DOI:10.1073/pnas.0810654106. PMID 19073922. (Hozzáférés: 2014. március 9.)
- ↑ Ádám Veronika, Dux László et al., Orvosi Biokémia. Szerk. Ádám Veronika. Budapest: Medicina Könyvkiadó, 2004. 60.
- ↑ Szárított lóhús, mint ATP-forrás ideiglenes előállítási technológiájának jóváhagyási ügye. 1955. június 21. Magyar Nemzeti Levéltár Országos Levéltára, XIX-K-1-c-097, 00526/1955
Források[szerkesztés]
- Dr. Otto-Albrecht Neumüller: Römpp vegyészeti lexikon. Műszaki Könyvkiadó, 1983., 1. kötet, 45–46. oldal. ISBN 963-10-3269-8
| A citromsavciklus anyagcsere-útvonala | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
