Peptidnukleinsav
A peptidnukleinsav (PNS) a DNS-hez és az RNS-hez hasonló, mesterségesen előállított polimer.[1]
A peptidnukleinsav-oligomerek 2017-től molekuláris biológiai folyamatokban, diagnosztikai assay-kben és antiszensz terápiákban használatosak.[2] Nagyobb kötéserősségük miatt nem kell e célokra hosszú PNS-oligomer, melyek általában 20-25 bázis hosszú oligonukleotidot igényel. A hossz legfőbb célja a specificitás biztosítása. A PNS-oligomerek ezenkívül a komplementer DNS-ekhez való kötésben specifikusabbak: a PNS/DNS bázistévesztés kevésbé stabil a DNS/DNS tévesztésnél. Ez igaz a PNS/RNS duplexekre is. A PNS-t nukleázok és proteázok se ismerik fel, így ellenállnak a katabolizmusnak. A PNS-ek széles pH-tartományban stabilak. Bár a módosítatlan PNS nem halad át a sejtmembránon, a sejten áthatoló peptidek PNS-hez való kovalens kapcsolása növelheti ennek mértékét.[3]
Nem ismert természetesen előforduló PNS, de a N-(2-aminoetil)-glicin, a PNS váza feltehetően a korai földi élet alapja volt, melyet cianobaktériumok állítanak elő, és neurotoxin.[4]
A PNS-t Peter E. Nielsen, Michael Egholm, Rolf H. Berg és Ole Buchardt hozta létre 1991-ben.[1]
Szerkezet[szerkesztés]
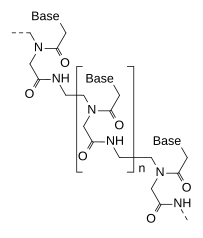
A DNS-nek és az RNS-nek rendre dezoxiribóz és ribózváza van, míg a PNS váza ismétlődő N-(2-aminoetil)-glicinből áll, melyeket peptidkötések kapcsolnak össze. A purin- és pirimidinbázisokat metilénhíd (-CH2-) és karbonilcsoport (-(C=O)-) kapcsolja össze. A PNS-eket gyakran a peptidekhez hasonlóan írják le, első helyen N-terminális, utolsó helyen C-terminális végükkel.[5]
Kötések[szerkesztés]
Mivel a PNS vázában nincs foszfátcsoport, a PNS/DNS-szálak közti kötés erősebb a DNS/DNS-kötés az elektrosztatikus taszítás hiánya miatt. Ez azonban hidrofóbbá teszi, így nehéz a sejtekhez oldatban való szállítása eltávolítás nélkül. Korai, homopiridin szálakkal való kísérletek szerint egy 6 bázisos timin PNS/adenin DNS kettős hélix denaturációs pontja 31 °C volt szemben a megfelelő DNS/DNS duplexszel, mely 10 °C alatt denaturálódik. A vegyes bázisú PNS-ek a DNS-ekhez hasonlóan viselkednek bázispár-felismerés tekintetében. A PNS/PNS kötés erősebb a PNS/DNS kötésnél.
A PNS a DNS-sel tripla hélixet is alkothat.[6]
PNS-transzláció más nukleinsavakból[szerkesztés]
Néhány szerző peptidnukleinsavak szekvenciaspecifikus polimerizációjáról számolt be DNS vagy RNS templátokból.[7][8][9] Liu és társai e polimerizációs módszereket működő PNS-ek létrehozására használták a fehérjékhez, aptamerekhez és ribozimekhez hasonló 3 dimenziós szerkezetek létrehozásához.[7]
PNS-világ-hipotézis[szerkesztés]
Feltételezések szerint a legkorábbi élet PNS-t használhatott annak rendkívüli ellenálló képessége, könnyű létrejötte és lehetséges spontán polimerizációja miatt 100 °C körül.[10] (bár légköri nyomáson a víz e hőmérsékleten forr, a nagyobb nyomású víz magasabb hőmérsékleten forr). Ha így van, az élet csak később tért át DNS/RNS-alapú rendszerre.[11][12] A PNS-világ-hipotézisre azonban nincs egyértelmű bizonyíték.[13] Ha létezett, akkor az RNS-világ előtt kellett léteznie.
Alkalmazása[szerkesztés]
Használatos például génexpresszió-változtatásra inhibitorként és promoterként, továbbá antigén- és antiszensz-terápiához, rák ellen, antivirális, antibakteriális és antiparazita szerként, molekuláris eszközként, bioszenzorként, DNS-szekvenciák észlelésére és a nanotechnológiában.[14][15]
A PNS-ek használhatók nagy sebességű 16S rRNS-génszekvenálásra növény- és talajmintákban az azokat tartalmazó plasztisz- és mitokondriális szekvenciák erősítésének akadályozásával.[16]
Sejtben – Funkcionális antagonizmus/gátlás[szerkesztés]
2001-ben Strauss és társai a PNS-oligomerek élő emlőssejtekben való használatáról számoltak be. A Xist kromatinkötő régiót először nőstény egerek fibroblasztsejtjeiben és embrionális őssejtjeiben találták meg PNS molekuláris antagonistával. A PNS közvetlenül igazolta az lncRNS (hosszú nem kódoló RNS) funkcióját. Az lncRNS, a Xist közvetlenül az inaktív X kromoszómához kötődik. A funkcionális PNS-inhibíciós kísérletek alapján a Xist RNS egyes részei feleltek a kromatinkötésért, így az RNS-átirat doménrégióinak tekinthetők. A PNS molekuláris antagonistát élő sejtekhez adták, és gátolta a Xist inaktív X kromoszómával való asszociációját a nem kódoló RNS élő sejtekben betöltött szerepét vizsgáló PNS-interferenciás leképezéssel. A kísérletekben egy sejten áthaladó 19 bázispáros, a Xist RNS adott részével szembe célzott antiszensz PNS zavarta meg a Xit. A Xi H2A makrohisztonnal való kapcsolatát is gátolta a PNS-interferenciás leképezés.[17]
Jegyzetek[szerkesztés]
- ↑ a b (1991. december 1.) „Sequence-selective recognition of DNA by strand displacement with a thymine-substituted polyamide”. Science 254 (5037), 1497–500. o. DOI:10.1126/science.1962210. PMID 1962210.
- ↑ (2017. október 1.) „Peptide nucleic acids: Advanced tools for biomedical applications”. Journal of Biotechnology 259, 148–159. o. DOI:10.1016/j.jbiotec.2017.07.026. PMID 28764969.
- ↑ (2015. november 1.) „Delivery of cell-penetrating peptide-peptide nucleic acid conjugates by assembly on an oligonucleotide scaffold”. Scientific Reports 5, 17640. o. DOI:10.1038/srep17640. PMID 26612536.
- ↑ (2012. november 7.) „Cyanobacteria Produce N-(2-Aminoethyl)Glycine, a Backbone for Peptide Nucleic Acids Which May Have Been the First Genetic Molecules for Life on Earth”. PLOS ONE 7 (11), e49043. o. DOI:10.1371/journal.pone.0049043. PMID 23145061.
- ↑ (1993. október 1.) „PNA hybridizes to complementary oligonucleotides obeying the Watson-Crick hydrogen-bonding rules”. Nature 365 (6446), 566–8. o. DOI:10.1038/365566a0. PMID 7692304.
- ↑ (2006. június 1.) „Peptide nucleic acid (PNA)—a review”. Journal of Chemical Technology & Biotechnology 81 (6), 892–899. o. DOI:10.1002/jctb.1505.
- ↑ a b (2010. február 1.) „An in vitro translation, selection and amplification system for peptide nucleic acids”. Nature Chemical Biology 6 (2), 148–55. o. DOI:10.1038/nchembio.280. PMID 20081830.
- ↑ (2008. április 1.) „DNA-templated polymerization of side-chain-functionalized peptide nucleic acid aldehydes”. Journal of the American Chemical Society 130 (14), 4646–59. o. DOI:10.1021/ja0753997. PMID 18341334.
- ↑ (2009. július 1.) „Self-assembling sequence-adaptive peptide nucleic acids”. Science 325 (5936), 73–77. o. DOI:10.1126/science.1174577. PMID 19520909.
- ↑ (1994. április 1.) „DNA-like double helix formed by peptide nucleic acid”. Nature 368 (6471), 561–563. o. DOI:10.1038/368561a0. PMID 8139692.
- ↑ (2000. április 1.) „Peptide nucleic acids rather than RNA may have been the first genetic molecule”. Proceedings of the National Academy of Sciences of the United States of America 97 (8), 3868–3871. o. DOI:10.1073/pnas.97.8.3868. PMID 10760258.
- ↑ Molecular Biology of the Cell, 4th, Routledge (2002. március 1.). ISBN 978-0-8153-3218-3
- ↑ (2009. január 1.) „Evolutionary roots. On the origin of life on Earth”. Science 323 (5911), 198–9. o. DOI:10.1126/science.323.5911.198. PMID 19131603.
- ↑ (2014. április 26.) „Peptide nucleic acid - an opportunity for bio-nanotechnology”. CHIMIA 68 (4), 264–8. o. DOI:10.2533/chimia.2014.264. PMID 24983612.
- ↑ (2018. február 1.) „A novel mode for transcription inhibition mediated by PNA-induced R-loops with a model in vitro system”. Biochimica et Biophysica Acta (BBA) - Gene Regulatory Mechanisms 1861 (2), 158–166. o. DOI:10.1016/j.bbagrm.2017.12.008. PMID 29357316.
- ↑ (2013. október 1.) „Practical innovations for high-throughput amplicon sequencing”. Nature Methods 10 (10), 999–1002. o. DOI:10.1038/nmeth.2634. PMID 23995388.
- ↑ „Beletskii et al 2001”/ (2001) „PNA interference mapping demonstrates functional domains in the noncoding RNA Xist”. Proceedings of the National Academy of Sciences of the United States of America 98 (16), 9215–9220. o. DOI:10.1073/pnas.161173098. PMID 11481485.
Források[szerkesztés]
- Nielsen, Peter E. (2008. december 1.). „Triple Helix: Designing a New Molecule of Life”. Scientific American 299 (6), 64–71. o. DOI:10.1038/scientificamerican1208-64. PMID 19143446.
- Chapter 12. Metal Complex Derivatives of Peptide Nucleic Acids (PNA), Interplay between Metal Ions and Nucleic Acids, Metal Ions in Life Sciences. Springer, 319–40. o.. DOI: 10.1007/978-94-007-2172-2_12 (2012). ISBN 978-94-007-2171-5
- Next-generation sequencing and bioinformatics for plant science. Caister Academic Press. DOI: 10.21775/9781910190654 (2017. június 1.). ISBN 978-1-910190-66-1
- (2004. június 1.) „Recognition of chromosomal DNA by PNAs”. Chemistry & Biology 11 (6), 749–758. o. DOI:10.1016/j.chembiol.2003.09.014. PMID 15217608.
- (2005. január 1.) „Alternative nucleic acid analogues for programmable assembly: hybridization of LNA to PNA”. Nano Letters 5 (1), 107–11. o. DOI:10.1021/nl048246f. PMID 15792422.
- (2004) „The peptide nucleic acids (PNAs): a new generation of probes for genetic and cytogenetic analyses”. Annales de Génétique 47 (4), 349–58. o. DOI:10.1016/j.anngen.2004.07.001. PMID 15581832.
- Castelvecchi, Davide: A New Game of Life. Blog at WordPress.com, 2004. június 1. [2021. január 25-i dátummal az eredetiből archiválva]. (Hozzáférés: 2023. augusztus 28.)
- (1999) „An Introduction to Peptide Nucleic Acid”. Curr. Issues Mol. Biol. 1 (2), 89–104. o. [2011. szeptember 16-i dátummal az eredetiből archiválva]. PMID 11475704. (Hozzáférés: 2023. augusztus 28.)
