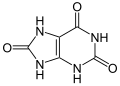
Húgysav
| Húgysav | |||
 |

| ||
| IUPAC-név | 7,9-dihidro-1H-purin-2,6,8(3H)-trion | ||
| Más nevek | 2,6,8-trioxipurin | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 69-93-2 | ||
| PubChem | 1175 | ||
| EINECS-szám | 200-720-7 | ||
| KEGG | C00366 | ||
| |||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C5H4N4O3 | ||
| Moláris tömeg | 168,11 g/mol | ||
| Megjelenés | fehér, kristályos | ||
| Sűrűség | 1,87 | ||
| Olvadáspont | hevítés hatására bomlik | ||
| Forráspont | (nincs) | ||
| Oldhatóság (vízben) | alig oldódik | ||
| Savasság (pKa) | 5,75; 10,3[1] | ||
| Veszélyek | |||
| EU osztályozás | nincsenek veszélyességi szimbólumok[2] | ||
| R mondatok | nincs[2] | ||
| S mondatok | nincs[2] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A húgysav heterociklusos vegyület. A purin 2,6,8-trihidroxiszármazékának tekinthető. Több tautomer alakja van. Sokkal nagyobb valószínűséggel található trilaktám alakban, mint a három hidroxilcsoportot tartalmazó trilaktim formában. Fehér színű, kristályos vegyület. Vízben alig oldódik, 100 gramm vízben 20 °C-on 0,0025 g, 100 °C-on 0,08 g oldódik fel. Oldhatatlan alkoholban és dietil-éterben. Olvadáspontja nincs, mert mielőtt megolvadna, elbomlik, elszenesedik. Kétértékű savként viselkedik. A sói az urátok. Savas jelleme miatt lúgokban feloldódik, de még a forró nátrium-karbonát oldat is feloldja. Oldódik forró, tömény kénsavban is. Kis mennyiségben megtalálható az emlősök és az ember vizeletében (normál érték: 120–420 μmol/l, nőkben kisebb, férfiakban nagyobb szinten) mint a purinanyagcsere végterméke. A hüllők és a madarak nagyobb mennyiségű húgysavat ürítenek, mert ezekben az állatokban a húgysav az aminosavak és a fehérjék anyagcseréjének a végterméke.
Története[szerkesztés]
A húgysav a legrégebben ismert purinvázas vegyület. A felfedezői Scheele és Bergman voltak, nekik sikerült először húgysavat kivonniuk hólyagkőből 1776-ban. A szerkezetét Medicus állapította meg 1875-ben, főként a húgysav oxidációjakor keletkező termékek szerkezete alapján. Húgysavat Horbaczewski szintetizált először 1882-ben, ugyanis ő fedezte fel, hogy a karbamid és a glicin keverékének hevítésekor képződő termék húgysavat is tartalmaz.
Tautoméria[szerkesztés]
A húgysav laktám-laktim tautomériát mutat, több tautomer alakja lehetséges. Létezik trilaktim és trilaktám alakja is. Vegyes, dilaktim alakban is létezhet. A legjellemzőbb alak a trilaktám forma, a húgysav legnagyobb valószínűséggel ebben az alakban van. A húgysav szerkezetét gyakran azért jellemzik a dilaktim alakkal, mert kétértékű savként viselkedik. Ez viszont nem indokolt, mert nemcsak oxigénatomhoz kapcsolódó hidrogénatom képes protonként lehasadni. Valójában a húgysav a 9-es helyzetű hidrogénatomját képes legkönnyebben protonként leadni (pKs: 5,75). Ennél sokkal kevésbé hajlamos disszociációra a 3-as helyzetben található hidrogénatom (pKs: 10,3).
-
A húgysav trilaktim alakja
-
A húgysav trilaktám alakja
Kémiai tulajdonságai[szerkesztés]
A húgysav kétértékű savként viselkedik. Oxidálószerekre érzékeny. Az oxidálószertől, illetve a körülményektől függően különböző termékek keletkezhetnek az oxidációjakor. Ha erélyes oxidációnak vetik alá savas kémhatású közegben (az oxidálószer például forró salétromsav vagy sósavas közegben kálium-klorát lehet), főként karbamiddá és alloxánná alakul, és az utóbbi tovább bomlik parabánsavvá. Ha viszont lúgos közegben kálium-permanganáttal oxidálják, akkor többek között allantoin képződik belőle. A húgysav szerkezetét is ezen lebontási termékek alapján sikerült először megállapítani.
A vegyület átalakítható 2,6,8-triklórpurinná, amely vegyületet gyakran röviden csak triklórpurinnak neveznek. A triklórpurin azért jelentős, mert klóratomjainak a reakciókészsége különböző, és emiatt más-más csoportokkal helyettesíthetők. Ha a húgysavat zárt térben foszfor-oxikloriddal (POCl3) hevítik, 2,6-diklór-8-hidroxi-purinná alakul. Ez csak fölöslegben lévő foszforoxiklorid hatására alakul tovább triklórpurinná. A húgysavból dimetilanilin jelenlétében foszforoxiklorid hatására egy lépésben is keletkezhet triklórpurin.
A murexid-próba[szerkesztés]
A murexid-próba a húgysav és a vele analóg purinvázas vegyületek régi kimutatási módja. Ha a húgysavhoz híg salétromsavat adnak, akkor többek között alloxantinná oxidálódik. A képződő oldatot bepárolják, és a leváló alloxantint alkoholos ammóniaoldattal reagáltatják. Ekkor az alloxantin az ammónia hatására a purpursav ammóniumsójává, murexiddé alakul. A bíborvörös színreakció ezen vegyület képződésével magyarázható.

Előállítása[szerkesztés]
A húgysavat legkorábban karbamid és glicin keverékének hevítésével sikerült előállítani. A reakcióban olyan termék képződött, ami kevés húgysavat is tartalmazott.
Előállítható izodialursav (vagy más néven dihidroxiuracil) és karbamid kondenzációs reakciójával is. A reakció kénsav jelenlétében megy végbe (ez volt egyben a húgysav első szerkezetbizonyító szintézise is). Húgysav képződik karbamidból és diaminouracilból is hevítés hatására.
Felhasználása[szerkesztés]
Egyes szerves vegyületek és gyógyszerek szintézisénél alkalmazzák.
Előfordulása, biológiai jelentősége[szerkesztés]
A húgysav megtalálható az ember és az emlősök vizeletében. Az ember húgysavürítése bizonyos betegségek, például köszvény esetén jelentősen megnőhet. Nagy mennyiségben tartalmaz húgysavat a hüllők és a madarak ürüléke. A kígyók ürüléke akár 90%-ban is tartalmazhatja a húgysav ammóniumsóját, az ammónium-urátot. A perui guanóban körülbelül 20% húgysav található.
A húgysav a purinok anyagcseréjének a végterméke. A hüllők és madarak az aminosavak és más nitrogéntartalmú vegyületek nitrogénjét is húgysav alakjában ürítik, az ilyen szervezeteket urikotél szervezeteknek nevezik. Ezekben az állatokban az aminosavak és a fehérjék anyagcseréjének végterméke is a húgysav.
Szerepe a purinbázisok lebontásában[szerkesztés]
Az emlősökben a purinbázisok nitrogéntartalmának nagy része húgysav és allantoin alakjában ürül, a purinváz tehát nem bomlik le teljesen.
Az adeninből és a guaninból (illetve az ezekből felépülő nukleozidokból és nukleotidokból (adenozin, guanozin, adenilsav, guanilsav)) először enzimek (például adenilát-dezamináz, guanilát-dezamináz) hatására lehasad az aminocsoport, az adeninből hipoxantin, a guaninból xantin keletkezik. A hipoxantin és a xantin továbbalakulását a xantin-oxidáz enzim segíti elő.
- xantin + O2 + H2O → húgysav + H2O2
Az emlősök nagy részének májában található húgysavat oxidáló enzim, aminek a neve urát-oxidáz vagy urikáz. Ez az enzim a húgysavat allantoinná oxidálja.
- húgysav + H2O + O2 → allantoin + CO2 + H2O2
Az urát-oxidáz enzim nem található meg az ember, a főemlősök, illetve a hüllők és a madarak egy részének májában, ezeknél az állatoknál a nukleotidok anyagcseréjének végterméke a húgysav. A halakban az allantoin tovább hidrolizálhat karbamidra és glioxilsavra.
A húgysav túltermelődése, betegségek[szerkesztés]
Egy normál ember naponta 150–250 mg húgysavat ürít ki. A húgysav egy része a porcokban rakódik le. Ha mennyisége a normálisnál nagyobb, köszvény alakulhat ki. Köszvény az esetek nagy többségében (95%) férfiaknál alakul ki. A húgysav rosszul oldódik vízben, emiatt a vesében kikristályosodhat. Ekkor urátvesekő alakul ki, ami károsíthatja a vesét.
A húgysav túltermelődését gyakran veleszületett anyagcserezavar okozza. A túltermelődést az allopurinol csökkenti. Az allopurinol a hipoxantin szerkezeti analógja, gátolja a xantin-oxidáz enzim működését. Az allopurinol megszünteti az urátköveket, csökkenti a köszvény tüneteit. Csökkenti a purinbázisok bioszintézisét is.
Jegyzetek[szerkesztés]
- ↑ Gergely Pál, Penke Botond, Tóth Gyula. Szerves és bioorganikus kémia. Budapest: Semmelweis Kiadó, 174. o. (1994). ISBN 963-815-44-2X
- ↑ a b c Biztonsági adatlap (Carl Roth) (németül)
Források[szerkesztés]
- Bruckner Győző: Szerves kémia, III/1-es kötet
- Kovács Kálmán, Halmos Miklós: A szerves kémia alapjai
- Bot György: A szerves kémia alapjai
- Erdey-Grúz Tibor: Vegyszerismeret
- Elődi Pál: Biokémia