Glicin
| Glicin | |||
| |||
 |

| ||
| IUPAC-név | 2-aminoecetsav | ||
| Szabályos név | 2-aminoetánsav | ||
| Más nevek | glicin | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 56-40-6 | ||
| PubChem | 750 | ||
| ATC kód | B05CX03 | ||
| Gyógyszer szabadnév | Glycine | ||
| Gyógyszerkönyvi név | Glycinum | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C2H5NO2 | ||
| Moláris tömeg | 75,07 g/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
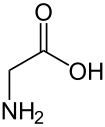
A glicin (INN: glycine) (Gly vagy G)[1] egy fehérjealkotó aminosav. (HO2CCH2NH2) Glikokoll néven is ismert.[2] Kodonjai: GGU, GGC, GGA és GGG. A glicin az egyetlen olyan aminosav, amely optikailag nem aktív. A legtöbb fehérjében csak kis mennyiségben fordul elő, kivéve a kollagént, melynek kb 35%-a glicin.[3] A selyemfibroin is nagy mennyiségben tartalmazza. Színtelen, édes ízű, kristályos anyag, 233 °C-on bomlik. Vízben jól, alkoholban, éterben nem oldódik.[4]
Neve az "édes" szó görög megfelelőjéből származik.
Szintézis[szerkesztés]
A glicint iparilag klórecetsavból állítják elő ammónia hozzáadásával.
- ClCH2COOH + NH3 → H2NCH2COOH + HCl
Élettani szerepe[szerkesztés]
Intermedier[szerkesztés]
A glicin számos biomolekula alkotórésze. Az eukariótákban a δ-aminolevulinsav, amely a porfirinek fő prekurzora, glicinből és szukcinil-koenzim-A-ból képződik. A glicin alkotja a purinok központi C2N egységét.[5]
Neurotranszmitter[szerkesztés]
A glicin egy gátló neurotranszmitter a központi idegrendszerben, különösen a gerincvelőben, az agytörzsben és a retinában. Amikor a glicinreceptorok aktiválódnak, kloridionok lépnek be a sejtbe az ionotróp receptorokon keresztül és a sejtben gátló posztszinaptikus potenciált (IPSP) váltanak ki.
A sztrichnin az ionotróp glicinreceptorokon antagonista hatású. A glicin szükséges az NMDA receptorokon, mint a glutamát ko-agonistája.
Élelmiszeripari felhasználása[szerkesztés]
Élelmiszerek esetén a glicint és nátriumsóját (nátrium-glicinát) pékáruk esetén ízfokozóként alkalmazzák, valamint egyúttal táplálékot szolgáltat az élesztőbaktériumoknak is. Napi maximum beviteli mennyisége nincs meghatározva, nincs ismert mellékhatása. Élelmiszeripari felhasználásra általában zselatinból állítják elő.
Fényképészeti felhasználása[szerkesztés]
Ritkán használt előhívó hatóanyag. Negatív anyagoknál rendkívül finom szemcsét ad, viszont hosszú előhívási időt, a negatív tekintetében 2-3-szoros túlexpozíciót igényel. Pozitív kidolgozásban a régebben használatos ezüstklorid és klórbróm emulziók esetén gazdag színárnyalatokat lehetett vele elérni.[6]
Jegyzetek[szerkesztés]
- ↑ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature: Nomenclature and Symbolism for Amino Acids and Peptides. Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. (Hozzáférés: 2007. május 17.)
- ↑ http://www.vilaglex.hu/Lexikon/Html/Glicin_.htm
- ↑ Nelson, D. L. & Cox, M. M. (2005). Lehninger Principles of Biochemistry, 4th Edition. New York: W. H. Freeman and Company, p. 127. ISBN 0-7167-4339-6.
- ↑ http://szerves.chem.elte.hu/oktatas/ea/aminosav-ap6.pdf
- ↑ Nelson, D. L. & Cox, M. M. (2005). Lehninger Principles of Biochemistry, 4th Edition. New York: W. H. Freeman and Company, p. 854. ISBN 0-7167-4339-6.
- ↑ Dr. Lentz Nándor–Kindl Ervin: Fotovegyszer lexikon, Fotosorozat 13–14., 2., bővített kiadás, Műszaki, 1960
Források[szerkesztés]
- Dawson, R.M.C., Elliott, D.C., Elliott, W.H., and Jones, K.M., Data for Biochemical Research (3rd edition), pp. 1–31 (1986) ISBN 0-19-855358-7
