Hisztidin
| Hisztidin | |||
| |||
| |||
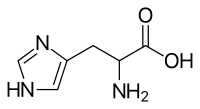
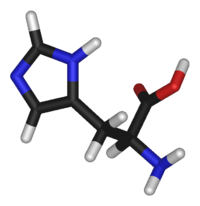
| IUPAC-név | 2-amino-3-(1H-imidazol-4-il)propánsav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 71-00-1 | ||
| PubChem | 773 | ||
| ChemSpider | 752 | ||
| Gyógyszer szabadnév | histidine | ||
| Gyógyszerkönyvi név | Histidinum, Histidini hydrochloridum monohydricum | ||
| |||
| |||
| InChIKey | HNDVDQJCIGZPNO-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C6H9N3O2 | ||
| Moláris tömeg | 155,15 g/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A hisztidin (His vagy H)[1] egyike a 22 fehérjealkotó aminosavnak. Táplálkozási szempontból emberekben a hisztidin esszenciális, különösen gyerekekben. Kodonjai a CAU és a CAC.
A hisztidint elsőként 1896-ban izolálta Albrecht Kossel német orvos.
A hisztidin elnevezés a görög hisztosz (ιστός = szövet) szóból származik.[2]
Kémia[szerkesztés]
Az imidazol oldallánc és a hisztidin viszonylag semleges pKa értéke (kb. 6,0) eredményeképpen a sejt pH-jának kis változása is megváltoztatja a molekula töltését.
Az imidazol oldalláncon két eltérő tulajdonságú nitrogénatom található : az egyikhez hidrogén kötődik, és átadja szabad elektronpárját az aromás gyűrűnek, és emiatt enyhén savas, míg a másik csak egy elektronpárt ad a gyűrűnek, ezért bázikus tulajdonságú.
Anyagcsere[szerkesztés]
A hisztidin a hisztamin és a karnozin bioszintézisének prekurzora.

A hisztidin ammónia-liáz enzim a hisztidint ammóniává és urokainsavvá alakítja. Ennek az enzimnek a hiánya figyelhető meg a histidinemia nevű ritka betegségben.
Előfordulása táplálékokban[szerkesztés]
Az érlelés, fermentálás elősegíti azon mikroorganizmusok szaporodását, melyek anyagcseréjük révén hisztamint állítanak elő.
Mivel a szervezet nem képes közvetlenül hisztamin előállítására, az alábbi élelmiszerek fogyasztása javallott:
- Érlelt sajtok, kolbászok, szalámik, sonka,
- fermentált zöldségek (például savanyú káposzta), fermentált szója.
- erjesztett alkoholok: bor, sör (ale, lager)
- csonthéjas és bogyós gyümölcsök
- trópusi gyümölcsök: citrusfélék, datolyafélék, ananász
- zöldségek: paradicsom, padlizsán, szójabab, spenót, sütőtök, vörösbab, olíva
Jegyzetek[szerkesztés]
- ↑ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature: Nomenclature and Symbolism for Amino Acids and Peptides. Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. (Hozzáférés: 2007. május 17.)
- ↑ Fülöp József: Rövid kémiai értelmező és etimológiai szótár. Celldömölk: Pauz–Westermann Könyvkiadó Kft. 1998. 64. o. ISBN 963 8334 96 7
