Pirogallol
| Pirogallol | |||
 Pirogallol | |||
| |||
| Más nevek | 1,2,3-trihidroxibenzol, vic-trihidroxibenzol, pirogalluszsav | ||
| Kémiai azonosítók | |||
| CAS-szám | 87-66-1 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C6H6O3 | ||
| Moláris tömeg | 126,11 g/mol | ||
| Megjelenés | Fehér színű, kristályos | ||
| Sűrűség | 1,45 g/cm³ (20 °C)[1] | ||
| Olvadáspont | 131-135 °C[1] | ||
| Forráspont | 309 °C[1] | ||
| Oldhatóság (vízben) | 400 g/l, 20 °C[1] | ||
| Gőznyomás | 2-4 hPa[1] | ||
| Veszélyek | |||
| EU osztályozás | Ártalmas (Xn)[2] | ||
| R mondatok | R20/21/22, R68, R52/53[2] | ||
| S mondatok | (S2), S36/37, S61[2] | ||
| LD50 | 790 mg/kg (patkány, szájon át)[3] | ||
| Rokon vegyületek | |||
| Rokon háromértékű fenolok | Hidroxihidrokinon Floroglucin | ||
| Rokon vegyületek | Galluszsav | ||
| Az infoboxban SI-mértékegységek szerepelnek. Ahol lehetséges, az adatok standardállapotra (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. Az ezektől való eltérést egyértelműen jelezzük. | |||
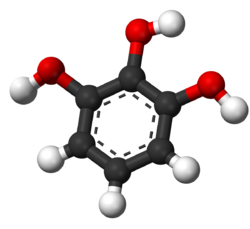
A pirogallol egy szerves vegyület, egy háromértékű fenol. Benzolgyűrűt tartalmaz, a benzolgyűrűjéhez három hidroxilcsoport kapcsolódik vicinális, szomszédos helyzetben (1,2,3-helyzet). Kristályos vegyület. Fehér színű csillogó lemezekből vagy tűkből áll. A két izomerje a hidroxihidrokinon és a floroglucin. Vízben jól, alkoholban és dietil-éterben kevésbé oldódik. Ha hevítik, szublimál.
Kémiai tulajdonságai[szerkesztés]
A pirogallol erős redukálószer, könnyen oxidálódik. Ha a vizes oldatához néhány csepp vas(II)- vagy vas(III)-sóoldatot adnak, kék színreakciót mutat. A kék szín állás közben lassan barnára változik. Vas(III)-ionok hatására purpurogallinná oxidálódik.
Redukálja a higany, az ezüst és az arany sóinak oldatát, ezekből fémet választ ki. Ekkor a vegyület aromás jellege megszűnik, a vegyület oxálsavvá és ecetsavvá alakul, oxidálódik.
A vegyület lúgos oldata nagyon könnyen elnyeli (abszorbeálja) az oxigént. A gyűrűje felbomlik, ecetsavvá és szén-dioxiddá (ez általában karbonáttá alakul) oxidálódik. Ez a reakció a gyűrű teljes felnyílásával jár. A színe feketésbarnává válik.
Előfordulása[szerkesztés]
A vegyület származéka, dimetil-étere megtalálható a bükkfakátrányban.
Előállítása[szerkesztés]
A pirogallol a legrégebben ismert többértékű fenol. Scheele állította elő először galluszsav hevítésével 1786-ban, a vegyület neve is innen ered. Ez egy dekarboxilezési reakció, a galluszsav karboxilcsoportja szén-dioxid formájában távozik.
A pirogallolt lényegében ma is a galluszsav dekarboxilezésével gyártják. Ma már azonban nem száraz hevítést alkalmaznak, hanem háromszoros mennyiségű víz jelenlétében, nyomás alatt melegítik a galluszsavat 210 °C-ra.
Felhasználása[szerkesztés]
A pirogallolt a fényképészetben előhívásra használják. Köztes termék gyógyszerek és aromaanyagok előállításánál. Emellett növényvédőszerek és festékek előállítására is használják. Emellett elektromos alkatrészek gyártására is szolgál.[1]
A pirogallol lúgos oldatát az analitikai kémiában az oxigéngáz kimutatására használják, mert az oxigénnel nagyon gyorsan reakcióba lép.
Források[szerkesztés]
- Bruckner Győző: Szerves kémia, II/1-es kötet
- Erdey-Grúz Tibor: Vegyszerismeret
Jegyzetek[szerkesztés]
- ↑ a b c d e f A pirogallol vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2011. január 21. (JavaScript szükséges) (angolul)
- ↑ a b c A pirogallol (ESIS)
- ↑ Biztonsági adatlap (Merck) (németül)
