Méhnyakrák
| Méhnyakrák | |
 | |
| Ez a nagy laphámsejtes rák (a kép alján) elzárta a nyakcsatornát és ráterjedt a méh alsó részére. A méh üregét csaknem kitölti egy nagy, kerek simaizom eredetű daganat (leiomyoma) (az előbbitől feljebb) | |
| Latinul | Cervix carcinoma |
| Angolul | Cervical cancer |
| Osztályozás | |
| BNO-10 | C5380 |
| Epidemiológia | |
| Incidencia | |
| Magyarországon | 1000–1500 fő/év |
| Világszerte | 473 000 fő/év (2008) |
| Halálozási arány | |
| Magyarországon | 500/ fő/év |
| Világszerte | 253 500 fő/év (2008) |
| Leírás | |
| Érintett szervek | a méhnyak és a nyakcsatorna hámja, később közeli és távolabbi szervek |
| Etiológia | HPV vírus (elsősorban a 16-os és 18-as típusok) |
| Kockázati tényezők | szexuális partnerek gyakori váltása stb. |
| Főbb tünetek | vérzés, fájdalom, később fogyás stb. |
| Diagnosztika | nőgyógyászati vizsgálat a szükséges kiegészítésekkel |
| Szövődmények | környező szervekben beszűrődés, majd távoli áttétek, térszűkítés, befertőződés |
| Kezelés | korai stádiumban a nyakcsatorna körüli szövet kúp alakú kimetszése (konizáció) későbbiekben általános daganatellenes terápia |
| Kórjóslat | korai stádiumban nagyon jó |
| Megelőzés | védőoltás, szűrővizsgálat, HPV fertőzés kerülése |
| Adatbázisok | |
| OMIM | 603956 |
| DiseasesDB | 2278 |
| MedlinePlus | 000893 |
| MeSH ID | D002583 |
A Wikimédia Commons tartalmaz Méhnyakrák témájú médiaállományokat. | |


A méhnyakrák[1][2] a méh alsó, elkeskenyedő részén, a méhnyakon kialakuló rosszindulatú daganatos betegség, mely során a méhnyak hámjában abnormális sejtek fejlődnek, amelyek késői szakaszban a test más részeibe is továbbterjedhetnek. Kezdetben, évekig általában tünetmentes, a későbbi tünetek a hüvelyi vérzés, medencei fájdalom vagy szexuális aktus közbeni fájdalom.[3] A méhnyakrák több mint 90%-ban humán papillomavírus (HPV) fertőzés hatására fejlődik ki.[4][5][6] Ugyanakkor a HPV-fertőzések alapjában igen gyakori, magától megszűnő fertőzések, és csak kis százalékukban fejlődik ki méhnyakrák.[7][8] A rákot okozó vírus emberről emberre alapvetően nemi úton terjed, azonban nem a testnedvek cseréjével fertőz, hanem bőrkontaktussal, így az óvszer nem jelent teljes védelmet a vírus ellen, csak jelentős mértékben, 60–70 százalékkal csökkenti a fertőzés veszélyét. Az aktív nemi életet folytató nők mintegy 80%-a valamelyik életszakaszában megfertőződik a vírus valamelyik típusával. A fertőzések legnagyobb része tünetek nélkül, magától elmúlik. Néhány emberben viszont a vírusok fennmaradnak, és egy részükben szemölcsöt illetve rákmegelőző állapotot jelentő hámfelmaródást (léziót) okoznak.[9] A kóros sejtek elszaporodása lassan, évek alatt jut a méhnyakrák állapotig. A beteg által is észlelhető tünetek általában csak előrehaladott állapotban jelentkeznek, amikor a teljes gyógyulást eredményező beavatkozásokra már nincs lehetőség.[10] Ebben az esetben – az orvosi kezelés ellenére – a beteg életminőségének lényeges romlásához, élettartamának megrövidüléséhez vezet. A rendszeres szűrővizsgálatok azonban lehetővé teszik a korai – még rákmegelőző – állapotok felismerését és lényegében teljes gyógyítását.[11] Emellett ma már hatékony vírusellenes védőoltások is rendelkezésre állnak.[12] A méhnyakrák megelőzéséhez a tünetmentes nőknek is fontos a rendszeres szakorvosi ellenőrzés és szűrővizsgálaton való részvétel.
Kivizsgálása[szerkesztés]
Diagnosztika[szerkesztés]
A kórisme megállapításának alapvető módja a nőgyógyászati vizsgálat, amihez a beteg panaszainak meghallgatása, a méhnyak kolposzkópos megfigyelése és a sejttani vizsgálat (a kinyert sejtek kenetének Papanicolaou szerinti festése után)[13] is hozzátartozik. Az orvos szükség szerint ezt kiegészíti virológiai vizsgálattal, a kimetszett szövet kórszövettani vizsgálatával, cisztoszkópiával (húgyhólyagtükrözés), rektoszkópiával (végbéltükrözés), radiológiai vagy modernebb képalkotási eljárásokat – komputertomográfiát (CT) vagy mágneses magrezonancia képalkotást (MRI)[14] – használó vizsgálati módszerekkel.
Panaszok és tünetek[szerkesztés]
Hosszú évek alatt, igen lassan fejlődik ki, panaszokat nagyon sokáig nem okoz.[15] Amikor már panaszok/tünetek jelentkeznek, a kórfolyamat már olyan előrehaladott, hogy tényleges gyógyítása nem lehetséges. Csak a szűrővizsgálatokkal elérhető korai kórisme, (diagnózis) vezethet eredményre.
A méhnyakrák hosszú idő alatt fejlődik ki, ez az időszak akár 10–20 év is lehet. Tünetei[15] csak későn jelentkeznek, a betegséget sokszor csak szűrővizsgálatok során fedezik fel.
Tünetei, kimenetele:
- Rendszertelen kisebb vérzések. A kiürülő vér élénk piros. A vérzést sokszor szexuális aktus provokálja.
- Gyakran jelentkező hüvelyi folyás. A váladék rossz szagú, sárgás színű, vagy enyhén véres.
- Egyes esetekben – daganat okozta elzáródás – erős alhasi fájdalmak, esetleg méhűri fertőzés, amely a keringési rendszeren keresztül általános fertőzést okozhat.
- A folyamat előrehaladásával mind gyakrabban jelentkező deréktáji fájdalmak. Fájdalmas a székelés, a vizelés és a szexuális aktus. Székrekedés, szorulás is jelentkezhet.
- A növekvő daganat a húgyvezeték (uréter) összenyomásával vizeletpangást okozhat a vesemedencében. A húgyhólyagba vagy a végbélbe áttörő tumor sipolyok kialakulásához vezethet.
- Elhanyagolt esetek vérzés vagy általános fertőzés (szepszis) miatt a beteg halálát okozzák.
- A többi rosszindulató daganathoz hasonlóan a méhnyakrákos esetekre is jellemző a fogyás, a látványos testsúlycsökkenés.
- Előrehaladott méhnyakráknál gyakori jelenség a medence bármelyik részében tapasztalható fájdalom, valamint a végtagfájdalom, a lábfájás is. Ez azért alakul ki, mert ahogy a rákos daganat egyre nagyobbra növekszik és terjed, már nyomja az idegeket.
A szűrés fontossága eléggé nem hangsúlyozható, mivel az időben történő diagnózis életmentő. Az előbb ismertetett tünetek jelentkezésekor a tényleges gyógyuláshoz vezető beavatkozás már elkésett.
Leletek[szerkesztés]
Rákmegelőző károsodások és kimutatásuk[szerkesztés]
A diszplázia vagy in situ carcinoma (CIS). A cevicalis intraepithéliális neoplázia (CIN) elnevezést helyezték előtérbe annak hangsúlyozására, hogy milyen változatos a megjelenése ezeknek az eltéréseknek, valamint, hogy elősegítsék a standardizált kezelést.[16] Enyhe diszpláziát (CIN1), mérsékelt diszpláziát (CIN2) és súlyos diszpláziát[16] (CIN2) különböztettek meg. Újabban a CIN2 és CIN3 kombinálásával kialakították a CIN2/3 stádiumot. Ezek azok az állapotok, amelyeket a patológusok megállapíthatnak egy biopsziás anyag vizsgálatának eredményeként. Míg a Papanicolaou módszerével festett kenetek vizsgálat már egy hatékony szűrési teszt, a méhnyakrák vagy a méhnyakrákot megelőző állapot diagnózisának megerősítéséhez anyagkimetszésre (biopszia) van szükség a méhnyakból. Ez leginkább kolposzkópos ellenőrzés mellett történik, ami lehetővé teszi a beavatkozási terület nagyított kolposzkópos képének megfigyelését, emellett a méhnyakat hígított ecetsavval ecsetelik be, aminek hatására jobban kirajzolódik az abnormális sejtekkel borított terület a méhnyakon.[5] A kolposzkópos megfigyelés része az elváltozás súlyossági foka megítélésének és a diagnózis megállapításának. A további diagnosztikai és kezelési eljárásokhoz tartozik az elektromosan fűtött huzalkaccsal történő kimetszés és a konizáció, amely során a nyakcsatorna hámját kimetszik, majd kórszövettanilag vizsgálják. Ezekre akkor kerül sor, ha a hámból kinyert sejtek súlyos hámon belüli (intraepitéliális) rosszindulatú elváltozásokat igazolnak.


A méhnyakrákot megelőző állapotok szövettani besorolása és besorolásának nevezékrendszere sokszor változott a 20. században. Az Egészségügyi Világszervezet[17] besorolása[16] leíró volt, azokat enyhe, közepes és súlyos fokozatokba sorolta.

Kórszövettani altípusai[szerkesztés]
- Laphámsejtes rák (≈ 80–85%)
- Mirigyszövet eredetű rák (≈ 15%)
- Kevert típus (az előző kettő kombinációja)
- Kis sejtes rák
Az egyéb rosszindulatú daganatok közül ritkán előfordulhat:
- Festékes daganat (melanoma)
- Nyiroksejtes daganat (lymphoma)
Stádiumai[szerkesztés]
A méhnyakrák súlyossági fokozat (stádium) szerinti osztályozása a FIGO[20] (Nemzetközi Nőgyógyászati és Szülészeti Szövetség) rendszerében lényegében megfelel a TNM[21] (A rosszindulatú (malignus) daganatok (tumorok) stádiumai) rendszernek, ahol:
- T – A tumor nagyságára és a közeli szövetekbe való behatolására (beszűrődés) vonatkozó jellemzők
- N – A tájéki (regionális) nyirokcsomók érintettsége
- M – Távoli áttétek (metastasis) jelenléte
- 0. stádium – A hám teljes vastagságában érintett, de nincs beszűrődés a szomszédos szövetekben (in situ carcinoma)
- I. stádium – A méhnyakra (cervix) korlátozódik
- IA. stádium – Csak mikroszkóposan diagnosztizálható; szabad szemmel látható elváltozás nincs
- IA1. stádium – Környezetbe beszüremlés (invázió) van, de mélységében kisebb, mint 3 mm, és haránt kiterjedése kisebb, mint 3 mm
- IA2. stádium – A környezetbe beszüremlés kiterjedése 3 és 5 mm között; haránt kiterjedése 7 mm, vagy kisebb
- IB. stádium. Szabad szemmel látható elváltozás, vagy olyan mikroszkópos elváltozás, amely mélyebb, mint 5 mm, vagy haránt kiterjedéses nagyobb, mint 7 mm
- IB1. stádium – Szabad szemmel látható elváltozás, amelynek legnagyobb átmérője 4 cm, vagy annál kisebb
- IB2. stádium – Szabad szemmel látható, 4 cm-nél nagyobb elváltozás
- IA. stádium – Csak mikroszkóposan diagnosztizálható; szabad szemmel látható elváltozás nincs
- II. stádium – A méhnyak körüli részbe szüremlik be
- IIA. stádium – A méhtől kétoldalt, a széles méhszalagban található kötőszövetes térbe (parametriumba) nem szüremkedik be, de már kiterjed a hüvely felső kétharmadára
- IIB. stádium – Beszüremkedik a parametriumba
- III. stádium – Ráterjed a kismedence falára vagy a hüvely alsó harmadára
- IIIA. stádium – A hüvely alsó harmadát is beszűri (infiltrálja)
- IIIB. stádium – Ráterjed a kismedence falára és/vagy vesemedencei pangást (hydronphrosis) okoz, és a vesefunkció kiesik
- IV. stádium – A hüvelyen kívülre terjed
- IVA. Stádium – Ráterjed a húgyhólyag/végbél nyálkahártyájára és/vagy túlterjed a tényleges kismedencén
- IV.B. stádium – Távoli daganatáttéteket (metastasis) képez
Kórokozója a humán papillomavírus (HPV)[szerkesztés]
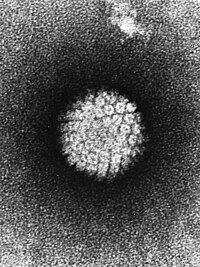
A méhnyakrák megbetegedések több mint 90%-a humán papillomavírus (HPV) fertőzés hatására fejlődik ki.[4][5][6] Ugyanakkor a HPV-fertőzéseknek csak kis százalékában fejlődik ki méhnyakrák. A vírus több mint 150 (mások szerint több mint 200) variánsának többsége nem rákkeltő. Vannak azonban rákot okozó variánsai is.[22] Ezek közül a HPV 16-os és 18-as változatok együtt a méhnyakrákok több mint 71%-át, a 45-ös és 31-es változatokat is hozzászámítva több mint 81%-át okozzák. A kórfolyamat létrejöttét bizonyos kockázati tényezők megléte előmozdítja. (A vírus a férfiakat is megfertőzi, de betegséget nem okoz. Viszont a fertőzött férfiakról a kórokozó ráterjedhet női szexuális partnerükre/partnereikre.[4]) A fertőzés a partnerek között oda-vissza terjedhet („ping-pong”-fertőzés). (A vírust elektronmikroszkóposan már 1949-ben megfigyelték, DNS-ét 1963-ban azonosították. Csak 1983-ban mutatta ki Harald zur Hausen német tudós méhnyakrákos szövetben (ezért a munkájáért 2008-ban Orvosi-fiziológiai Nobel-díjat kapott). Ezután fejlesztették ki a vírusfertőzés elleni védelmet szolgáló oltóanyagokat (vakcina).[12] A vírus nem csak méhnyakrákot, de szájüregi rákokat, végbélrákot és bőrelváltozásokat (szemölcsök) is okozhat.[23][24]
A humán papillomavírus (HPV) terjedése[szerkesztés]
A vírus[25] emberről emberre alapvetően nemi úton terjed. Ehhez nem feltétlenül szükséges a tényleges szexuális aktus, hanem az aktus nélküli intim együttlét során, az egyéb módon történő testi érintkezés is elegendő lehet. Ebből következik, hogy az aktív nemi életet folytató nők mintegy 80%-a valamelyik életszakaszában megfertőződik a vírus valamelyik típusával. Emiatt a gumióvszer használata sem jelent teljes védelmet, bár van kockázatcsökkentő hatása. Egy közlés szerint az ondóban lévő prosztaglandin elősegíti a méhdaganatok kifejlődését, ezért a kondom használata bizonyos védelmet nyújthat a nőknek.[26][27] A fertőzést követően a folyamat további lefolyása már nagy mértékben a fertőzést okozó vírus típusától és az egyén immunrendszerének állapotától függ. Az immunológiai védekezésnek köszönhető, hogy a vírus – az esetek többségében – bizonyos idő után eltűnik a szervezetből. (Nemi betegségeknél fordul elő, hogy a nemi partner kezelésének elmaradásakor a kezelt beteget visszafertőzheti kezeletlen partnere, ez a ping-pong fertőzés. Az ilyen betegségek fennállása esetén javasolt mind a férfit, mind a nőt kezelni a fenti fertőzési mechanizmus elkerüléséhez.)
Módosító tényezők[szerkesztés]
Kockázati tényezők[szerkesztés]
Ezek a következők:[28]
- A HPV rákkeltő variánsának tartós jelenléte a szervezetben (legalább 6–12 hónapon keresztül)
- Genetikai tényezők (a jelenlegi álláspont szerint nagyon kis mértékben)
- Dohányzás[29][30]
- Az immunrendszer csökkent működése
- Szájon át szedett fogamzásgátlók folyamatos, tartós – öt évet meghaladó – használata
- Többszöri terhesség
- Korán kezdett aktív szexuális élet[31]
- A testhigiénia elhanyagolása
- Nemi élettel terjedő betegségek[32]
- A férfi szexuális partner(ek) HPV-fertőzöttsége
- A szexuális partnerek gyakori váltogatása
Az Amerikai Rákellenes Társaság[33] a méhnyakrák kockázati tényezőinek az alábbi listáját adja meg: (HPV) fertőzés, dohányzás, HIV-vírus fertőzés, chlamydiafertőzés, stressz és stresszel kapcsolatos rendellenességek, hormonális fogamzásgátlás, ismételt terhesség, hormonkészítmény szedése, dietilsztilbösztrol és méhnyakrákos családi előzmények. A fiatal korban kezdett szexuális élet és első terhesség szintén a kockázati tényezőkhöz tartozik, aminek kockázati hatását fokozza a korán megkezdett szájon át szedhető fogamzásgátlók használata.[31] A korán kezdett szexuális élet és a korai terhesség főleg a fejlődő országokban fokozza a méhnyakrák kockázatát.[31] Lehetséges genetika kockázat kapcsolódik a HLA-B7-hez.[34] Semmiféle határozott bizonyíték nem támasztja alá azt a feltételezést, hogy a férfi partner körülmetélése csökkentené a méhnyakrák kockázatát, bár néhány kutató szerint epidemiológiailag nyilvánvaló, hogy a körülmetélésen átesett férfiak kevésbé hajlamosak a HPV-fertőzésre. Ugyanakkor az alacsony kockázattal járó szexuális viselkedésű férfiaknál, akik női partnerükkel monogám szexuális életet élnek, a körülmetélés nem okoz eltérést a méhnyakrák kockázatban.[35] A dohányfüstből származó karcinogén anyagok számos ráktípus, közöttük a méhnyakrák kockázatát is növelik. A dohányzó nők mintegy kétszeres valószínűséggel betegszenek meg méhnyakrákban, a nemdohányzókhoz viszonyítva.[29]
A WEBBeteg.hu figyelmeztetése a következő: "Ez a ráktípus gyakrabban fordul elő azokban a nőkben, akik fiatal korban kezdték a nemi életet, akik gyakran váltogatják partnerüket, vagy többször szültek. Azonban sokáig nem okoz panaszt, ezért fontos hangsúlyozni a nőgyógyászati rákszűrés fontosságát a korai felismerésben."[36]
Védő hatású tényezők[szerkesztés]
Táplálkozás[szerkesztés]
- Gyümölcsök és zöldségek
A magas gyümölcs- és zöldségfogyasztás 54%-kal csökkentette a HPV jelenlét tartósságát.[37]
- A-vitamin
Vannak arra utaló – nem túl meggyőző – adatok, hogy a retinol nagyfokú hiánya hajlamosít a méhnyakhám diszpláziájára a HPV-vírus fertőzés hiányában is. Egy kis létszámú (500 fő körüli) csoporton végzett vizsgálatban, amelyet egy szűk etnikai csoporton végeztek (nevezetesen Új-Mexikóban élő amerikai őslakosokon), meghatározták a vérszérumban lévő mikrotápanyagok szintjét abban az összefüggésben, hogy kockázati tényezőkként szerepelhetnek-e a méhnyakhám diszpláziákban. A szérum retinol szint szerinti eloszlás alsó kvartilisában növekedett volt a hámon belüli (cervicalis intraepitéliális) neoplázia (CIN) kockázata, mint a felső kvartilisekbe tartozó nőknél.[38]
Ugyanakkor az egész populációnál kimutatható volt a normálisnál alacsonyabb szérum retinol szint, ami hiányra utalt. A szérum retinol szint vizsgálata egy jól táplált populációnál kiderítette, hogy az alsó 20% retinol szintje állt közel az újmexikói csoportnál mért legmagasabb szérum retinol szintjéhez.[38]
- C-vitamin
A típus-specifikus, tartós HPV-fertőzés alacsonyabb volt azoknál a nőknél akik a C-vitamin fogyasztás mennyiségét tekintve az eloszlás felső kvartilisába tartoztak, azokhoz képest, akik ennek az eloszlásnak az alsó kvartilisába tartoztak.[39][40]
- E-vitamin
A HPV jelenlétének megszűnéséhez szükséges időtartam szignifikánsan rövidebb volt a legmagasabb szérum tokoferol szintet mutató nőknél, azokkal összehasonlítva, akiknél a legalacsonyabb volt ez az érték. Az ezzel kapcsolatos szignifikáns trendek azonban csak a 120 napnál rövidebb tartós fertőzöttségek (≤120 nap) esetében jelentkeztek. A 120 napnál hosszabb (>120 nap) fertőzöttségek esetében a vírusmentessé válás nem mutatott szignifikáns összefüggést a vérben keringő tokoferol szintjével. Ezeknek a vizsgálatoknak az eredményei alátámasztották azt, hogy összefüggés van a mikrotápanyagok és a véletlen fertőzéssel a méhnyakba bekerült rákkeltő HPV-vírusok kiürülése/eliminálása között.[41] Statisztikailag alacsonyabb alfa-tokoferol szintet figyeltek meg a HPV pozitív[41] méhnyaki intraepitéliális neopláziát mutató nők esetében. A diszplázia kockázata négyszer nagyobb volt, ha a tokoferol szintje 7,95 mumol/l-nél alacsonyabb volt.[42]
Napi 5 mg folsav az ötödrészére csökkenti a méhnyakhám diszpláziájának előfordulását.[43]
- Karotinoidok
Egy onkogén HPV vírus fertőzés felderítésének valószínűsége szignifikánsan magasabb megnövekedett glikopén szint esetén.[44] A HPV tartós jelenlétének kockázata 56%-kal volt alacsonyabb azoknál a nőknél, akiknél a plazma likopén szintje a legmagasabb volt, szemben a legalacsonyabb likopén plazmakoncentrációval bíró csoporttal. Ezek az adatok arra utalnak, hogy a zöldségfogyasztás és a keringő likopén védő hatású lehet a HPV tartós jelenlétével szemben.[37][39][40]
Életkor[szerkesztés]
Világviszonylatban a 15–45 év közötti nők körében a méhnyakrák a második helyen áll, előfordulási gyakoriságát tekintve (azaz nem az idős korban halmozódik az előfordulás!).[45]
Genetika[szerkesztés]
A genetikai tényezők szerepét a méhnyakrák kialakulása szempontjából elhanyagolhatónak tartják. Arra viszont vannak adatok, hogy a HLA-B7 és a HLA-DQ8 fehérjék szintézisét kódoló gének bizonyos populációkban növelték a méhnyakrák kockázatát.[34]
Biztató kutatások folynak az indol-3-karbinol nevű, a brokkoliban nagy mennyiségben megtalálható vegyülettel a HPV megelőzésében, kezelésében való felhasználására.[46] A jelenlegi feltételezések szerint az indol-3karbinol az antigének inhibíciójával segíti a HPV módosult sejtek normális fenotípusú sejtekre való átalakulását és támogatja a daganatos és humán papillomavírussal fertőzött sejtek beprogramozott elhalását.
Terápia[szerkesztés]


A gyógyulás[47] esélyeit alapjában az határozza meg, hogy a betegség felfedezése melyik fokozatban (stádiumban) történik. Ha az elváltozás még a hámon belül van, a teljes gyógyulás egyszerű műtéti beavatkozással, az érintett szövetrész kúp alakú kimetszésével (konizációval)[1][15][48] elérhető. Ha már tovább terjedt, csak bonyolultabb műtéti eljárásokkal, sugárkezeléssel[49] és sejtoszlást gátló szerekkel[47][50] kombinálva hozhatnak esetleges eredményt. Bizonyos súlyossági fokozatokon túl a gyógyulás már reménytelen, a beteg élettartamát a nagyon súlyos és kiterjedt (heroikus) műtéti beavatkozások, az intenzív sugárkezelés és a sejtoszlást gátló gyógyszerek kiterjedt alkalmazása is csak meghosszabbítani tudja. Ugyanakkor ezek kellemetlen mellékhatásokat is okoznak, fontos a fájdalomcsillapítás.[51] A kezelés módját a kezelőorvos más szakorvosokkal konzultálva határozza meg.
A méhnyakrák gyógyításában alkalmazott fő eljárások súlyossági fokozatok (stádiumok) szerint[szerkesztés]
- 1-A1 stádium fiatal nőknél – konizáció éles határral. Többgyermekes nők – műtéti úton történő méheltávolítás (hiszterektómia).[1]
- 1-A2 stádium. A nyirokcsomók eltávolítása a hasüreg megnyitásával (laparoszkópia) + a méhnyak sebészeti eltávolítása (trechelektómia) + sugárterápia.
- 1B & 2A stádium. 1. Wertheim-féle méheltávolítás[52] a hasfal műtéti felmetszésével, laparotomiával a hasüreg felől, . 2. Schauta szerinti,[53] hüvelyen keresztüli (vaginális) méheltávolítás + hasüreg tükrözéses (laparoszkópiás) nyirokcsomó-eltávolítás.[54]
- 2B, 3, 4 stádium. Kemoterápia (sejtoszlást gátló gyógyszerek adagolása).
Kórjóslat (prognózis)[szerkesztés]
Erre vonatkozóan az előző részek már tartalmaznak néhány alapvető szempontot. A korai stádiumban felismert elváltozás lényegében teljes mértékben gyógyítható. A későbbi stádiumokat elért konkrét, egyedi eseteknél a gyógymódot a szakorvosok az alapbetegség előrehaladottsága mellett, egyéb szempontok figyelembevételével – életkor, általános fizikális állapot, más betegségek fennállása, a beteg személyisége, családi körülményei stb. – tudják meghatározni.[55]
Megelőzés[szerkesztés]
HPV védőoltás[szerkesztés]
A megfelelő vakcinákkal[56][57][58][59][60] történő védőoltások (mesterséges aktív immunitás) jelentik a leghatásosabb megelőzést. A védőoltás beadásának optimális időpontja az aktív szexuális élet megkezdése előtti időszakra esik.
Kockázati tényezők elkerülése[szerkesztés]
A megelőzés egyéb formáit – értelemszerűen – a fentebb felsorolt kockázati tényezők lehetőség szerinti elkerülése jelenti.

Szűrővizsgálatok[szerkesztés]
Mivel a korai hatásos védőoltásokból a veszélyeztetett női népesség nagy része nem részesülhetett (bár előbbiek azt mutatják, hogy később is vannak lehetőségek), a kórkép pedig a beteg által észlelhetetlenül, tünet- és panaszmentesen alakul ki, a nőgyógyászati szűrővizsgálatoknak igen nagy a jelentősége.[11][61][62] A szűrővizsgálatokkal emellett más, műtétileg jól korrigálható nőgyógyászati elváltozások is felismerhetők.
Méhnyakrák szűréskor végzett vizsgálatok[szerkesztés]
Kolposzkópia[szerkesztés]
A nőgyógyász a feltárt hüvelyen keresztül egy fényforrással és mikroszkópos nagyítóval ellátott optikai készülékkel (kolposzkóp) megtekinti a méhszájat az esetleges elváltozások észlelésére.
Citológiai vizsgálat (sejttani, sejtkenet vizsgálat, Pap-teszt, Papanicolaou-teszt)[szerkesztés]
A kolposzkópia után a nőgyógyász a méhszájból kenetet készít, amelyet Papanicolaou-szerint megfestve laboratóriumban sejttani (citológiai) vizsgálat alá vetnek.[63] Az eljárás a szokásos rutin nőgyógyászati vizsgálatok kellemetlenségein kívül fájdalmat nem okoz. Esetleges rendellenesség fennállása esetén a nőgyógyász további vizsgálatokat, illetve kezeléseket javasol.
HPV-vizsgálat[szerkesztés]
Erre akkor kerül sor, ha ezt két egymást követő citológiai (sejttani) lelet indokolttá teszi, vagy a páciens maga kéri. Magyarországon 2003 óta van államilag szervezett, a 25–65 éves korosztályra kiterjedő ingyenes, három évenkénti szűrés, emellett minden nőgyógyászati vizsgálat egyben szűrés is (ami térítés ellenében ezen kívül is kérhető). Az átlagos részvételi arány ennek ellenére csak 37%-os. A magánrendelésen végzett vizsgálatok térítéskötelesek. A média manapság rengeteg információval szolgál a méhnyakrákról, mindez azonban nem helyettesíti a páciensét jól ismerő orvos személyre szóló tanácsait.
Epidemiológia[szerkesztés]

Világszerte[szerkesztés]
A méhnyakrák[65] a 12. leggyakoribb ráktípus,[66] és a női halálozási arányt tekintve az ötödik a rák okozta elhalálozások között.[7] Évente 100 000 nőből 16 betegszik meg, ebből 9 eset halálos kimenetelű.[67] A méhnyakrákos megbetegedések megközelítőleg 80%-a a fejlődő országokban fordul elő. Becslések szerint a világon mintegy 500 000 új eset van évente. 2008-ban 473 000 méhnyakrákos eset volt, a méhnyakrákban elhaltak évi száma pedig 253 500 főt tett ki.[68]
Magyarországon[szerkesztés]
A méhnyakrák okozta évenkénti halálozások száma Magyarországon mintegy 500 főre tehető,[10] és 1000–1500 új eset van évente (a közölt adatok elég eltérőek).[10]
A nőgyógyászati méhnyakrákszűréseken való 37%-os részvételi arány a legmagasabb szűrési kultúrájú országokhoz képest viszonylag alacsony. Ebben – egy tanulmány szerint – szerepet játszik a magyar nők nőgyógyászati vizsgálatokkal szembeni – nem teljesen indokolatlan – averziója is.[69] (Az intim szférát érintő és elég kellemetlen vizsgálatról van szó, amihez az optimális feltételek nem mindenütt adottak.)
Társadalmi és kulturális tényezők
A nők ismeretei sajnos még a fejlett országokban is szerénynek mondhatóak a méhnyakrákot illetően. Egy amerikai felmérés szerint a nőknek csak 40%-a hallott a HPV vírusfertőzésről, és csak 20% tudott annak a méhnyakrákkal való kapcsolatáról.[70] Az előbbi hazai adatok sem utalnak jobb helyzetre, bár az idézett magyar források azt mutatják, hogy igen intenzív felvilágosító munka folyik.
Jegyzetek[szerkesztés]
- ↑ a b c Lampé László:. "Szülészet nőgyógyászat" (Egyetemi tankönyv; Harmadik, javított kiadás (magyar nyelven). Medicina Könyvkiadó (Budapest) (1987)
- ↑ "Méhnyakrák" (magyar nyelven). [2013. május 17-i dátummal az eredetiből archiválva]. (Hozzáférés: 2011. szeptember 16.)
- ↑ "Cervical Cancer Treatment (PDQ®)". NCI. 2014-03-14. Eredetiből archiválva 2014. július 5-én. Feltöltve: 2014. június 24.
- ↑ a b c Walboomers JM, Jacobs MV, Manos MM, et al (1999). „Human papillomavirus is a necessary cause of invasive cervical cancer worldwide” (angol nyelven). J. Pathol. 189 (1), 12–9. o. DOI:<12::AID-PATH431>3.0.CO;2-F 10.1002/(SICI)1096-9896(199909)189:1<12::AID-PATH431>3.0.CO;2-F. PMID 10451482.
- ↑ a b c Kumar, Vinay; Abbas, Abul K.; Fausto, Nelson; & Mitchell, Richard N.:. Robbins Basic Pathology (8th ed.) (angol nyelven). Saunders Elsevier., 718–721. o. (2007)
- ↑ a b Kufe, Donald (2009). Holland-Frei cancer medicine (8th ed.). New York: McGraw-Hill Medical. p. 1299. ISBN 9781607950141. Archived from the original on 2015-12-01.
- ↑ a b World Cancer Report 2014. World Health Organization. 2014. pp. Chapter 5.12. ISBN 9283204298.
- ↑ Dunne, EF; Park, IU (Dec 2013). "HPV and HPV-associated diseases". Infectious Disease Clinics of North America. 27 (4): 765–78. doi:10.1016/j.idc.2013.09.001. PMID 24275269.
- ↑ Ljubojevic, Suzana; Skerlev, Mihael (2014). "HPV-associated diseases". Clinics in Dermatology. [1]
- ↑ a b c Kiss Éva (2010. június 4.). „"Félezer elkerülhető haláleset"” (magyar nyelven). HáziPatika. (Hozzáférés: 2011. szeptember 12.) [halott link]
- ↑ a b U.S. Preventive Services Task Force: "Screening for Cervical Cancer: Recommendations and Rationale". AHRQ Publication No. 03-515A. (angol nyelven). Agency for Healthcare Research and Quality, 2003. [2016. január 2-i dátummal az eredetiből archiválva]. (Hozzáférés: 2010. június 5.)
- ↑ a b McNeil C (2006. April). „[jnci.oxfordjournals.org/cgi/content/full/98/7/433 Who invented the VLP cervical cancer vaccines?]” (angol nyelven). J. Natl. Cancer Inst. 98 (7), 433. o. DOI:10.1093/jnci/djj144. PMID 16595773. (Hozzáférés: 2011. szeptember 16.) PMID 16595773
- ↑ „"Pap smear"” (Hozzáférés: 2011. szeptember 12.) (angol nyelvű)
- ↑ Kastler Bruno ; Patay Zoltán. "MRI orvosoknak" (magyar nyelven). Budapest ISBN 88-85980-14-7, 252. o. (1993). Hozzáférés ideje: 2011. szeptember 12.
- ↑ a b c Lám Luca: (2007. július 18). „"A méhnyakrák 6 előjele. A rák és a HPV vírus"” (magyar nyelven). Femina.hu. (Hozzáférés: 2011. szeptember 11.)
- ↑ a b c DeMay, M. "Practical principles of cytopathology. Revised edition.". Chicago, IL: American Society for Clinical Pathology Press (2007). ISBN 978-0-89189-549-7
- ↑ World Health Organization
- ↑ Garcia, Agustin; Omid Hamid, Anthony El-Khoueiry: "Cervical Cancer" (angol nyelven). eMedicine. WebMD, 2006. július 6. (Hozzáférés: 2011. szeptember 11.)
- ↑ Dolinsky, Christopher. „"Cervical Cancer: The Basics"”, OncoLink, University of Pennsylvania, 2006. július 17.. [2008. január 18-i dátummal az eredetiből archiválva] (Hozzáférés: 2011. november 2.) (angol nyelvű)
- ↑ International Federation of Gynecology and Obstetrics
- ↑ National Cancer Institute. „accessdate=2011-09-12 "Cancer staging: TNM"” (angol nyelvű)
- ↑ Parkin DM (2006). „The global health burden of infection-associated cancers in the year 2002”. Int. J. Cancer 118 (12), 3030–44. o. DOI:10.1002/ijc.21731. PMID 16404738. „With respect to cancer of the cervix, oncogenic HPV may be detected by PCR in virtually all cases of cervix cancer, and it is generally accepted that the virus is necessary for development of cancer, and that all cases of this cancer can be ‘attributed’ to infection.”
- ↑ Maura L. Gillison, Keerti V. Shah. „"Mucosal Human Papillomavirus in Non genital Cancers"” (angol nyelven). Journal of the National Cancer Institute Monographs No. 31. (Hozzáférés: 2011. szeptember 15.)
- ↑ James McGil. „"History of HPV"”. eHow health. (Hozzáférés: 2011. szeptember 15.)
- ↑ "HPV" (magyar nyelven). (Hozzáférés: 2011. szeptember 11.)[halott link]
- ↑ Cornelis J.A. Hogewoning, Maaike C.G. Bleeker, et al. (2003). „"Condom use Promotes the Regression of Cervical Intraepithelial Neoplasia and Clearance of HPV: Randomized Clinical Trial"”. International Journal of Cancer 107 (5), 811–816. o. DOI:10.1002/ijc.11474. PMID 14566832. (Hozzáférés: 2011. szeptember 12.)
- ↑ Anna R Giuliano, Alan G Nyitray, Ginesa Albero (2011. January 15). „"Male circumcision and HPV transmission to female partners"”. The Lancet 377 (9761), 183 - 184. o. DOI:10.1016/S0140-6736(10)62273-8. (Hozzáférés: 2011. szeptember 29.)
- ↑ Marrazzo JM, Koutsky LA, Kiviat NB, Kuypers JM, Stine K (2001). „Papanicolaou test screening and prevalence of genital human papillomavirus among women who have sex with women.” (angol nyelven). Am J Public Health 91 (6), 947–52. o. DOI:10.2105/AJPH.91.6.947. PMID 11392939. (Hozzáférés: 2011. szeptember 20.)
- ↑ a b American Cancer Society: ”What are the risk factors for cervical cancer?” (angol nyelven), 2010. September 19. [2011. szeptember 24-i dátummal az eredetiből archiválva]. (Hozzáférés: 2011. szeptember 16.)
- ↑ WebMD: ”Smoking Boosts Cervical Cancer Risk” (angol nyelven), 2006. November 17. (Hozzáférés: 2011. szeptember 16.)
- ↑ a b c (2009. március 10.) „"Early age at first sexual intercourse and early pregnancy are risk factors for cervical cancer in developing countries"” (angol nyelven). British Journal of Cancer 100 (7), 1191–1197. o. DOI:10.1038/sj.bjc.6604974.
- ↑ "Sexually transmitted disease; STD" (angol nyelven). (Hozzáférés: 2011. szeptember 12.)
- ↑ American Cancer Society
- ↑ a b National Cancer Institute. „"Cancer, various tissues; Cervical cancer"”, National Institute of Health (Hozzáférés: 2011. szeptember 16.) (angol nyelvű)
- ↑ Nader, Carol. „”Expert says circumcision makes sex safer””, The Age, Fairfax Media, 2005. február 16. (Hozzáférés: 2011. szeptember 15.) (angol nyelvű)
- ↑ [1]
- ↑ a b Sedjo RL, Roe DJ, Abrahamsen M, et al (2002). „Vitamin A, carotenoids, and risk of persistent oncogenic human papillomavirus infection”. Cancer Epidemiol. Biomarkers Prev. 11 (9), 876–84. o. PMID 12223432.
- ↑ a b Yeo AS, Schiff MA, Montoya G, Masuk M, van Asselt-King L, Becker TM (2000). „Serum micronutrients and cervical dysplasia in Southwestern American Indian women”. Nutrition and cancer 38 (2), 141–50. o. DOI:10.1207/S15327914NC382_1. PMID 11525590.
- ↑ a b Giuliano AR, Siegel EM, Roe DJ, et al (2003). „Dietary intake and risk of persistent human papillomavirus (HPV) infection: the Ludwig-McGill HPV Natural History Study”. J. Infect. Dis. 188 (10), 1508–16. o. DOI:10.1086/379197. PMID 14624376.
- ↑ a b Giuliano AR, Papenfuss M, Nour M, Canfield LM, Schneider A, Hatch K (1997). „Antioxidant nutrients: associations with persistent human papillomavirus infection”. Cancer Epidemiol. Biomarkers Prev. 6 (11), 917–23. o. PMID 9367065.
- ↑ a b Goodman MT, Shvetsov YB, McDuffie K, et al (2007). „Hawaii cohort study of serum micronutrient concentrations and clearance of incident oncogenic human papillomavirus infection of the cervix”. Cancer Res. 67 (12), 5987–96. o. DOI:10.1158/0008-5472.CAN-07-0313. PMID 17553901.
- ↑ Kwaśniewska A, Tukendorf A, Semczuk M (1997). „Content of alpha-tocopherol in blood serum of human Papillomavirus-infected women with cervical dysplasias”. Nutrition and cancer 28 (3), 248–51. o. DOI:10.1080/01635589709514583. PMID 9343832.
- ↑ Alan H. Pressman, Sheila Buff: The Complete Idiot's Guide to Vitamins and Minerals, alpha books (A Simon and Schuster Macmillan Company), 1997, ISBN 0-02-862116-6
- ↑ Sedjo RL, Papenfuss MR, Craft NE, Giuliano AR (2003). „Effect of plasma micronutrients on clearance of oncogenic human papillomavirus (HPV) infection (United States)”. Cancer Causes Control 14 (4), 319–26. o. DOI:10.1023/A:1023981505268. PMID 12846362.
- ↑ „"Cervical cancer - UK statistics"” (Hozzáférés: 2011. szeptember 16.) (angol nyelvű)
- ↑ Indole-3-Carbinol Prevents PTEN Loss in Cervical Cancer In Vivo[2]
- ↑ a b "Rákgyógyítás" (magyar nyelven). (Hozzáférés: 2011. szeptember 16.)
- ↑ Erstad, Shannon. „"Cone biopsy (conization) for abnormal cervical cell changes"”, WebMD, 2007. január 12. (Hozzáférés: 2011. szeptember 11.) (angol nyelvű)
- ↑ Camphausen KA, Lawrence RC. "Principles of Radiation Therapy" Archiválva 2009. május 15-i dátummal a Wayback Machine-ben in Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (Eds) Cancer Management: A Multidisciplinary Approach Archiválva 2013. október 4-i dátummal a Wayback Machine-ben. 11 ed. 2008.
- ↑ „"FDA Approves First Drug Treatment for Late-Stage Cervical Cancer"”, U.S. Food and Drug Administration, 2006. június 15. (Hozzáférés: 2011. szeptember 11.) (angol nyelvű)
- ↑ Richard S. Snell:.szerk.: Lippincott Williams & Wilkins, Ed.6th; Philadelphia, Baltimore, New York, London: Clinical Neuroanatomy (angol nyelven) (2006 ISBN 978-963-226-293-2)
- ↑ "Wertheim-féle méheltávolítás" (angol nyelven). [2012. március 17-i dátummal az eredetiből archiválva]. (Hozzáférés: 2011. szeptember 16.)
- ↑ Massi, G.:: "Schauta-Amreich vaginal hysterectomy and Wertheim-Meigs ..." (angol nyelven). (Hozzáférés: 2011. szeptember 16.)
- ↑ D. Dargent, P. Mathevet (1995. December). „"4 Schauta's vaginal hysterectomy combined with laparoscopic lymphadenectomy"” (angol nyelven). Baillière's Clinical Obstetrics and Gynaecology; Advanced Laparoscopic Surgery 9 (4), 691-705. o. (Hozzáférés: 2011. szeptember 16.)
- ↑ "Cervical Cancer" (angol nyelven). Cervical Cancer: Cancers of the Female Reproductive System: Merck Manual Home Edition. Merck Manual Home Edition
- ↑ Athol Kent, MBChB, MPhil, FRCOG (2010 Winter. March 1). „”. Rev Obstet Gynecol. Full Text 3 (01). (Hozzáférés: 2011. november 14.)
- ↑ Hámor Éva (2007. január 31). „"Lehetőség a méhnyakrák megelőzésére"” (magyar nyelven). HáziPatika. (Hozzáférés: 2011. szeptember 11.) [halott link]
- ↑ "HPV prevention" (angol nyelven)[halott link]
- ↑ "HPV Vaccines" (angol nyelven). Centers for Disease Control and Prevention (CDC), 2010. október 15. (Hozzáférés: 2011. február 27.)
- ↑ "Genital HPV Infection - CDC Fact Sheet" (angol nyelven). Centers for Disease Control and Prevention (CDC), 2009. november 24. (Hozzáférés: 2011. szeptember 16.)
- ↑ Saslow D, Runowicz CD, Solomon D, et al (2002). „"American Cancer Society guideline for the early detection of cervical neoplasia and cancer"” (angol nyelven). CA: a cancer journal for clinicians 52 (6), 342–62. o. DOI:10.3322/canjclin.52.6.342. PMID 12469763. (Hozzáférés: 2011. szeptember 17.)
- ↑ "M. Arbyn; et al. (2010). „"European Guidelines for Quality Assurance in Cervical Cancer Screening". Second Edition” (angol nyelven). Annals of Oncology 21 (3), 448–458. o. DOI:10.1093/annonc/mdp471. PMID 20176693. (Hozzáférés: 2011. szeptember 17.)
- ↑ Hans N, Cave AJ, Szafran O, Johnson G, Glass A, Spooner GR, Klemka PJ, Schipper S. at Meadowbrook Medical Clinic, Edmonton (2007. Aug). „"Papanicolaou smears: to swab or not to swab"” (angol nyelven). Can Fam Physician (8), Kiadó: pub med. gov. (Hozzáférés: 2011. szeptember 25.)
- ↑ WHO Disease and injury country estimates, 2009. (Hozzáférés: 2011. szeptember 14.)
- ↑ (1999. August 15) „"Cervical Cancer Overview, Incidence & Prevalence of Cervical Cancer"” (angol nyelven). HealthCommunities.com, Kiadó: HealthCommunities.com. (Hozzáférés: 2011. szeptember 17.)
- ↑ Egészségügyi Világszervezet: Fact sheet No. 297: Cancer, 2006. February. (Hozzáférés: 2011. szeptember 14.)
- ↑ GLOBOCAN 2002 database: summary table by cancer. [2008. június 16-i dátummal az eredetiből archiválva]. (Hozzáférés: 2011. szeptember 17.)
- ↑ NCCC National Cervical Cancer Coalition. [2008. augusztus 22-i dátummal az eredetiből archiválva]. (Hozzáférés: 2011. szeptember 17.)
- ↑ Karamánné Pataki Annamária. A méhnyakrák szürésen való megjelenés motivációjának vizsgálata; Doktori értekezés. Semmelweis Egyetem Patológiai Tudományok Doktori Iskola (Budapest) (2010). Hozzáférés ideje: 2011. szeptember 25.
- ↑ Tiro JA, Meissner HI, Kobrin S, Chollette V (2007). „"What do women in the U.S. know about human papillomavirus and cervical cancer?"” (angol nyelven). Cancer Epidemiol. Biomarkers Prev. 16 (2), 288–94. o. DOI:10.1158/1055-9965.EPI-06-0756. PMID 17267388. (Hozzáférés: 2011. szeptember 16.)
Források[szerkesztés]
- DeMay, M.: Practical principles of cytopathology. Revised edition.. (IL: American Society for Clinical Pathology Press, Chicago 2007). ISBN 978-0-89189-549-7.
- Lampé, László: Szülészet nőgyógyászat (Egyetemi tankönyv; Harmadik, javított kiadás: 1-3. kötet(Medicina Könyvkiadó, Budapest 1987) ISBN 963-241-587-6
További információk[szerkesztés]
- A méh rosszindulatú daganatai (méhnyakrák, méhtesrák) Archiválva 2018. február 18-i dátummal a Wayback Machine-ben
- Méhnyakrák az Open Directory Project-ben
- A méhnyakrák tünetei, kezelése és megelőzése
| Az itt található információk kizárólag tájékoztató jellegűek, nem minősülnek orvosi szakvéleménynek, nem pótolják az orvosi kivizsgálást és kezelést. A cikk tartalmát a Wikipédia önkéntes szerkesztői alakítják ki, és bármikor módosulhat. |


