Hepatitis C
| Hepatitis C | |
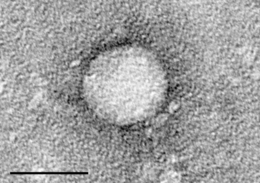 | |
| Elektronmikroszkópos felvétel a HCV vírusról (negatív festés). Skálavonal = 50 nanométer | |
| Szinonimák | Vírusos (virális) májgyulladás, Krónikus májgyulladás |
| Latinul | Hepatitis C |
| Angolul | Hepatitis C |
| Osztályozás | |
| BNO-10 | B17.1, B18.2 |
| BNO-9 | 070.70,070.4, 070.5 |
| Epidemiológia | |
| Földrajzi előfordulás | Fejlődő országokban gyakoribb |
| Prevalencia | |
| Magyarországon | A vírushordozók számát 0,7-1,3%-ra becsülik |
| Világszerte | 130-170 millió ember |
| Incidencia | |
| Világszerte | nincsenek pontos adatok |
| Halálozási arány | |
| Magyarországon | Hirtelen, súlyos lefolyású formájánál közel 100%. Krónikus lefolyású eseteknél már a szövődmények okozta halálesetek dominálnak. |
| Világszerte | 250 000 évente |
| Leírás | |
| Érintett szervek | Elsősorban a máj, közvetve az egész szervezet. |
| Etiológia | Hepatitis C vírus |
| Kockázati tényezők | Nem megfelelően ellenőrzött vérkészítmény, nem kellő gondossággal megválasztott eszközök, intravénás droghasználat, tetoválás. Testnedvekkel történő fertőzés |
| Főbb tünetek | Általános rosszullét, emésztési zavarok, sárgaság, nagyfokú fáradékonyság, de az esetek 85%-ban tünetmentes. |
| Diagnosztika | Tünetek értékelése, laboratóriumi vizsgálat, vírus kimutatása. |
| Szövődmények | Májelégtelenség, májzsugor, egész életen át tartó panaszok és fertőzőképesség. Magyarországon évente 2000-4000 májzsugor és 600 májrák. |
| Kezelés | Oki terápiaként az interferont és a vírusölő ribavirint használják. Májkímélő étrend, a májműködés támogatása, a máj által termelt fontos faktorok pótlása, kortikoszteroidok, elkülönített eszközökkel való kezelés. A májátültetés nem jelent végleges megoldást. |
| Kórjóslat | Igen kedvezőtlen az életminőség szempontjából |
| Megelőzés | Vérkészítmények gondos szűrése, egyszer használatos eszközök használata, drogosoknál eldobható tűk és fecskendők.[1] Hatásos védőoltás ellene jelenleg még nincs. |
| Adatbázisok | |
| OMIM | 609532 |
| DiseasesDB | 5783 |
| MedlinePlus | 000284 |
| eMedicine | med/993 ped/979 |
| MeSH ID | D006526 |
A Wikimédia Commons tartalmaz Hepatitis C témájú médiaállományokat. | |
A hepatitis C vírusos fertőzés, amelyet a hepatitis C-vírus (HCV) okoz.[2][3] A kórkép elsősorban a májat érinti, de a máj sokrétű funkcióinak károsításával az egész szervezet súlyos állapotba kerül, emellett a kórokozó más szervekben is elterjed és azokat is megbetegíti. Lappangási ideje 2-25 hét. A hepatitis C gyakran tünetmentes, a krónikus fertőzés azonban a máj hegesedéséhez, majd több év után májzsugorhoz vezethet. Egyes esetekben a májzsugorban szenvedő betegeknél májelégtelenség, májrák is kialakulhat, vagy - mivel a portális keringés akadályozott - (a portocavalis anastomozisok - a májkapugyűjtőér (vena portae) alsó nagy vénával (vena cava inferior) meglévő vékony falú összekötő erei) kitágulnak és megrepedhetnek a nyelőcsőben és a végbélben és vérzést okozhatnak. A nyelőcső vénatágulatainak vérzése nagyon gyakran halálos kimenetelű.[2] A végbél aranyeres csomóiból bekövetkező vérzés viszont a portális keringés tehermentesítésével jó hatású is lehet.
A hepatitis C főként vérrel való érintkezés útján terjed intravénás droghasználat, nem steril orvosi eszközök alkalmazása, és vérátömlesztés során. Becslések szerint világszerte 130–170 millió ember fertőződött meg a hepatitis C-vírussal. A kutatók az 1970-es években kezdték el a HCV tanulmányozását és 1989-ben bizonyították a vírus létezését.[4] Ismereteink szerint a vírus állatoknál nem, csak embereknél és csimpánzoknál okoz megbetegedést.
A hepatitis C abban hasonlít az A-hoz és a B-hez, hogy szintén vírusos májgyulladás, de lényeges tulajdonságaiban különbözik is azoktól. Behatóbb megismerése lényegében az utóbbi évek eredménye, és ez a megismerési folyamat ma is tart. Rengeteg még a megválaszolandó kérdés, ez magyarázza, hogy az irodalomban is nagyon sok az egymástól eltérő, vagy éppen ellentmondó adat, ahhoz hasonlóan, ahogy korábban a Hepatitis B is komoly gondokat okozott, de az orvostudományi kutatásoknak abban is sikerült igen jelentős eredményeket elérni, és az alapvető kérdéseket megoldani.
A HCV okozta megbetegedésben általánosan alkalmazott gyógyszer a peginterferon és a ribavirin. A kezelt betegek 50 és 80 közötti százaléka meggyógyul. A betegség előrehaladott szakaszában azonban, a májzsugorban vagy májrákban szenvedő betegek esetében májátültetésre lehet szükség. A műtét lehetővé teszi a beteg túlélését, de a vírus a szervátültetést követően általában visszatér.[5] A hepatitis C-vírus ellen jelenleg nincs védőoltás a vírus rendkívüli változékonysága miatt.
Tünetek[szerkesztés]
Akut fertőzés[szerkesztés]
A hepatitis C csupán az esetek 15%-ában okoz akut tüneteket.[6] A tünetek a leggyakrabban enyhék és nem körülhatároltak, beleértve az étvágycsökkenést, a fáradtságot, a hányingert, az izom- és az ízületi fájdalmakat, valamint a súlycsökkenést.[7] Csak néhány esetben fordul elő, hogy az akut fertőzés sárgaságot okoz.[8] A fertőzés az esetek 10 és 50 közötti százalékában kezelés nélkül is elmúlik, (vagy csak tünetmentessé válik?) fiatal nőknél gyakrabban, mint másoknál.[8]
Krónikus fertőzés[szerkesztés]

A vírusfertőzés az esetek nyolcvan százalékában krónikus megbetegedést alakít ki.[9] A fertőzés első tíz évében a legtöbb beteg tünetszegény vagy tünetmentes,[10] jóllehet a krónikus hepatitis C állandó, fokozott fáradékonysággal jár.[11] A hepatitis C a több éven át fertőződött betegeknél a májzsugor és a májrák kialakulásának elsődleges oka.[5] Magyarországon évente 2000 - 4000 beteg májzsugorának kialakulásáért és 600 májrákos esetért felelős a hepatitis C fertőzés.[12] A 30 évnél hosszabb ideig fertőzött betegek 10-30 százalékánál májzsugor alakul ki.[5][7] A májzsugor előfordulásának gyakorisága nagyobb az alkoholistáknál, a férfiaknál, valamint azoknál a betegeknél, akiknél hepatitis B-vírussal vagy HIV-vel való fertőzés is fennáll.[7] A májzsugorban szenvedő betegeknél a májrák kialakulásának valószínűsége hússzor nagyobb, évente 1-3%-os arányban.[5][7] Az alkoholisták esetében a kockázat százszor nagyobb.[13] A májzsugoros esetek 27%-át és a májrákos esetek 25%-át hepatitis C okozza.[14]
A májzsugor a májhoz kapcsolódó (portális) vénák-ban fokozott nyomást idézhet elő és hasi vízgyülemhez (hasvízkór; ascites) vezethet, valamint a beteg hajlamosabb a véraláfutásra vagy a vérzésre, és a betegség, különösen a nyelőcsőben és a gyomorban visszértágulathoz, sárgasághoz (hepatocellularis icterus), valamint agykárosodáshoz (ami a megismerési funkciók zavarával jár; Hepaticus encephalopathia) vezethet.[15]
Májon kívüli hatások[szerkesztés]
A hepatitis C fertőzés ritkábban Sjögren-szindrómát (autoimmun betegség), thrombocytopéniát (a vérlemezkék normálisnál alacsonyabb száma), krónikus bőrbetegséget, cukorbetegséget vagy non-Hodgkin limfómát[16] okozhat.[17][18] A Hyde's prurigo nodularis[19]-sal és a membranoproliferative glomerulonephritis[20]-sel való feltételezett összefüggésről is beszámoltak,[11] a Hepatitis C fertőzés szintén kapcsolatban áll a kevert cryoglobolinémiának[21] nevezett állapottal, amely a kis és közepes nagyságú véredények gyulladása (azaz olyan vasculitis, amelyet cryoglobolint tartalmazó immunkomplexek lerakódása okoz[22]
Kiváltó okok[szerkesztés]

A hepatitis C-vírus kisméretű, burokkal rendelkező, egyszálú, pozitív irányú RNS-vírus.[5] A Flaviviridae családon belül a Hepacivirus nemzetségbe tartozik.[11] Hét főbb HCV genotípust különböztetünk meg.[23] Az Egyesült Államokban az esetek 70%-át az 1-es, 20%-át a 2-es, 1%-át pedig a többi genotípus okozza.[7] Az 1-es genotípus úgyszintén a leggyakoribb Dél-Amerikában és Európában.[5]
Terjedés[szerkesztés]
A fejlett országokban a fertőzés elsősorban intravénás droghasználat útján terjed. A fejlődő országokban a betegség főként vérátömlesztés és a nem biztonságos orvosi eljárások miatt alakul ki.[24] A terjedés okaira az esetek 20%-ában nem derül fény,[25] azonban feltételezik, hogy ezen esetek túlnyomó többsége az intravénás droghasználatnak tudható be.[8]
Intravénás droghasználat[szerkesztés]
A világ sok részén a hepatitis C legfontosabb kockázati tényezője az intravénás drog használat.[26] Egy 77 országra kiterjedő tanulmányban kimutatták, hogy 25 országban (köztük az Egyesült Államokban és Kínában) az intravénás droghasználók között a hepatitis C fertőzés aránya 60 és 80% közötti.[9][26] Tizenkét országban ez az arány nagyobb, mint 80%.[9] Világszerte tízmillió intravénás droghasználó fertőződhetett meg hepatitis C-vel, legtöbben Kínában (1,6 millió), az Egyesült Államokban (1,5 millió), és Oroszországban (1,3 millió).[9] Az Egyesült Államokban a börtönlakók között 10-20-szor nagyobb a hepatitis C előfordulása, mint az átlagpopulációban. Tanulmányok szerint ez a magas kockázatú viselkedési formáknak – például az intravénás droghasználatnak és a nem steril eszközökkel végzett tetoválásnak – tudható be.[27][28]
Kitettség egészségügyi ellátáskor[szerkesztés]
HCV-szűrés nélküli vérátömlesztés, vérkészítmény, és szervátültetés jelentősen növeli a fertőzés kockázatát.[7] Kanadában 1990-ben, az Egyesült Államokban 1992-ben általános szűrést vezettek be. Azóta a fertőzés aránya 200 egységnyi vérre eső egy esetről (0,5%)[29] 10 000 egységenként egy esetre, majd 10 000 000 egységenként egy esetre csökkent.[8][25] Ez az alacsony kockázat továbbra is fennáll, mivel a potenciális véradó hepatitis C-vel való megfertőződése és a véradó pozitív vérvizsgálati eredményének a kimutatása között hozzávetőlegesen 11 és 70 nap közötti időszak van.[25] Egyes országok a költségek miatt még mindig nem szűrnek hepatitis C-re.[14] Magyarországon 1992. óta végeznek szűrővizsgálatokat a hepatitis C vírus ellen.[12]
Amennyiben HCV-fertőzött személytől származó tűszúrás okozta sérülés jön létre, a megbetegedés esélye 1,8%.[7] A kockázat nagyobb, ha a tű üreges és a szúrt seb mély.[14] Fertőzés veszélye akkor is fennáll, ha a nyálkahártya vérrel érintkezik, ez a kockázat azonban alacsony. Nincs kockázat akkor, ha a vér ép bőrrel érintkezik.[14]
Kórházi felszereléssel is közvetíthető a hepatitis C-vírus, mégpedig tű és fecskendő újbóli használatával, többször használatos injekciós ampullával, infúziós tasakkal és nem steril sebészeti felszerelés többszöri használatával.[14] A világon Egyiptomban a legmagasabb a fertőzöttek aránya, ahol a HCV terjedése legfőképpen az orvosi és a fogorvosi létesítményekben alkalmazott nem megfelelő színvonalú szabványok (protokoll) használatával.[30]
Nem mellékes, hogy a vérrel és szövetekkel kapcsolatba kerülő egészségügyi személyzet szintén a fokozott kockázati csoportba tartozik. Különösen eszméletlen betegen végzett sürgős beavatkozások esetén semmi garancia nincs arra, hogy a beteg nem Hepatitis C vírus fertőzött-e (amiről a hozzátartozók, sőt maga a beteg sem tud). Az általános védőfelszerelések sem jelentenek teljes védelmet, életveszélyes állapotban lévő beteg ellátásakor pedig sokszor a "beöltözésre" sincs idő. Különösen veszélyeztetett helyzetben vannak a fogászok,[31] de más szakmák veszélyeztetettsége is komoly. Paradox módon éppen azokban a munkakörökben, ahol ez könnyen elkerülhető lenne, de nincsenek tudatában a fennálló kockázatnak.[32]
Nemi érintkezés[szerkesztés]
Nem ismert, hogy a hepatitis C nemi úton terjed-e.[33] Míg összefüggés van a magas kockázattal járó szexuális kapcsolat és a hepatitis C között, nem egyértelmű azonban, hogy a betegség a be nem ismert intravénás droghasználat vagy maga a nemi érintkezés útján terjed.[7] A tények alátámasztják, hogy nem áll fenn kockázat azoknál a heteroszexuális pároknál, akik nem élnek nemi életet másokkal.[33] Kockázatot jelent a végbélcsatorna belső felületének súlyos sérülését okozó nemi tevékenység - például az anális behatolás - vagy ha az érintkezéskor nemi úton terjedő fertőzés – többek között HIV-fertőzés vagy a nemi szervek fekélye - is fennáll.[33] Az Egyesült Államok Veteránügyi Minisztériuma óvszer használatát javasolja a hepatitis C fertőzés elkerülésére azoknál, akiknek több partnere is van de nem javasolja azoknál, akiknek csak egy partnerrel van viszonyuk.[34]
Tetoválás[szerkesztés]
A tetoválás elterjedésével két-háromszorosára nőtt a hepatitis C fertőzés veszélye.[35] Ez a nem steril eszközök használatának vagy az alkalmazott festékek szennyeződésének tudható be.[35] Az 1980-as évek közepe előtt alkalmazott, illetve a nem szakszerűen készült tetoválás vagy testékszer különös figyelmet érdemel, mivel abban a környezetben a steril eljárások nem megfelelő színvonalúak lehetnek. Úgy tűnik, a kockázat terjedelmes tetoválás esetén nagyobb.[35] A börtönlakók közel fele használ közösen nem steril tetováló felszerelést.[35] Engedéllyel rendelkező létesítményben készült tetoválást csak ritkán lehet közvetlen összefüggésbe hozni HCV fertőzéssel.[36] A testékszerek (piercing) behelyezése szintén jár bizonyos kockázattal.
Vérrel való érintkezés[szerkesztés]
Az olyan tisztálkodási eszköz, mint a borotva, a fogkefe, a manikűr- vagy a pedikűrkészlet vérrel érintkezhet. Közös használatukkor HCV-kitettség veszélye áll fenn.[37][38] Fokozott figyelemmel kell lenni a vágásra és az egyéb sérülésre vagy a vérzésre.[38] A HCV nem terjed olyan mindennapos érintkezéssel, mint az ölelés, a csók vagy az evő- és főzőeszközök közös használata.[38] (A fodrászoknál az AIDS miatt megtiltották a borotva használatát. Ez a Hepatitis C terjedésének korlátozására is szerencsés intézkedésnek bizonyult.)
Terjedés anyáról gyermekre[szerkesztés]
A hepatitis C terjedése fertőzött anyáról gyermekre a terhességek kevesebb, mint 10%-ában fordul elő.[39] A kockázat csökkentésére semmilyen intézkedés nincs.[39] A fertőzés a terhesség alatt vagy a szüléskor adható át.[25] A hosszas vajúdás nagyobb fertőzési kockázattal jár.[14] Nincs bizonyíték arra vonatkozóan, hogy a HCV szoptatás útján terjed; ennek ellenére a fertőzött anyának kerülnie kell a szoptatást, ha a mellbimbója kirepedt vagy vérzik,[40] vagy ha az anya vírusterhelése magas.[25]
Diagnózis[szerkesztés]

A hepatitis C kimutatására alkalmazott vizsgálatok többek között: HCV elleni antitest, az ELISA, a Western blot és a HCV-RNS mennyiségi vizsgálata.[7] A polimeráz-láncreakció (PCR) a fertőzés után egy-két héttel képes kimutatni HCV-RNS-t, míg az antitestek képződése és kimutatása között lényegesen hosszabb idő telhet el.[15] A korai diagnózist nyilván jelentősen megnehezíti az, hogy a tünetmentesség ill. a jellegtelen tünetek miatt a betegek nagy része nem is fordul orvoshoz. A későbbi diagnózis pedig már nagyon bekorlátozza a terápiás lehetőségeket. A krónikus hepatitis C olyan fertőzés, amelyben a hepatitis C-vírus több mint hat hónapig fennmarad; ezt az RNS jelenléte igazolja.[10] Mivel a krónikus fertőzések jellemzően évtizedekig tünetmentesek maradnak,[10] a klinikusok általában májfunkciós tesztek vagy a magasabb kockázatnak kitett személyek rutin szűrővizsgálata során fedezik fel. A teszt nem tesz különbséget az akut és a krónikus fertőzés között.[14]
Vérvizsgálat[szerkesztés]
A hepatitis C tesztelése jellemzően vérvizsgálattal kezdődik a HCV elleni antitestek minőségi meghatározásával rekombináns sejtekben, immunoblot eljárással (RIBA teszttel).[7] Amennyiben ez a teszt pozitív, az immunteszt ellenőrzésére, valamint a súlyosság megállapítására második tesztet is elvégeznek.[7] Az immuntesztet a HCV elleni antitestek minőségi meghatározásával rekombináns sejtekben, immunoblot eljárással ellenőrzik és HCV RNS polimeráz-láncreakcióval határozzák meg a fertőzés súlyosságát.[7] Ha nincs RNS és az immunoblot teszt pozitív, a személy korábbi fertőzésen esett át, azonban kezeléssel vagy spontán módon meggyógyult, ha az immunoblot negatív, az immunteszt érvénytelen volt.[7] A fertőzést követően hat-nyolc hétnek kell eltelnie ahhoz, hogy az immunteszt pozitív legyen.[11]
A fertőzés kezdeti szakaszában a májenzimek változást mutathatnak;[10] a számuk általában a fertőzést követő hetedik héten kezd emelkedni.[11] A májenzimek és a betegség súlyossága közötti kapcsolat gyenge.[11]
Szövettani vizsgálat[szerkesztés]
A máj szövettani vizsgálatával megállapítható a májkárosodás mértéke, az eljárás azonban - mint minden szövetmintavétel (biopszia) - kockázatokkal jár.[5] A szövettani vizsgálattal jellemzően a májszövet elváltozásai mutathatók ki, emellett rendellenességek találhatók a limfocitákban, a májkapu (porta hepatis) területének nyiroktüszőiben és az epeutakban.[5] Számos olyan vérvizsgálat áll rendelkezésre, amellyel megkísérelhető a károsodás súlyosságának a meghatározása és annak érdekében, hogy minél kevésbé kelljen szövettani vizsgálathoz folyamodni.[5]
Szűrés[szerkesztés]
Az Egyesült Államokban és Kanadában a fertőzöttek mindössze 5 és 50 közötti százaléka van tudatában az állapotának.[35] Az olyan magas kockázatcsoportba tartozók, mint a tetováltak esetében vizsgálatot javasolnak.[35] A szűrés továbbá a magas májenzimszinttel rendelkező személyeknél is ajánlott, mivel a krónikus hepatitisnek gyakorta ez az egyedüli jele.[41] Az Egyesült Államokban nem javasolt a rutinszűrés,[7] de fontolgatják az 1945 és 1965 között született személyek egyszeri szűrését.[42]
Megelőzés[szerkesztés]
2011-ben a hepatitis C ellen még nem létezett védőoltás. A védőoltások fejlesztés alatt állnak, és egyes esetekben biztatóak az eredmények.[43] Ezt azonban rendkívül megnehezíti a vírus nagyfokú változóképessége. Az olyan megelőzési stratégiák, mint a tűcsere-programok és a kábítószer-abúzus kezelése, együttes alkalmazásával a hepatitis C kockázata az intravénás droghasználók körében hozzávetőleg 75%-kal csökkenthető.[44] Egyaránt fontos a véradók országos szintű szűrése és az egészségügyi intézményekben nemzetközileg előírt óvintézkedések betartása.[11] Azokban az országokban, ahol nem elégséges a steril fecskendő ellátás, az egészségügyi szakembereknek a gyógyszereket injekció helyett szájon át kellene beadniuk.[14]
Kezelés[szerkesztés]
A HCV krónikus fertőzést okoz a fertőzött személyek 50 és 80 közötti százalékában. Az esetek 40 és 80 közötti százaléka kezeléssel gyógyítható.[45][46] Ritka eset, hogy a fertőzés kezelés nélkül is elmúlik.[8] A krónikus hepatitis C-ben szenvedő betegnek kerülnie kell az alkoholt és a májra nézve toxikus gyógyszert,[7] és a beteget be kell oltani hepatitis A és hepatitis B ellen.[7] Májzsugorban szenvedő betegnél ultrahangos vizsgálat ajánlott a májrák kimutatására.[7]
Gyógyszerek[szerkesztés]
Azoknak, akiknél a májrendellenességet bizonyítottan HCV okozta, kezelésre van szükségük.[7] A kezelés jelenleg, a HCV típusától függően, 24 vagy 48 héten keresztül tartó pegilált interferon és egy vírusellenes gyógyszer, a ribavirin[47] együttes alkalmazásából áll.[7] A gyógyszeres kezelést követően a betegek 50 és 60 közötti százalékánál jelentős javulás tapasztalható.[7] A boceprevirnek vagy a telaprevirnek a ribavirinnel és az alfa peginterferonnal történő együttes alkalmazása javítja a hepatitis C 1-es genotípus elleni választ.[48][49][50] A kezelés gyakran jár mellékhatásokkal, a kezelt betegek fele az influenzához hasonló tüneteket, egyharmaduk pedig érzelmi problémákat mutat.[7] A fertőzés utáni első hat hónapban alkalmazott kezelés hatékonyabb, mint azután, hogy a hepatitis C krónikussá válik.[15] Ha valaki újrafertőződik és nyolc-tizenkét hét után nem sikerül kigyógyulnia, pegilált interferon alkalmazása ajánlott 24 hétig.[15] A thalassemiában (az egyik vérbetegségben) szenvedő betegeknél a ribavirin alkalmazása hatásosnak tűnik, vérátömlesztésre lehet azonban szükség.[51]
Alternatív kezelés[szerkesztés]
Az alternatív gyógymódok hívei több kezelést is hatékonynak tartanak a hepatitis C kezelésében, többek között a máriatövis, ginzeng és ezüst-kolloid terápiát.[52] Azonban semmilyen alternatív gyógymódról nem tudták eddig kimutatni, hogy javulást okozott a hepatitis C fertőzés kimenetelében, és nincs bizonyíték arra, hogy az alternatív gyógymódok hatnának egyáltalán a vírusra.[52][53][54]
Kilátások[szerkesztés]
A kezelésre adott válasz genotípusonként változik. A HCV 1-es genotípussal fertőzöttek esetében a 48 hetes kezelés alatt elért tartós vírusválasz 40 és 50% közötti.[5] A 2-es és 3-as genotípussal fertőzött betegek esetében a 24 hetes kezelést követően 70 és 80% közötti tartós vírusválasz figyelhető meg.[5] A 4-es genotípussal fertőzötteknél a 48 hetes kezelést követően a tartós vírusválasz 65%. Jelenleg a 6-os genotípus okozta megbetegedésnél alkalmazott kezelésről nincsenek konkrét bizonyítékok; az eddigi bizonyítékok a 48 hetes kezelésre vonatkoznak, amely megegyezik az 1-es genotípus által okozott betegség esetén alkalmazott adaggal.[55]
Epidemiológia[szerkesztés]

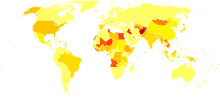
130 - 170 millió személy, azaz a világ népességének megközelítően 3%-a krónikus hepatitis C fertőzéssel él.[56] Évente 3 és 4 millió közötti személy fertőződik meg és több mint 350 000-en halnak meg hepatitis C-vel kapcsolatos betegségben.[56] A 20. században az intravénás droghasználat és az intravénás gyógyszerek alkalmazása, valamint a nem sterilizált orvosi eszközök használata következtében az arány jelentősen megnövekedett.[14]
Az Egyesült Államokban a népesség 2%-a hepatitis C-fertőzött,[7] és évente 35 000 és 185 000 fő közötti új esetet jegyeznek fel. Az arány csökkent annak köszönhetően, hogy Nyugaton javult a vérátömlesztés előtti szűrés az 1990-es években.[15] Az Egyesült Államokban évente 8000 és 10 000 közötti személy hal meg HCV-fertőzésben. Ez a halálozási arány várhatóan növekedni fog, mivel a HCV vizsgálat előtt a vérátömlesztéssel fertőzött személyek megbetegednek és meghalnak.[57]
Magyarországon a vírushordozók aránya 0,7 - 1,3%-ra tehető, és a HCV vírus okozta krónikus fertőzést évente 2000 - 4000 májzsugor kialakulásával és 600 májrákos esettel hozzák összefüggésbe.[12]
Egyes afrikai és ázsiai országokban a fertőzés gyakorisága magasabb.[58] A legmagasabb fertőzési gyakorisággal rendelkező országok Egyiptom (22%), Pakisztán (4,8%) és Kína (3,2%).[56] Az egyiptomi magas arány összefüggésbe hozható a mára már beszüntetett vérmételyfertőzés kampányszerű tömeges kezelésével, amelynek során nem megfelelően sterilizált üvegfecskendőket használtak.[14]
A vírus felfedezésének története[szerkesztés]
Az 1970-es évek közepén Harvey J. Alter,[59] az egyesült államokbeli Nemzeti Egészségügyi Intézet Transzfúziós osztálya Fertőző betegségek részlegének főorvosa, és kutatócsoportja kimutatta, hogy a legtöbb vérátömlesztést követő hepatitis esetet nem a hepatitis A- vagy B-vírus okozza (a betegséget ekkor non-A non-B hepatitis-nek - rövidítése NANB - nevezték el). A felfedezés ellenére a következő évtizedben a vírus azonosítását célzó nemzetközi kutatások nem jártak eredménnyel. 1987-ben Michael Houghton, Qui-Lim Choo és George Kuo a Chiron Corporation alkalmazottai és Dr. D.W. Bradley, az USA-beli Betegségfelügyeleti Központ munkatársának közreműködésével az ismeretlen organizmus azonosítására új molekuláris klónozást alkalmaztak és diagnosztizáló tesztet fejlesztettek ki.[60] 1988-ban Alter megerősítette a vírus létezését azáltal, hogy nem-A és nem-B Hepatitis-mintasorozatokat tartalmazó tálcán kimutatja a vírus jelenlétét. 1989 áprilisában a Science két cikkében közölték a HCV felfedezését.[61][62] A felfedezés eredményeként jelentősen javult a diagnosztizálás esélyei és a vírusellenes kezelések hatékonysága.[60] 2000-ben Dr. Altert és Dr. Houghtont a klinikai orvosi kutatások Albert Lasker-díj[63] ával tüntették ki „a hepatitis C-t okozó vírus felfedezéséért tett úttörő munkájukért, valamint a szűrési eljárások kifejlesztéséért, amely következtében az Egyesült Államokban a vérátömlesztéssel kapcsolatos fertőzések kockázata 1970-ben 30%-ról 2000-ben gyakorlatilag nullára csökkent.”[64]
A Chiron számos szabadalmi kérelmet nyújtott be a vírussal és diagnosztizálásával kapcsolatban.[65] 1990-ben ejtettek egy, a Betegségfelügyeleti Központ által benyújtott konkurens szabadalmi kérelmet, miután Chiron a Betegségfelügyeleti Központnak 1,9 millió, Bradleynek pedig 337 500 dollárt fizetett. 1994-ben Bradley beperelte a Chiront, a szabadalom hatályon kívüli helyezését követelve, önmagát társfeltalálónak foglalta bele a kérelembe és kártérítést, valamint jogdíjbevételt kért. Miután a fellebbviteli bíróságon elvesztette a pert, 1998-ban ejtette a keresetet.[66]
2020-ban Harvey Alternek, Michael Houghtonnak and Charles Rice-nak ítélték az fiziológiai és orvostudományi Nobel-díjat a vírus felfedezéséért.[67]
Társadalom és kultúra[szerkesztés]
A Hepatitis Világszövetség minden év július 28-án rendezi meg a Hepatitis világnapot.[68] A hepatitis C jelentős gazdasági terhet ró az egyénre és a társadalomra egyaránt. Az Egyesült Államokban a betegség átlagos, egész életre szóló költségét 33 407 dollárra becsülték 2003-ban,[69] amely 2011-ben a májátültetés költségével együtt megközelítően 200 000 dollárt tett ki.[70] Kanadában egy vírus elleni kezeléssorozat ára 2003-ban 30 000 dollár volt,[71] míg 1998-ban az Egyesült Államokban a költségek 9200 és 17 600 dollár közé tehetőek.[69] A világ sok részén az emberek nem engedhetik meg maguknak a vírus elleni kezelést, mivel nincs biztosításuk vagy ha van is, az nem terjed ki a vírus elleni gyógyszerekre.[72]
Kutatás[szerkesztés]
2011-ben a Hepatitis C okozta megbetegedés kezelésére hozzávetőleg száz gyógyszer állt fejlesztés alatt.[70] A gyógyszerek közé tartoznak a hepatitis-védőoltások, az immunomodulátorok és a ciklofilin-gátlók.[73] Ezek a potenciálisan új kezelési módok a hepatitis C-vírus alaposabb megismerésének köszönhetően jöttek létre.[74]
Jegyzetek[szerkesztés]
- ↑ Alacsonyküszöbű ellátási formák (magyar nyelven). Droginfo.hu. [2013. április 13-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. október 18.)
- ↑ a b szerk.: Ryan KJ, Ray CG (editors): Sherris Medical Microbiology, 4th, McGraw Hill, 551–2. o. (2004). ISBN 0838585299
- ↑ Máriáss Márta: Hepatitis C. Házipatika.com. (Hozzáférés: 2012. október 18.)
- ↑ Houghton M (2009. November). „The long and winding road leading to the identification of the hepatitis C virus”. Journal of Hepatology 51 (5), 939–48. o. DOI:10.1016/j.jhep.2009.08.004. PMID 19781804.
- ↑ a b c d e f g h i j k Rosen, HR (2011. június 23.). „Clinical practice. Chronic hepatitis C infection.”. The New England journal of medicine 364 (25), 2429–38. o. [2012. december 15-i dátummal az eredetiből archiválva]. PMID 21696309. (Hozzáférés: 2012. június 20.)
- ↑ Maheshwari, A, Ray, S, Thuluvath, PJ (2008. július 26.). „Acute hepatitis C.”. Lancet 372 (9635), 321–32. o. DOI:10.1016/S0140-6736(08)61116-2. PMID 18657711.
- ↑ a b c d e f g h i j k l m n o p q r s t u v Wilkins, T, Malcolm, JK, Raina, D, Schade, RR (2010. június 1.). „Hepatitis C: diagnosis and treatment.”. American family physician 81 (11), 1351–7. o. PMID 20521755.
- ↑ a b c d e Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future.. Springer Verlag, 4. o. (2011). ISBN 9781461411918
- ↑ a b c d Nelson, PK, Mathers, BM, Cowie, B, Hagan, H, Des Jarlais, D, Horyniak, D, Degenhardt, L (2011. augusztus 13.). „Global epidemiology of hepatitis B and hepatitis C in people who inject drugs: results of systematic reviews.”. Lancet 378 (9791), 571–83. o. DOI:10.1016/S0140-6736(11)61097-0. PMID 21802134.
- ↑ a b c d Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future.. Springer Verlag, 103–104. o. (2011). ISBN 9781461411918
- ↑ a b c d e f g Dolin, [edited by] Gerald L. Mandell, John E. Bennett, Raphael. Mandell, Douglas, and Bennett's principles and practice of infectious diseases, 7th ed., Philadelphia, PA: Churchill Livingstone/Elsevier, Chapter 154. o. (2010). ISBN 978-0443068393
- ↑ a b c Hepatitis C: tünetei és kezelése. (Hozzáférés: 2012. június 21.)
- ↑ Mueller, S, Millonig, G, Seitz, HK (2009. július 28.). „Alcoholic liver disease and hepatitis C: a frequently underestimated combination.”. World journal of gastroenterology : WJG 15 (28), 3462–71. o. PMID 19630099.
- ↑ a b c d e f g h i j Alter, MJ (2007. május 7.). „Epidemiology of hepatitis C virus infection.”. World journal of gastroenterology : WJG 13 (17), 2436–41. o. PMID 17552026.
- ↑ a b c d e Ozaras, R, Tahan, V (2009. április 1.). „Acute hepatitis C: prevention and treatment.”. Expert review of anti-infective therapy 7 (3), 351–61. o. PMID 19344247.
- ↑ Non-Hodgkin limfóma (magyar nyelven). Daganatok.hu. (Hozzáférés: 2012. október 19.)
- ↑ Zignego AL, Ferri C, Pileri SA, Caini P, Bianchi FB (2007. January). „Extrahepatic manifestations of Hepatitis C Virus infection: a general overview and guidelines for a clinical approach”. Digestive and Liver Disease 39 (1), 2–17. o. DOI:10.1016/j.dld.2006.06.008. PMID 16884964.
- ↑ Louie, KS, Micallef, JM, Pimenta, JM, Forssen, UM (2011. január 1.). „Prevalence of thrombocytopenia among patients with chronic hepatitis C: a systematic review.”. Journal of viral hepatitis 18 (1), 1–7. o. PMID 20796208.
- ↑ Lee, MR, Shumack, S (2005. November). „Prurigo nodularis: a review”. The Australasian journal of dermatology 46 (4), 211–18; quiz 219–20. o. DOI:10.1111/j.1440-0960.2005.00187.x. PMID 16197418.
- ↑ David C. Dugdale, Herbert Y. Lin, David Zieve: Membranoproliferative glomerulonephritis (angol nyelven). Medline Plus Medical Encyclopedia, 2012. (Hozzáférés: 2012. október 19.)
- ↑ Zak K. Shihabi (2006). „Cryoglobulins: An Important but Neglected Clinical Test” (angol nyelven). Annals of Clinical & Laboratory Science. (Hozzáférés: 2012. október 19.)
- ↑ (2010. May) „Management of hepatitis C virus-related mixed cryoglobulinemia”. Am. J. Med. 123 (5), 400–8. o. DOI:10.1016/j.amjmed.2009.09.038. PMID 20399313.
- ↑ Nakano T, Lau GM, Lau GM, Sugiyama M, Mizokami M (2011. December). „An updated analysis of hepatitis C virus genotypes and subtypes based on the complete coding region”. Liver Int.. DOI:10.1111/j.1478-3231.2011.02684.x. PMID 22142261.
- ↑ Maheshwari, A, Thuluvath, PJ (2010. február 1.). „Management of acute hepatitis C.”. Clinics in liver disease 14 (1), 169–76; x. o. PMID 20123448.
- ↑ a b c d e Pondé, RA, Mikhaĭlova, A (2011. február 1.). „Hidden hazards of HCV transmission.”. Medical microbiology and immunology 200 (1), 7–11. o. PMID 20461405.
- ↑ a b Xia, X, Luo, J, Bai, J, Yu, R (2008. október 1.). „Epidemiology of HCV infection among injection drug users in China: systematic review and meta-analysis.”. Public health 122 (10), 990–1003. o. DOI:10.1016/j.puhe.2008.01.014. PMID 18486955.
- ↑ Imperial, JC (2010. június 1.). „Chronic hepatitis C in the state prison system: insights into the problems and possible solutions.”. Expert review of gastroenterology & hepatology 4 (3), 355–64. o. PMID 20528122.
- ↑ Vescio, MF, Longo, B, Babudieri, S, Starnini, G, Carbonara, S, Rezza, G, Monarca, R (2008. április 1.). „Correlates of hepatitis C virus seropositivity in prison inmates: a meta-analysis.”. Journal of epidemiology and community health 62 (4), 305–13. o. PMID 18339822.
- ↑ Marx, John. Rosen's emergency medicine: concepts and clinical practice 7th edition. Philadelphia, PA: Mosby/Elsevier, 1154. o. (2010). ISBN 9780323054720
- ↑ Highest Rates of Hepatitis C Virus Transmission Found in Egypt. Al Bawaba, 2010. augusztus 9. [2012. május 15-i dátummal az eredetiből archiválva]. (Hozzáférés: 2010. augusztus 27.)
- ↑ Győrfi Adrienne, Fazekas Árpád (2007). „Az infekciókontroll jelentősége a fogászatban(Összefoglaló referátum)” (magyar nyelven). Fogorvosi Szemle 100 (4), 141-152. o, Kiadó: Semmelweis Egyetem, Konzerváló Fogászati Klinika, Budapest. (Hozzáférés: 2012. október 20.)
- ↑ Mihály Ilona: Az egészségügyi dolgozók hepatitis veszélyeztetettsége - A vérrel átvihetô vírusok és a kockázatot befolyásoló tényezôk (magyar nyelven). HIPPOCRATES. [2012. október 14-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. október 20.)
- ↑ a b c Tohme RA, Holmberg SD (2010. June). „Is sexual contact a major mode of hepatitis C virus transmission?”. Hepatology 52 (4), 1497–505. o. DOI:10.1002/hep.23808. PMID 20635398.
- ↑ Hepatitis C Group Education Class. United States Department of Veteran Affairs
- ↑ a b c d e f Jafari, S, Copes, R, Baharlou, S, Etminan, M, Buxton, J (2010. november 1.). „Tattooing and the risk of transmission of hepatitis C: a systematic review and meta-analysis.”. International journal of infectious diseases : IJID : official publication of the International Society for Infectious Diseases 14 (11), e928-40. o. PMID 20678951.
- ↑ Hepatitis C. Center for Disease Control and Prevention. (Hozzáférés: 2012. január 2.)
- ↑ Lock G, Dirscherl M, Obermeier F, et al. (2006. September). „Hepatitis C —contamination of toothbrushes: myth or reality?”. J. Viral Hepat. 13 (9), 571–3. o. DOI:10.1111/j.1365-2893.2006.00735.x. PMID 16907842.
- ↑ a b c Hepatitis C. FAQ – CDC Viral Hepatitis. (Hozzáférés: 2012. január 2.)
- ↑ a b Lam, NC, Gotsch, PB, Langan, RC (2010. november 15.). „Caring for pregnant women and newborns with hepatitis B or C.”. American family physician 82 (10), 1225–9. o. PMID 21121533.
- ↑ Mast EE (2004). „Mother-to-infant hepatitis C virus transmission and breastfeeding”. Advances in Experimental Medicine and Biology 554, 211–6. o. PMID 15384578.
- ↑ Senadhi, V (2011. július 1.). „A paradigm shift in the outpatient approach to liver function tests.”. Southern medical journal 104 (7), 521–5. o. PMID 21886053.
- ↑ Centers for Disease Control and Prevention (CDC) (May 18, 2012). "CDC Announces First Ever National Hepatitis Testing Day and Proposes that All Baby Boomers Be Tested Once for Hepatitis C". Sajtóközlemény. Elérés: 2012-06-21.
- ↑ Halliday, J, Klenerman, P, Barnes, E (2011. május 1.). „Vaccination for hepatitis C virus: closing in on an evasive target”. Expert review of vaccines 10 (5), 659–72. o. DOI:10.1586/erv.11.55. PMID 21604986.
- ↑ Hagan, H, Pouget, ER, Des Jarlais, DC (2011. július 1.). „A systematic review and meta-analysis of interventions to prevent hepatitis C virus infection in people who inject drugs.”. The Journal of infectious diseases 204 (1), 74–83. o. PMID 21628661.
- ↑ Torresi, J, Johnson, D, Wedemeyer, H (2011. június 1.). „Progress in the development of preventive and therapeutic vaccines for hepatitis C virus.”. Journal of hepatology 54 (6), 1273–85. o. DOI:10.1016/j.jhep.2010.09.040. PMID 21236312.
- ↑ Ilyas, JA, Vierling, JM (2011. augusztus 1.). „An overview of emerging therapies for the treatment of chronic hepatitis C.”. Clinics in liver disease 15 (3), 515–36. o. PMID 21867934.
- ↑ Information about Ribavirin (angol nyelven). About.com - Hepatitis. [2013. január 16-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. október 19.)
- ↑ Foote BS, Spooner LM, Belliveau PP (2011. September). „Boceprevir: a protease inhibitor for the treatment of chronic hepatitis C”. Ann Pharmacother 45 (9), 1085–93. o. DOI:10.1345/aph.1P744. PMID 21828346.
- ↑ Smith LS, Nelson M, Naik S, Woten J (2011. May). „Telaprevir: an NS3/4A protease inhibitor for the treatment of chronic hepatitis C”. Ann Pharmacother 45 (5), 639–48. o. DOI:10.1345/aph.1P430. PMID 21558488.
- ↑ Ghany MG, Nelson DR, Strader DB, Thomas DL, Seeff LB (2011. October). „An update on treatment of genotype 1 chronic hepatitis C virus infection: 2011 practice guideline by the American Association for the Study of Liver Diseases”. Hepatology 54 (4), 1433–44. o. DOI:10.1002/hep.24641. PMID 21898493.
- ↑ Alavian SM, Tabatabaei SV (2010. April). „Treatment of chronic hepatitis C in polytransfused thalassaemic patients: a meta-analysis”. J. Viral Hepat. 17 (4), 236–44. o. DOI:10.1111/j.1365-2893.2009.01170.x. PMID 19638104.
- ↑ a b Hepatitis C and CAM: What the Science Says. NCCAM, 2011. March. [2013. május 13-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. augusztus 7.)
- ↑ Liu, J, Manheimer, E, Tsutani, K, Gluud, C (2003. március 1.). „Medicinal herbs for hepatitis C virus infection: a Cochrane hepatobiliary systematic review of randomized trials.”. The American journal of gastroenterology 98 (3), 538–44. o. PMID 12650784.
- ↑ Rambaldi, A, Jacobs, BP, Gluud, C (2007. október 17.). „Milk thistle for alcoholic and/or hepatitis B or C virus liver diseases.”. Cochrane database of systematic reviews (Online) (4), CD003620. o. PMID 17943794.
- ↑ Fung J, Lai CL, Hung I, et al. (2008. September). „Chronic hepatitis C virus genotype 6 infection: response to pegylated interferon and ribavirin”. The Journal of Infectious Diseases 198 (6), 808–12. o. DOI:10.1086/591252. PMID 18657036.
- ↑ a b c WHO Hepatitis C factsheet, 2011. (Hozzáférés: 2011. július 13.)
- ↑ Colacino, ed. by J. M., Heinz, B. A.. Hepatitis prevention and treatment. Basel: Birkhäuser, 32. o. (2004). ISBN 9783764359560
- ↑ al.], edited by Gary W. Brunette ... [et. CDC health information for international travel : the Yellow Book 2012. New York: Oxford University, 231. o.. ISBN 9780199769018
- ↑ Harvey Alter, MD; Senior Staff (angol nyelven). NIH Clinical Center. [2012. október 27-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. október 19.)
- ↑ a b Boyer, JL. Liver cirrhosis and its development: proceedings of the Falk Symposium 115. Springer Science+Business Media/Springer, 344. o. (2001). ISBN 9780792387602
- ↑ Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M (1989. April). „Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome”. Science 244 (4902), 359–62. o. DOI:10.1126/science.2523562. PMID 2523562.
- ↑ Kuo G, Choo QL, Alter HJ, et al. (1989. April). „An assay for circulating antibodies to a major etiologic virus of human non-A, non-B hepatitis”. Science 244 (4902), 362–4. o. DOI:10.1126/science.2496467. PMID 2496467.
- ↑ Albert és Mary Lasker nevét viselő alapítvány díja - a "Nobel-díj előszobája" (angol nyelven). [2016. március 4-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. október 19.)
- ↑ 2000 Winners Albert Lasker Award for Clinical Medical Research. The Lasker Foundation.. [2008. február 25-i dátummal az eredetiből archiválva]. (Hozzáférés: 2015. március 14.)
- ↑ Houghton, M., Q.-L. Choo, and G. Kuo. NANBV Diagnostics and Vaccines. European Patent No. EP-0-3 18-216-A1. European Patent Office (filed 18 November 1988, published 31 May 1989).
- ↑ Wilken, Judge: United States Court of Appeals for the Federal Circuit. United States Court of Appeals for the Federal Circuit. (Hozzáférés: 2012. január 11.)
- ↑ The Nobel Prize in Physiology or Medicine 2020. The Nobel Prize in Physiology or Medicine, 2020. október 5. (Hozzáférés: 2020. október 5.)
- ↑ Eurosurveillance editorial, team (2011. július 28.). „World Hepatitis Day 2011.”. Euro surveillance : bulletin europeen sur les maladies transmissibles = European communicable disease bulletin 16 (30). PMID 21813077.
- ↑ a b Wong, JB (2006). „Hepatitis C: cost of illness and considerations for the economic evaluation of antiviral therapies.”. PharmacoEconomics 24 (7), 661–72. o. PMID 16802842.
- ↑ a b El Khoury, A. C., Klimack, W. K., Wallace, C., Razavi, H. (2011. december 1.). „Economic burden of hepatitis C-associated diseases in the United States”. Journal of Viral Hepatitis. DOI:10.1111/j.1365-2893.2011.01563.x.
- ↑ Hepatitis C Prevention, Support and Research ProgramHealth Canada. Public Health Agency of Canada, 2003. Nov. (Hozzáférés: 2012. január 10.)
- ↑ Zuckerman, edited by Howard Thomas, Stanley Lemon, Arie. Viral Hepatitis., 3rd ed., Oxford: John Wiley & Sons, 532. o. (2008). ISBN 9781405143882
- ↑ Ahn, J, Flamm, SL (2011. augusztus 1.). „Hepatitis C therapy: other players in the game”. Clinics in liver disease 15 (3), 641–56. o. DOI:10.1016/j.cld.2011.05.008. PMID 21867942.
- ↑ Vermehren, J, Sarrazin, C (2011. február 1.). „New HCV therapies on the horizon.”. Clinical microbiology and infection : the official publication of the European Society of Clinical Microbiology and Infectious Diseases 17 (2), 122–34. o. PMID 21087349.
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben a Hepatitis C című egyszerűsített angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
További információk[szerkesztés]
- Hepatitis C a hazipatika.com oldalon
- Hogyan győzhető le a hepatitis C?
- Újfajta gyógyszert engedélyeztek a hepatitis C gyógyítására
- Hepatitis C - a betegséggel és a gyógymódokkal foglalkozó blog
- Hepatitis C a Magyar Hemofília Egyesület oldalán
- Fontos tudnivalók a Hepatitis C-ről a Munkahet.hu magazinon
Kapcsolódó szócikkek[szerkesztés]
| Az itt található információk kizárólag tájékoztató jellegűek, nem minősülnek orvosi szakvéleménynek, nem pótolják az orvosi kivizsgálást és kezelést. A cikk tartalmát a Wikipédia önkéntes szerkesztői alakítják ki, és bármikor módosulhat. |

