„Petefészekrák” változatai közötti eltérés
| [ellenőrzött változat] | [ellenőrzött változat] |
Nincs szerkesztési összefoglaló |
Nincs szerkesztési összefoglaló |
||
| 131. sor: | 131. sor: | ||
[[Fájl:Scheme hysterectomy-de.svg|bélyegkép|jobbra|200px|A hiszterektómia sémás képe]] |
[[Fájl:Scheme hysterectomy-de.svg|bélyegkép|jobbra|200px|A hiszterektómia sémás képe]] |
||
A gyermekes nők kevésbé vannak kitéve a petefészekráknak, mint a gyermektelenek. A szoptatás szintén csökkenti bizonyos petefészekrák típusok kockázatát. A petevezeték lekötése és a méh eltávolítása ''(hysterectomia)'' csökkenti a kockázatot, a kétoldali petevezeték és petefészek eltávolítása ''(bilaterális salpingo-oophorectomy)'' pedig drámaian csökkenti nem csupán a petefészekrák, de a mellrák kockázatát is.<ref>{{cite journal|author=Finch A, Beiner M, Lubinski J, et al.:|title="Salpingo-oophorectomy and the risk of ovarian, fallopian tube, and peritoneal cancers in women with a BRCA1 or BRCA2 Mutation"|journal=JAMA |volume=296|issue=2|pages=185–92| doi:10.1001/jama.296.2.185.|year=2006|Month=July|PMID=16835424|url= http://jama.ama-assn.org/cgi/pmidlookup?view=long&pmid=16835424.}}</ref> A petefészkek és a méh együttes eltávolítása egyharmadára csökkentik a petefészekrák kifejlődésének kockázatát,<ref>{{cite web|title="What are the risk factors for ovarian cancer?"|url=http://www.cancer.org/cancer/ovariancancer/detailedguide/ovarian-cancer-risk-factors.|accesdate=2011-08-18}}</ref> ugyanakkor nem növekszik a más típusú rákok, a szívbetegségek vagy a combnyaktörések kockázata, amint azt az University of California San Franciscoi részlegéből publikálták az Archives of Internal Medicine-ben.<ref>{{cite web|publisher=Univ California|title="Ektomy"|url=http://www.medicalnewstoday.com/articles/223544.php}}</ref> A Lancet egy közleménye arra utal, hogy az örökletes petefészekrák kockázatát a méhkürt lekötése 72%-al csökkenti a BRCA1 gént hordozó nőkben.<ref>{{cite web|title="Fallopian"|url=http://scienceblog.com/community/older/2001/E/200115711.html}}</ref> Az orális fogamzásgátlók ''(születésszabályozó tabletták)'' öt vagy több éven át szedve 50%-al csökkentik a veleszületett petefészekrák kockázatát az idősebb nőknél.<ref>Bast RC, Brewer M, Zou C, et al. |
A gyermekes nők kevésbé vannak kitéve a petefészekráknak, mint a gyermektelenek. A szoptatás szintén csökkenti bizonyos petefészekrák típusok kockázatát. A petevezeték lekötése és a méh eltávolítása ''(hysterectomia)'' csökkenti a kockázatot, a kétoldali petevezeték és petefészek eltávolítása ''(bilaterális salpingo-oophorectomy)'' pedig drámaian csökkenti nem csupán a petefészekrák, de a mellrák kockázatát is.<ref>{{cite journal|author=Finch A, Beiner M, Lubinski J, et al.:|title="Salpingo-oophorectomy and the risk of ovarian, fallopian tube, and peritoneal cancers in women with a BRCA1 or BRCA2 Mutation"|journal=JAMA |volume=296|issue=2|pages=185–92| doi:10.1001/jama.296.2.185.|year=2006|Month=July|PMID=16835424|url= http://jama.ama-assn.org/cgi/pmidlookup?view=long&pmid=16835424.}}</ref> A petefészkek és a méh együttes eltávolítása egyharmadára csökkentik a petefészekrák kifejlődésének kockázatát,<ref>{{cite web|title="What are the risk factors for ovarian cancer?"|url=http://www.cancer.org/cancer/ovariancancer/detailedguide/ovarian-cancer-risk-factors.|accesdate=2011-08-18}}</ref> ugyanakkor nem növekszik a más típusú rákok, a szívbetegségek vagy a combnyaktörések kockázata, amint azt az University of California San Franciscoi részlegéből publikálták az Archives of Internal Medicine-ben.<ref>{{cite web|publisher=Univ California|title="Ektomy"|url=http://www.medicalnewstoday.com/articles/223544.php}}</ref> A Lancet egy közleménye arra utal, hogy az örökletes petefészekrák kockázatát a méhkürt lekötése 72%-al csökkenti a BRCA1 gént hordozó nőkben.<ref>{{cite web|title="Fallopian"|url=http://scienceblog.com/community/older/2001/E/200115711.html}}</ref> Az orális fogamzásgátlók ''(születésszabályozó tabletták)'' öt vagy több éven át szedve 50%-al csökkentik a veleszületett petefészekrák kockázatát az idősebb nőknél.<ref>{{cite journal|author=Bast RC, Brewer M, Zou C, et al.:|title="Prevention and early detection of ovarian cancer: mission impossible?"|journal=Recent Results Cancer Res|year=2007|volume=174|page=91–100| doi:10.1007/978-3-540-37696-5_9. |PMID=17302189}}</ref> |
||
== Diagnózis == |
== Diagnózis == |
||
| 140. sor: | 140. sor: | ||
A szérum BHCG (a [[Méhlepény|vér human chorion gonadotropin hormon]] szintjét meg kell határozni minden olyan nőnél, akinél a terhesség lehetősége fennáll. Ezen túlmenően a szérum [[Down-szindróma|alfa-fetoprotein]] (AFP) és [[Enzim|''laktát-dehidrogenáz'']] (LDH) szint meghatározandó petefészek tumor gyanús fiatal és serdülőkorú lányokon, mivel minél fiatalabb a páciens, annál nagyobb a valószínűsége egy rosszindulatú csírasejt daganatnak. |
A szérum BHCG (a [[Méhlepény|vér human chorion gonadotropin hormon]] szintjét meg kell határozni minden olyan nőnél, akinél a terhesség lehetősége fennáll. Ezen túlmenően a szérum [[Down-szindróma|alfa-fetoprotein]] (AFP) és [[Enzim|''laktát-dehidrogenáz'']] (LDH) szint meghatározandó petefészek tumor gyanús fiatal és serdülőkorú lányokon, mivel minél fiatalabb a páciens, annál nagyobb a valószínűsége egy rosszindulatú csírasejt daganatnak. |
||
Ha a [[Daganat|rosszindulatú petefészek-daganat]] diagnosztikai valószínűsége fennáll, bizonyos laboratóriumi vizsgálatok elvégzése szükséges. A [[Vér|teljes vérkép]] és a [[Elektrolit|szérum elektrolit]] vizsgálat minden páciensnél elvégzendő. A CA-125 elnevezésű marker vérvizsgálata hasznos az elkülönítő diagnózishoz és a betegség követéséhez, de önmagában nem elég hatékony módszer a petefészekrák korai stádiumainak követéséhez, mert ehhez az érzékenysége és specifikussága nem elegendő. |
Ha a [[Daganat|rosszindulatú petefészek-daganat]] diagnosztikai valószínűsége fennáll, bizonyos laboratóriumi vizsgálatok elvégzése szükséges. A [[Vér|teljes vérkép]] és a [[Elektrolit|szérum elektrolit]] vizsgálat minden páciensnél elvégzendő. A CA-125 elnevezésű marker vérvizsgálata hasznos az elkülönítő diagnózishoz és a betegség követéséhez, de önmagában nem elég hatékony módszer a petefészekrák korai stádiumainak követéséhez, mert ehhez az érzékenysége és specifikussága nem elegendő. |
||
Az új teszt, amit az FDA "(US Food and Drug Administration)" |
Az új teszt, amit az FDA "(US Food and Drug Administration)" 2011-ben hagyott jóvá, az OVA1 felülmúlja a petefészekrák észlelésében a CA125 vértvizsgálattal kombinált klinikai értékelést. 2011 júniusában egy, az Obstetrics & Gynecology-ban publikált cikkben leírták, hogy az OVA1 kombinálása egy preoperatív orvosi vizsgálattal biztosabban képes kimutatni egy nő petefészek-szövetszaporulatáról, hogy petefészekrákról vagy petefészekkel kapcsolatos rákról van-e szó, mint egy preoperatív orvosi vizsgálat önmagában.<ref>{{Rossing, Mary Anne; Wicklund, Kristine G.; Cushing-Haugen, Kara L.; Weiss, Noel S. (2010-01-28). "Predictive Value of Symptoms for Early Detection of Ovarian Cancer". J Natl Cancer Inst. 102 (4): djp500v1. doi:10.1093/jnci/djp500. PMC 2826180. PMID 20110551. http://jnci.oxfordjournals.org/cgi/content/full/djp500v1</ref>. |
||
Az OVA1 csak az olyan 18 évet betöltött nőknek javasolt, akit már műtétre kiválasztottak a kismedencei szövetburjánzásuk miatt. Nem szánják a petefészekrák szűrésére, vagy a petefészekrák végleges diagnózisának megállapítására. Az OVA1-et a Johan Hopkins Egyetem (Baltimore) kutatói fejlesztették ki.<ref>FDA Clears a Test for Ovarian Cancer</ref>. |
Az OVA1 csak az olyan 18 évet betöltött nőknek javasolt, akit már műtétre kiválasztottak a kismedencei szövetburjánzásuk miatt. Nem szánják a petefészekrák szűrésére, vagy a petefészekrák végleges diagnózisának megállapítására. Az OVA1-et a Johan Hopkins Egyetem (Baltimore) kutatói fejlesztették ki.<ref>FDA Clears a Test for Ovarian Cancer</ref>. |
||
A folyamatban lévő vizsgálatokban keresik annak a módját, hogyan kombinálhatók a tumor marker fehérjék a betegség más jelzőivel (pl. a radiológiai vagy más tünetekkel), hogy a pontosságot javítsák. Ennek a megközelítésnek az a nehézsége, hogy a petefészekrák egyenetlen előfordulási gyakorisága miatt még a nagy érzékenységű és fajlagosságú tesztek is számos fals pozitivitást eredményeznek (azaz olyan esetekben is sebészeti beavatkozásra kerülhet sor, amikor végül is a műtét során nem találnak rosszindulatú daganatot.) A fehérje természetű jelzőanyagok felhasználása azonban még korai szakaszában van, és további finomítást igényel. A fehérje természetű jelzőanyagok vizsgálatának jelenlegi helyzete viszont azt is jelzi, hogy a terápiás elvek az egyénre szabott eljárások felé tolódik el.<ref>{{cite book|author=Dunn, J. D. (Ed.)| title=Associated Title(s): PROTEOMICS – Clinical Applications|publisher=Online ISSN: 1615-9861|Vol. 11|issue=15|url| year=|doi= }}</ref> |
A folyamatban lévő vizsgálatokban keresik annak a módját, hogyan kombinálhatók a tumor marker fehérjék a betegség más jelzőivel (pl. a radiológiai vagy más tünetekkel), hogy a pontosságot javítsák. Ennek a megközelítésnek az a nehézsége, hogy a petefészekrák egyenetlen előfordulási gyakorisága miatt még a nagy érzékenységű és fajlagosságú tesztek is számos fals pozitivitást eredményeznek (azaz olyan esetekben is sebészeti beavatkozásra kerülhet sor, amikor végül is a műtét során nem találnak rosszindulatú daganatot.) A fehérje természetű jelzőanyagok felhasználása azonban még korai szakaszában van, és további finomítást igényel. A fehérje természetű jelzőanyagok vizsgálatának jelenlegi helyzete viszont azt is jelzi, hogy a terápiás elvek az egyénre szabott eljárások felé tolódik el.<ref>{{cite book|author=Dunn, J. D. (Ed.)| title=Associated Title(s): PROTEOMICS – Clinical Applications|publisher=Online ISSN: 1615-9861|Vol. 11|issue=15|url| year=|doi= }}</ref> |
||
| 345. sor: | 345. sor: | ||
[[Fájl:Most common cancers - female, by mortality.png|thumb|Mortalitás szerint.<ref name=Jemal/>]] |
[[Fájl:Most common cancers - female, by mortality.png|thumb|Mortalitás szerint.<ref name=Jemal/>]] |
||
A betegség általánosabb az iparilag fejlett nemzeteknél, kivéve Japánt. Az Egyesült Államokban a nők 1,4-2,5%-ának (egynek 40-60 közül) van esélye arra, hogy élete folyamán petefészekrák alakuljon ki nála. Az idősebb nőknél a kockázat nagyobb.<ref>{{cite web|title=Ovarian cancer symptoms, early warning signs, and risk factors|journal=MedicineNet.com|url=http://www.genetichealth.com|author=Stöppler, Melissa Conrad; Lee, Dennis; Shiel, William C. Jr., MD, FACP, FACR|accessdate=08 August 2011}}</ref> A petefészekrák okozta elhalálozások több mint fele az 55 és 74 éves életkor közötti nőknél következik be, és mintegy negyede a 35 és 54 éves életkorok között. |
A betegség általánosabb az iparilag fejlett nemzeteknél, kivéve Japánt. Az Egyesült Államokban a nők 1,4-2,5%-ának (egynek 40-60 közül) van esélye arra, hogy élete folyamán petefészekrák alakuljon ki nála. Az idősebb nőknél a kockázat nagyobb.<ref>{{cite web|title="Ovarian cancer symptoms, early warning signs, and risk factors"|journal=MedicineNet.com|url=http://www.genetichealth.com|author=Stöppler, Melissa Conrad; Lee, Dennis; Shiel, William C. Jr., MD, FACP, FACR|accessdate=08 August 2011}}</ref> A petefészekrák okozta elhalálozások több mint fele az 55 és 74 éves életkor közötti nőknél következik be, és mintegy negyede a 35 és 54 éves életkorok között. |
||
Az [[Amerikai Egyesült Államok]]ban a statisztikák szerint 2010-ben {{szám|21880}} új esetet diagnosztizáltak és {{szám|13850}} nő halt meg petefészekrákban. A kockázat az életkorral nő, a terhességek számának növekedésével viszont csökken. Az életkori kockázat 1,6% körül van, de azoknál a nőknél, akiknél közvetlen rokonok érintettek ez az arány 5%-os. Azoknál a nőknél, akiknél a BRCA1 vagy a BRCA2 gének estek át mutáción, a kockázat 25% és 60% között van, attól függően, hogy a mutáció mennyire volt specifikus.<ref>{{cite book |author=Robert C. Young |chapter=Ch. 83, Gynecologic Malignancies |editor=Jameson JN, Kasper DL, Harrison TR, Braunwald E, Fauci AS, Hauser SL, Longo DL |title=Harrison's principles of internal medicine|publisher=McGraw-Hill Medical Publishing Division |location=New York |year=2005 |edition=16th |isbn=0-07-140235-7 |url=http://highered.mcgraw-hill.com/sites/0071402357/information_center_view0/}}</ref> |
Az [[Amerikai Egyesült Államok]]ban a statisztikák szerint 2010-ben {{szám|21880}} új esetet diagnosztizáltak és {{szám|13850}} nő halt meg petefészekrákban. A kockázat az életkorral nő, a terhességek számának növekedésével viszont csökken. Az életkori kockázat 1,6% körül van, de azoknál a nőknél, akiknél közvetlen rokonok érintettek ez az arány 5%-os. Azoknál a nőknél, akiknél a BRCA1 vagy a BRCA2 gének estek át mutáción, a kockázat 25% és 60% között van, attól függően, hogy a mutáció mennyire volt specifikus.<ref>{{cite book |author=Robert C. Young |chapter=Ch. 83, Gynecologic Malignancies |editor=Jameson JN, Kasper DL, Harrison TR, Braunwald E, Fauci AS, Hauser SL, Longo DL |title=Harrison's principles of internal medicine|publisher=McGraw-Hill Medical Publishing Division |location=New York |year=2005 |edition=16th |isbn=0-07-140235-7 |url=http://highered.mcgraw-hill.com/sites/0071402357/information_center_view0/}}</ref> |
||
A lap 2011. augusztus 19., 07:55-kori változata
| Az itt található információk kizárólag tájékoztató jellegűek, nem minősülnek orvosi szakvéleménynek, nem pótolják az orvosi kivizsgálást és kezelést. A cikk tartalmát a Wikipédia önkéntes szerkesztői alakítják ki, és bármikor módosulhat. |
| Petefészekrák | |
 | |
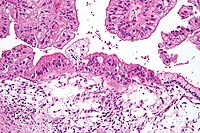
| Kétoldali szerózus petefészekrák. (Kórbonctani készítmény) | |
| Szinonimák | Rosszindulatú petefészekdaganat |
| Latinul | Carcinoma ovarii |
| Angolul | Ovarian cancer |
| Osztályozás | |
| BNO-10 | C56H0 |
| Epidemiológia | |
| Földrajzi előfordulás | fejlettebb országokban gyakoribb |
| Leírás | |
| Érintett szervek | egyik vagy mindkét petefészek, áttétképzés után a hashártya és életfontos szervek |
| Etiológia | genetikai hiba és/vagy számos ismeretlen tényező együttesen |
| Kockázati tényezők | hibás gének, életkor |
| Főbb tünetek | nem jellemzőek |
| Diagnosztika | nincs megbízható korai diagnosztika vagy szűrővizsgálat; gyanú esetén: hüvelyi ultrahang, laparoszkópia(hasi tükrözés), CT, MRI |
| Szövődmények | áttétek a kismedencében, majd az egész szervezetben; az áttétek által károsított szervek funkciójának romlása |
| Kezelés | műtét, citosztatikum, sugárterápia |
| Kórjóslat | igen kedvezőtlen |
| Megelőzés | ma még nem ismert, ill. a különösen nagy genetikai kockázatú csoportoknál a petefészek műtéti eltávolítása jöhet szóba |
| OMIM | |
| DiseasesDB | 9418 |
| MedlinePlus | 000889 |
A Wikimédia Commons tartalmaz Petefészekrák témájú médiaállományokat. | |
A petefészekrák a petefészek (ovarium) valamelyik részéből kiinduló rosszindulatú rákos burjánzás. Egyik legnagyobb probléma vele, hogy gyakran túl későn kerül felismerésre. Nem mindegyik, a betegségben szenvedő nőnél jelentkeznek tünetek, amelyek közül a jellegzetesek: haspuffadás, medencei fájdalom, étkezési zavarok, és a gyakori vizeletűrítés könnyen összetéveszthetők más betegségekkel.[1] A petefészekrák a második leggyakoribb nőgyógyászati rák.[2] és elérte – a kedvezőnek nem tekinthető - 47%-os túlélési arányt a késő 1970-es[1] évek 38%-áról. Ez idő alatt más rákok általános ötéves túlélési ideje sokkal jelentősebben javult, az általános népességet tekintve 68%-ra a 2001-ben diagnosztizált esetek aránya az 1970-es[1] évek 50%-áról. Megközelítőleg a nők 5-10%-át műtötték életük során valamilyen ováriális szövetszaporulat miatt, amelyek jelentős részben jóindulatúak voltak.[1] A legtöbb (>90%) petefészekrákot a hám eredetűek közé sorolják, de vannak arra utaló bizonyítékok is, amelyek szerint a méhkürt szintén kiindulója lehet bizonyos petefészekrákoknak.[3] Mivel az ovariumok és a méhkürtök nagyon közeli viszonyban állnak egymással, feltételezik, hogy a méhkürtök sejtjeinek elfajulásai utánozhatják a petefészekrákot.[4] Más típusok a petesejtekből indulnak ki (csírasejt daganatok), vagy a kötőszöveti sejtekből a gonádlécek/redők ’’(plica gonadalis)’’ támasztósejtjeiből.
Statisztika
2010-ben az Amerikai Egyesült Államokban – becslések szerint – 21 800 új esetet diagnosztizáltak, és 13 850 nő halt meg petefészekrákban. A kockázat az életkorral nő, míg a terhességek számával csökken. Az életkori kockázat 1,6% körül van, de azoknál a nőknél, akiknél elsőfokú rokonokat érintett a betegség, ez 5,0% -os. Azoknál a nőknél, akiknél a BRCA1 vagy a BRCA2 gén mutációja volt kimutatható a kockázat 25% és 50% között volt, a mutáció jellegétől függően.[5] A petefészekrák a gyakoriságában a második helyen van a nőknél (mintegy 1/70-ed részüket érinti, és a vezető helyen áll a nőgyógyászati rákok okozta halálozásban, és a leginkább halálos kimenetelű (a nők 1%-a ebben hal meg). Az ötödik helyen áll nőkben az összes rákos halálokok között. 2008-ban – becslések szerint –15 000 nő halálát okozta. Ezek a mutatók a fejlett országokban a magasabbak. 2004 és 2008 között a petefészekrák diagnózisok a 63 éveseknél érték el a életkor szerinti gyakorisági eloszlás medián értékét.
| Életkor | Előfordulási gyakoriság % |
|---|---|
| 20 év alatt | ~1,2% |
| 20 és 34 év között | 3,5% |
| 35 és 44 év között | 7,3% |
| 45 és 54 év között | 19,1% |
| 55 és 64 év között | 23,1% |
| 65 és 74 év között | 19,7% |
| 75 és 84 év között | 18,2% |
| 85 év felett | 8,0% |
| Összesen | 100% |
A 10 éves túlélési idő az IA stádium 84,1%-ától a IIIC stádium 10,4%-áig változott (romlott).
Jelek és tünetek
A petefészekrák korai jelei és tünetei gyakran hiányoznak, és amennyiben meg is vannak nagyon enyhék és jellegtelenek lehetnek.[8] A legtöbb esetben ezek a tünetek több hónapon keresztül fennállnak, mielőtt felismernék és diagnosztizálnák azokat. A petefészekrákban megbetegedett nők jeleznek egy vagy több tünetet, mint például a hasüregi fájdalmat vagy diszkomfort (kellemetlen) érzést, hasüregi szövetszaporulatot, haspuffadást, hirtelen vizelési kényszert, hátfájást, fáradékonyságot és más nem specifikus tüneteket, de jellemzőbb tüneteket is mint a kismedencei fájdalmat, rendellenes hüvelyi vérzést, vagy nem indokolt fogyást.[9] [10][11] A hasüregben folyadék (ascites ) szaporodhat fel. Egy előre tervezett (prospectív) esetvizsgálatban 1709 nőn, akik rendszeresen látogatták a járóbeteg rendelést, azt találták, hogy haspuffadás, megnövekedett hastérfogat, és vizelettel kapcsolatos panaszok voltak jelen azok 43%-ánál, akiknél petefészekrák volt jelen, de ezeknek csak 8%-a jelentkezett az elsődleges ellátást biztosító klinikákon.[12] Két előre tervezett esettanulmányról számoltak be. Az elsőben azt találták, hogy a petefészekrákban szenvedők tünetei a megnövekedett hastérfogat, a puffadás, a sürgős vizelési inger és a medencei fájdalom.[11] A második, kisebb vizsgálatban azt állapították meg, hogy a petefészekrákos nők tünetei a megnövekedett hastérfogat/puffadás és evési nehézség/teltségérzet.[13] Ebben a második vizsgálatban meghatároztak egy tünet-listát, amelyet kritikusnak ítéltek, legalábbis abból hatot, amelyek „több mint tizenkét esetben jelentek meg havonta, de kevesebb mint egy évig jelentkeztek”.
Okok
Az esetek többségében a petefészekrák pontos oka ismeretlen marad. A petefészekrák kifejlődésére úgy látszik, hogy sok tényező hat.[14] Az idősebb nőknél és azoknál, akik a betegséget tekintve az első vagy második fokozatban vannak, a kockázati tényező magasabb. A petefészekrák örökletes formáit okozhatják specifikus gének mutációi (nevezetesen a ’’BRCA1” és a ’’BRCA2’’, de okozhatják az örökletes nem-polipózus vastag- és végbélrák ’’(colorectalis rák)’’ génjei is. A meddő nők valamint azok, akik az endometriozisnak nevezett kórképben szenvednek, azok akiknek sohasem volt terhessége és akik postmenstruális ösztrogén pótló kezelést kaptak, ugyancsak fokozott kockázati tényezővel bírnak. A kombinált orális fogamzásgátló tabletták szedése viszont védő hatású [15][16] Minél több a nő gyermekeinek száma, annál inkább csökken nála a petefészekrák kockázata. Az első terhesség koraisága, az utolsó terhesség életkorának kitolódása és az alacsony dózisú hormonális fogamzásgátló tabletták szintén védő hatásúnak bizonyultak. A kockázati tényező azoknál a nőknél is csökken, akiknek a Fallop-kürtjét (méhkürtjét) ’’(tuba uterina)’’ lekötéssel sebészetileg elzárták. 489 magas fokozatú komoly petefészek adenocarcinómánál azt találták, hogy 96%-ban a p53 gén mutált. Más elég általánosan előforduló mutált gének voltak az NF1, BRCA1, 3RB1 és a cyclin-dependens kináz 12 (CDK12).
Hormonok
Az orális fogamzásgátlók használata és a petefészekrák közötti összefüggést 45 csoporton végzett, kontrollcsoportokkal összehasonlított és előre megtervezett vizsgálatok összegzéseként mutatták ki. A vizsgálatok összesítése szerint az orális fogamzásgátlók védő hatásúak a petefészekrákokkal szemben. Azoknál a nőknél, akik 10 éven keresztül használtak orális fogamzásgátlókat, mintegy 60%-al csökkent a petefészekrák kockázata.[15][16] (a kockázati arány és a statisztikai szignifikancia megbízhatóságának széles intervalluma a nagy mintán végzett vizsgálat miatt nem meglepő). Ez azt jelenti, hogy ha 250 nő tíz éven keresztül orális fogamzásgátlót szedett, egy petefészekrák megelőzésre kerülhetett. Ez volt mindeddig a legkiterjedtebb epidemiológiai vizsgálat a petefészekrák esetében (a 45 vizsgálat 20 000 petefészekrákban szenvedő és mintegy 80 000 kontroll egyénre terjedt ki). A petefészkek petesejteket tartalmaznak és hormonokat választanak ki, amelyek a reproduktív ciklust szabályozzák (lásd még: Menstruációs ciklus). A petefészkek és a petevezetékek műtéti eltávolítása erősen csökkenti a vérben keringő ösztrogén és progeszteron hormonok szintjét. Ez leállíthatja vagy lassíthatja az emlő- és petefészekrákok fejlődését, amelyeknek szükségük van ezekre a hormonokra.[15] A fogamzást elősegítő gyógyszerek alkalmazásával való kapcsolat, mint például a Clomiphene citrát az adagolásával, az eredmények ellentmondásosak voltak. Egy 1991-ben végzett elemzés felvetette azt a lehetőséget, hogy az ilyen gyógyszerek növelhetik a petefészekrák kockázatát. Számos követéses és kontrollcsoportos vizsgálatot végeztek azóta anélkül, hogy következetes bizonyítékot találtak volna erre az összefüggésre. Ez mindenesetre egy komplex téma marad, mivel a meddő populáció nem tekinthető azonosnak a termékeny populációval.
Genetika

Az örökletes mellrák kialakulásában szereplő gének megközelítő aránya:
- BRCA1 mutációk (28%)
- BRCA2 mutációk (19%)
- Az összes többi ismert gén (8%)
- Ismeretlen gének vagy többszörös gének (45%)
Nagyon komoly bizonyítékok vannak arra nézve, hogy a nők egy részénél a genetikai tényezők fontosak. Bizonyos BRCA mutációk hordozói jelentős kockázattal rendelkeznek. A BRCA1 és a BRCA2 gének mintegy 5-13%-ban szerepelnek a petefészekrákokban.[17] és bizonyos populációkban (például az askenázi zsidó nőknél) nagyobb a kockázata mind a mellráknak, mind a petefészekráknak, és gyakrabban jelentkezik korábbi életkorban, mint a populáció egészében.[18] Azoknál a pácienseknél, akiknél előzetes emlőrák kórtörténet van, vagy az emlő/petefészekrák halmozott családi előfordulása áll fenn, különösen ha a diagnózis fiatalkorból származik, nagyobb rizikófaktorral rendelkezőknek tekintendők, és szükséges, hogy a karcinóma gén- re nézve kivizsgálásra kerüljenek.
Az Egyesült Államokban 10-20%-a mellrákos és a petefészekrákos pácienseknek első-, vagy másodfokú viszonylagos kockázata van ezen betegségek valamelyikére vonatkozóan. Bármelyik nagy hajlamosító gén mutációja - a mellrák 1-es hajlamosító gén (BRCA1) és a 2-es hajlamosító gén (BRCA2) – életkor rövidülési kockázatot jelent a mellrák esetébe 60-85%-ban, a petefészekrák esetében 15-40 %-ban. Ugyanakkor ezeknek a géneknek a mutációja a mellrákoknak csak 2-3%-ában játszik szerepet.[19]
A méhrákra, vastagbélrákra és más gyomor-bélrendszeri rákra vonatkozó halmozott családi előzmények azt jelenthetik, hogy örökletes nem-polipózus vastag- és végbélrák (HNPCC, másként Lynch-szindrómaként ismert) tünetcsoport van jelen, amely a petefészekrák magasabb kockázatával jár. A petefészekrákra magas kockázattal bíró páciensek esetében megfontolható a profilaktikus, azaz preventív (megelőző jellegű) kétoldali, sebészeti petefészek-eltávolítás a gyermekszülésre alkalmas évek elmúltával. A megelőző petefészek-eltávolítás jelentősen csökkenti mind az emlőrák, mind a petefészekrák kifejlődését a magas fokú kockázattal bíró csoportoknál. Azoknál a nőknél, akiknél a BRCA gének mutációja mutatható ki, általában a méhkürtöt is eltávolítják (salpingo-oophorectomia), tekintettel arra, hogy a méhkürtből kiinduló daganatokra nézve is magasabb a kockázati tényezőjük.[20]
Egy örökletes mell- és petefészekrák szindrómára (HBOC) vonatkozó vizsgálatban azt találták, hogy a szindróma a normálnál magasabb gyakorisággal eredményez mellrákot és petefészekrákot az örökletesen rokon családokban (akárcsak egy családtag szenvedett mindkettőben, vagy pedig a család több tagja a kórképek egyikében). Az örökletes tényező jelenléte bizonyítható, vagy gyanítható a mell- és petefészekrákok családi előfordulása alapján.
Alkohol
Az alkoholfogyasztás – úgy tűnik – nem befolyásolja a petefészekrák kialakulását.[21]
Egyebek
Egy svéd vizsgálatban, amelyben több mint 61 000 nőt követtek figyelemmel 13 évig, szignifikáns összefüggést találtak a tejfogyasztás és a petefészekrák között. A BBC szerint ’’a vizsgálatok azt mutatták, hogy a tejfogyasztásnak van a legszorosabb összefüggése a petefészekrákkal, mivel azok a nők, akik napi két pohárnak megfelelő, vagy annál több tejet fogyasztottak, kétszeres kockázattal bírtak azokkal szemben, akik egyáltalán nem fogyasztottak, vagy csak kis mennyiségben tejet.[22] Az újabb vizsgálatok szerint a nagyobb napsütést kapó országokban élő nők petefészekrák kockázata kisebb, ami valamiképpen összefügg a magasabb D-vitamin szinttel.[23] Más vizsgálatok szerint, az olyan anyagok felhasználásával járó munkák, mint a talkum, [24][25][26] vagy az azbeszt, vagy a gyermekkori fültőmirigy gyulladás (mumpsz)[27] hatása ellentmondásos, és nem kerültek egyértelműen igazolásra. Ezen túlmenően ezek a kockázati tényezők bizonyos esetekben inkább a rákra hajlamos genetikai tulajdonságú egyéneknél jelentkeznek.[26]
Kockázati tényezők

A gyermekes nők kevésbé vannak kitéve a petefészekráknak, mint a gyermektelenek. A szoptatás szintén csökkenti bizonyos petefészekrák típusok kockázatát. A petevezeték lekötése és a méh eltávolítása (hysterectomia) csökkenti a kockázatot, a kétoldali petevezeték és petefészek eltávolítása (bilaterális salpingo-oophorectomy) pedig drámaian csökkenti nem csupán a petefészekrák, de a mellrák kockázatát is.[28] A petefészkek és a méh együttes eltávolítása egyharmadára csökkentik a petefészekrák kifejlődésének kockázatát,[29] ugyanakkor nem növekszik a más típusú rákok, a szívbetegségek vagy a combnyaktörések kockázata, amint azt az University of California San Franciscoi részlegéből publikálták az Archives of Internal Medicine-ben.[30] A Lancet egy közleménye arra utal, hogy az örökletes petefészekrák kockázatát a méhkürt lekötése 72%-al csökkenti a BRCA1 gént hordozó nőkben.[31] Az orális fogamzásgátlók (születésszabályozó tabletták) öt vagy több éven át szedve 50%-al csökkentik a veleszületett petefészekrák kockázatát az idősebb nőknél.[32]
Diagnózis


A petefészekrák diagnosztizálása fizikális vizsgálattal kezdődik (beleértve a kismedence vizsgálatát is), ezen kívül szükség van egy vérvizsgálatra (a CA-125-re és esetenként más markerekre), egy hüvelyen keresztüli ultrahangra. A diagnózist meg kell erősíteni a hasüreg sebészeti megnyitásával történő megtekintéssel és biopsziás anyagvétellel (mikroszkópos vizsgálatra alkalmas anyagminta kimetszésével) és keresni kell a rákos sejteket a hasüregi folyadékban. A petefészekrákot korai stádiumaiban (I/II) nehéz felismerni mindaddig míg tovább nem terjed a későbbi fokozatokig (III/IV). Ez amiatt van, hogy a tünetek többsége nem specifikus, így kicsi a diagnosztikus értékük. A szérum BHCG (a vér human chorion gonadotropin hormon szintjét meg kell határozni minden olyan nőnél, akinél a terhesség lehetősége fennáll. Ezen túlmenően a szérum alfa-fetoprotein (AFP) és laktát-dehidrogenáz (LDH) szint meghatározandó petefészek tumor gyanús fiatal és serdülőkorú lányokon, mivel minél fiatalabb a páciens, annál nagyobb a valószínűsége egy rosszindulatú csírasejt daganatnak. Ha a rosszindulatú petefészek-daganat diagnosztikai valószínűsége fennáll, bizonyos laboratóriumi vizsgálatok elvégzése szükséges. A teljes vérkép és a szérum elektrolit vizsgálat minden páciensnél elvégzendő. A CA-125 elnevezésű marker vérvizsgálata hasznos az elkülönítő diagnózishoz és a betegség követéséhez, de önmagában nem elég hatékony módszer a petefészekrák korai stádiumainak követéséhez, mert ehhez az érzékenysége és specifikussága nem elegendő. Az új teszt, amit az FDA "(US Food and Drug Administration)" 2011-ben hagyott jóvá, az OVA1 felülmúlja a petefészekrák észlelésében a CA125 vértvizsgálattal kombinált klinikai értékelést. 2011 júniusában egy, az Obstetrics & Gynecology-ban publikált cikkben leírták, hogy az OVA1 kombinálása egy preoperatív orvosi vizsgálattal biztosabban képes kimutatni egy nő petefészek-szövetszaporulatáról, hogy petefészekrákról vagy petefészekkel kapcsolatos rákról van-e szó, mint egy preoperatív orvosi vizsgálat önmagában.[33]. Az OVA1 csak az olyan 18 évet betöltött nőknek javasolt, akit már műtétre kiválasztottak a kismedencei szövetburjánzásuk miatt. Nem szánják a petefészekrák szűrésére, vagy a petefészekrák végleges diagnózisának megállapítására. Az OVA1-et a Johan Hopkins Egyetem (Baltimore) kutatói fejlesztették ki.[34]. A folyamatban lévő vizsgálatokban keresik annak a módját, hogyan kombinálhatók a tumor marker fehérjék a betegség más jelzőivel (pl. a radiológiai vagy más tünetekkel), hogy a pontosságot javítsák. Ennek a megközelítésnek az a nehézsége, hogy a petefészekrák egyenetlen előfordulási gyakorisága miatt még a nagy érzékenységű és fajlagosságú tesztek is számos fals pozitivitást eredményeznek (azaz olyan esetekben is sebészeti beavatkozásra kerülhet sor, amikor végül is a műtét során nem találnak rosszindulatú daganatot.) A fehérje természetű jelzőanyagok felhasználása azonban még korai szakaszában van, és további finomítást igényel. A fehérje természetű jelzőanyagok vizsgálatának jelenlegi helyzete viszont azt is jelzi, hogy a terápiás elvek az egyénre szabott eljárások felé tolódik el.[35] A kismedencei vizsgálat és a képalkotó eljárások, beleértve a Computeres tomográfiás (CT) vizsgálatokat és a hüvelyen keresztüli ultrahangot, alapvető fontosságúak. A fizikális vizsgálatok kimutathatják a has körfogatának növekedését és/vagy az ascites (folyadék a hashártya üregében) jelenlétét. A medencei vizsgálat kimutathatja a petefészeki vagy kismedencei szövetszaporulatot. A kismedencei vizsgálathoz hozzátartozik a végbélen és a hüvelyen keresztüli tapintás, amely a petefészkek jobb kitapintását teszi lehetővé. A nagyon fiatal páciensek esetében a mágneses magrezonancia képalkotás (MRI) vizsgálatot kell előnyben részesíteni a végbélen és hüvelyen keresztüli vizsgálatokkal szemben.
A petefészekrák biztos diagnózisához szükség van a hasüregbe való betekintésre. Ez történhet a hasüreg sebészeti feltárásával (laparatomia), vagy egy kis bemetszésen át egy erre alkalmas optikai műszer bevezetésével (laparoscopia). E vizsgálatok során a gyanús területekről szövetminták vehetők kórszövettani vizsgálatra. A hasüregi folyadékot szintén vizsgálni lehet rákos sejtek jelenlétére. Amennyiben rák van jelen ezek az eljárások módot adnak a folyamat előrehaladottságának, a rosszindulatú daganat fokozatának (stádiumának) meghatározására is.
Osztályozás


A petefészektumorokat a daganat patológiailag megállapított szövettani szerkezete szerint osztályozzák. A szövettani lelet a klinikai eljárásnak, az általános kezelésnek, és a kórjóslatnak (prognózis) számos elemét meghatározza.
- A felszíni hám-kötőszöveti "(epithelial-stromal)" daganat, amely ’’’petefészek-hám rák”-ként is ismert, a petefészekrákok leggyakoribb formája. Ebbe beletartozik a szerózus, az endometriális daganat, és a nyákos, üreges daganat (cisztadenocarcinoma).
- A nemi kötőszöveti gerenda/léc támasztósejtjeinek (sex cord-stromal) daganatai, amelyekhez tartozik a granulosa sejtek és a férfiasság felé vezető Sertoli-Leydig sejt daganata , vagy arrhenoblasotma, amely mintegy 8%-át okozza a petefészekrákoknak.
- A csírasejt eredetű daganatok a petefészektumoroknak mintegy 30%-át teszik ki, de petefészekrákoknak csak kb. 5%-át, mivel a legtöbb csírasejt eredetű daganat teratoma, és a teratómák többsége jóindulatú. Az ivarsejt eredetű daganatok főleg a fiatal nőkben és lányokban hajlamosak megjelenni. A kórjóslat a csírasejt eredetű daganatoknál az adott tumor szövettani jellemzőitől függ, de általában kedvező.
- Vegyes/kevert daganatok, amelyek több mint egy elemét tartalmazzák a fentebb felsorolt daganatféleségeknek.
| A petefészekrákok megoszlása 20 évnél idősebb nőknél % |
Kórszövettan | 5 éves relativ túlélési arány RSR % |
|---|---|---|
| 89,7 | Felszíni hám-kötőszöveti váz tumor (adenocarcinóma) | 54,4 |
| 26,4 | Papilláris szerózus cisztadenocarinóma | 21,0 |
| 15,9 | "Határeset" (borderline) adenocarcinóma (alábecsült b/c , ha az adatgyűjtés ideje rövid) |
98,2 |
| 12,6 | Egyébként nem specifikált adenocarcinóma | 18,3 |
| 9,8 | Endometrioid daganat | 70,9 |
| 5,8 | Szerózus cisztadenocarcinóma | 44,2 |
| 5,5 | Szemölcsös daganat (papilloma) | 21,0 |
| 4,2 | Nyákos cisztadenocarcinóma | 77,7 |
| 4,0 | Világos-sejtes petefészekdaganat | 61,5 |
| 3,4 | Nyákos adenocarcinóma | 49,1 |
| 1,3 | Cisztadenocarcinóma | 50,7 |
| 5,5 | Carcinóma | n. a.[37] |
| 4,1 | Egyébként nem specifikált karcinóma | 26,8 |
| 1,1 | Szex-léc vázi tumor | 87,8 |
| 0,3 | Más, specifikált karcinómák | 37,3 |
| 1,7 | Müller-cső tumor | 29,8 |
| 1,5 | Szaporítósejt tumor | 91,0 |
| 0,8 | Teratóma | 89,1 |
| 0,5 | Diszgerminóma | 96,8 |
| 0,3 | Más, specifikált | 85,1 |
| 0,6 | Egyébként nem definiált | 23,0 |
| 0,5 | Epidermoid (laphámsejtes) karcinóma) | 51,3 |
| 0,2 | Brenner daganat | 67,9 |
| 0,2 | más specifikált | 71,7 |
A petefészekrák lehet másodlagos is, ha más - szervekben bárhol a testben- , képződött elsődleges daganatok áttételeként jön létre. A petefészekrákok 7%-a áttétel (metastasis) következménye, míg a többi elsődleges tumor (rák). A leggyakoribb elsődleges rákok a mellrák és a gyomor-béltraktus daganatai (általánosan tévesen értelmezik a Krukenberg-féle daganatot[38] valamely, a gyomor-béltraktus daganataiból származó áttétnek, holott ez csak akkor igaz, ha az áttét elsődleges gyomor-daganatból származik. A felszíni hámból és a szerv kötőszövetes vázából kiinduló tumorok kiindulhatnak a hashártyából[39], amikor is a petefészekrák a hashártyadaganat következménye (azaz másodlagos), de a kezelés alapvetően azonos a petefészekrákból kiinduló, és a hashártyán terjedő daganatokkal.
A petefészekrák stádiumai
A petefészekrák stádium (súlyossági, előrehaladottsági fokozat) szerinti osztályozása a FIGO („International Federation of Gynecology and Obstetrics”; Nemzetközi Nőgyógyászati és Szülészeti Szövetség) rendszere szerint történik, amelyhez az információk a sebészeti beavatkozások során kapott megfigyelésekből és adatokból származnak. A sebészeti beavatkozás lehet teljes, hasüreg felőli méheltávolítás (hysterectomia), általában mindkét petefészek, a méhkürtök és a cseplesz eltávolítása, a kismedencei hashártyaüreg átmosása vizsgálatra alkalmas sejtek kinyeréséhez. Az AJCC „(American Joint Committee on Cancer)" "(Based on the AJCC Cancer Staging Manual)” stádiumbeosztása megegyezik a FIGO stádiumbeosztással.[40]. Az AJCC stádiumbeosztási rendszere leírja az elsődleges (primer) Tumor (T) nagyságát, az áttétek hiányát vagy meglétét a szomszédos Nyirokcsomókban (N) és a távoli áttétek (metastasis) (M) hiányát vagy meglétét. [41]
- I. Stádium – az egyik vagy mindkét oldali petefészekre korlátozódik
- IA – az egyik petefészkre terjed ki; a tok ép; nincs tumor a petefészek felszínén; nincsenek malignus sejtek a hashártyaüregi folyadékban vagy az öblítéssel nyert folyadékban
- IB – mindkét oldali petefészekre ráterjed; a tok ép; nincs tumor a petefészek felszínén; nincsenek malignus sejtek a hashártyaüregi folyadékban vagy az öblítéssel nyert folyadékban
- IC – az ovariumokra korlátozódó tumornál a következők közül valamelyik jelen van: a tok megrepedt, daganatsejtek a petefészek felszínén, tumorsejtek a mosófolyadékban
- II. Stádium – ráterjed a kismedencére vagy kisebb különálló áttéteket képez azon
- IIA – ráterjed az anyaméhre vagy a méhkürtökre vagy kisebb különálló áttéteket képez azokon, a mosófolyadékban nincsenek tumorsejtek
- IIB - ráterjed a kismedence más képződményeire vagy kisebb különálló áttéteket képez azokon, a mosófolyadékban nincsenek tumorsejtek
- IIC - ráterjed a kismedence más képződményeire vagy kisebb különálló áttéteket képez azokon, a mosófolyadékban tumorsejtek vannak
- III. Stádium – mikroszkópikus áttétek a kismedencén kívüli hashártyaterületeken; vagy megmarad a kismedencében, de ráterjed a vékonybélre vagy a csepleszre (omentum)
- IIIA – mikroszkópikus hashártyaáttétek a kismedencén kívül
- IIIB - 2 cm-nél kisebb méretű makroszkópikus áttétek a medencén kívüli hashártyán
- IIIC - 2 cm-nél nagyobb méretű makroszkópikus áttétek a medencén kívüli hashártyán, vagy nyirokcsomóáttétek
IV. Stádium – távoli áttétek a májban vagy a hashártyaüregen kívül
A főverőér menti (para-aortikus) nyirokcsomók áttétei tájéki nyirokcsomó-áttéteknek tekintendők (IIIC stádium). Mivel csupán egy para-aortikus nyirokcsomó van közbeiktatva a mellvezeték (ductus thoracicus) előtt a test jobb oldalán, a petefészekrák gyorsan képezhet áttéteket olyan távoli szervekben is, mint a tüdők. Az AJCC/TNM stádiumbeosztás a petefészekráknak három kategóriáját foglalja magába, nevezetesen a T, az N és M kategóriákat. A T kategória három másik alkategóriát tartalmaz, a T1, T2 és T3 alkategóriákat, amelyek aszerint vannak besorolva, hogy a tumor hol fejlődött ki (egyik vagy mindkét petefészekben, a petefészek belsejében vagy a petefészken kívül). A petefészekrák T1 kategóriája azokat a petefészekdaganatokat írja le, amelyek a petefészekre korlátozódnak, és azok közül egyet vagy mindkettőt érintik. A T1a alkategóriát arra a rákos stádiumra alkalmazzák, amelyeknél a rákos daganat csak az egyik oldali petefészket érinti, a tokot épen hagyja, és nem mutatható ki a kismedencei folyadékból. Az olyan rák, amely nem szűri be a tokot, csak a petefészek állományában található és rákos sejtek nincsenek a kismedencei folyadékban, de minkét oldali petefészket érinti a T1b alkategóriába sorolandó. A T1c kategória egy olyan tumort jelent, amely egyik vagy mindkét oldali petefészket érintheti, és amely áttör a petefészek (petefészkek) (ovarium) tokján, és a rákos sejtek megtalálhatók a kismedencei hashártyai folyadékban. A T2 a rák egy előrehaladottabb stádiuma. Ebben az esetben az egyik vagy mindkét petefészekből kiinduló daganat ráterjed az anyaméhre (uterus) és egyik, vagy mindkét oldali méhkürtre (tuba uterina) A petefészekrák stádiumbeosztása a TNM kategóriák kombinációjával a következőképpen történik:
- I. Stádium: T1+N0+M0
- IA: T1a+N0+M0
- IB: T1b+N0+M0
- IC: T1c+N0+M0
- II.Stádium: T2+N0+M0
- IIa: T2a+N0+M0
- IIB: T2b+N0+M0
- IIC: T2c+N0+M0
- III. Stádium: T3+ N0+M0
- IIIA: T3a+ N0+M0
- IIIB: T3b+ N0+M0
- IIIC: T3c+ N0+M0 or Any T+N1+M0
- IV. Stádium: Bármelyik T+ Bármelyik N+M1
A petepészekrákot – hasonlóan más ráktípusokhoz – a stádiumbeosztáson kívül fokozatokba is sorolják. A kórszövettani fokozat azt jelzi, hogy milyen a rosszindulatú tumoros sejtek mikroszkópos kinézete.[42] Négy fokozatot különböztetnek meg, amelyek azt mutatják, hogy milyen a valószínűsége a daganat továbbterjedésének. A magasabb fokozat nagyobb továbbterjedési valószínűséget jelent. A 0 fokozat a nem invazív (nem tovaterjedő) daganatokat jelenti. A 0 fokozatot használják a határesetei tumorokra is.[42] Az 1-es fokozatú tumorok olyan sejtekből állnak, amelyek jól differenciáltak (nagyon hasonlítanak a normál szövetekre), ezek a legjobb prognózisúak. A 2-es fokozatú daganatok szintén mérsékelten jól differenciáltak, és a normál szövetekre hasonlító sejtekből állnak. A 3-as fokozatú daganatok prognózisa a legrosszabb, sejtjeik abnormálisak, nagyon kevéssé differenciáltak. A T2a stádiumot az olyan rákos daganatok jellemzésére használják, amelyek az anyaméhre vagy/és a méhkürtre terjedtek rá, de a tumorsejtek nincsenek jelen a kismedencei hashártyaüregi (peritóneális) folyadékban. A T2b és a T2c olyan stádiumokat jelent, amelyek áttéteket képeztek az anyaméhen és a méhkürtön kívüli kismedencei szerveken/szöveteken, és amelyek sejtjei nem találhatóak meg a kismedencéből nyert peritóneális folyadékban. A T3 stádium olyan rák megjelölésére szolgál, amely ráterjedt a hashártyára . Ez a stádium a daganatáttétek nagyságára vonatkozó jellemzőket jelent (amelyek a test más tájékain találhatók, de a petefészekrákból indultak ki ). Ezek a daganatok lehetnek nagyon kis méretűek, amelyek csak mikroszkóp alatt láthatók (T3a), szabad szemmel láthatók, de nem nagyobbak 2 cm-nél (T3b), valamint nagyobbak, mint 2 cm (T3c). Az AJCC/TNM stádiumbeosztás a petefészekráknak három kategóriáját foglalja magába, nevezetesen a T, az N és M kategóriákat. A T kategória három másik alkategóriát tartalmaz, a T1, T2 és T3 alkategóriákat, amelyek aszerint vannak besorolva, hogy a tumor hol fejlődött ki (egyik vagy mindkét petefészekben, a petefészek belsejében vagy a petefészken kívül. A petefészekrák T1 kategóriája azokat a petefészekdaganatokat írja le, amelyek a petefészekre korlátozódnak, és azok közül egyet vagy mindkettőt érintik. A T1a alkategóriát arra a rákos stádiumra alkalmazzák, amelyeknél a rákos daganat csak az egyik oldali petefészket érinti, a tokot épen hagyja, és nem mutatható ki a kismedencei folyadékból. Az olyan rák, amely nem szűri be a tokot, csak a petefészek állományában található és rákos sejtek nincsenek a kismedencei folyadékban, de minkét oldali petefészket érinti a T1b alkategóriába sorolandó. A T1c kategória egy olyan tumort jelent, amely egyik vagy mindkét oldali petefészket érintheti, és amely áttör a petefészek (petefészkek) (ovarium) tokján, és a rákos sejtek megtalálhatók a kismedencei hashártyai folyadékban. A T2 a rák egy előrehaladottabb stádiuma. Ebben az esetben az egyik vagy mindkét petefészekből kiinduló daganat ráterjed az anyaméhre (uterus) és egyik, vagy mindkét oldali méhkürtre (tuba uterina) vagy más kismedencei szövetekre. A T2a stádiumot az olyan rákos daganatok jellemzésére használják, amelyek az anyaméhre vagy/és a méhkürtre terjedtek rá, de a tumorsejtek nincsenek jelen a kismedencei hashártyaüregi (peritóneális) folyadékban. A T2b és a T2c olyan stádiumokat jelent, amelyek áttéteket képeztek az anyaméhen és a méhkürtön kívüli kismedencei szerveken/szöveteken, és amelyek sejtjei nem találhatóak meg a kismedencéből nyert peritóneális folyadékban. A T3 stádium olyan rák megjelölésére szolgál, amely ráterjedt a hashártyára . Ez a stádium a daganatáttétek nagyságára vonatkozó jellemzőket jelent (amelyek a test más tájékain találhatók, de a petefészekrákból indultak ki ). Ezek a daganatok lehetnek nagyon kis méretűek, amelyek csak mikroszkóp alatt láthatók (T3a), szabad szemmel láthatók, de nem nagyobbak 2 cm-nél (T3b), valamint nagyobbak, mint 2 cm (T3c). Ez a stádiumbosztási rendszer szinté N-kategóriákat használ azoknak a rákoknak a jellemzésére, amelyek túljutottak (vagy nem) a közeli nyirokcsomókon. Csak két N kategória van: az N0, amely azt jelzi, hogy a rákos sejtek nem érték el a közeli nyirokcsomókat, és az N1, amely azt jelzi, hogy a daganat közeli nyirokcsomók érintettek. Az M kategóriák az AJCC/TNM rendszerben arról adnak információt, hogy a petefészekrák hova adott áttétet a távoli szervekbe, mint pl. a májba és a tüdőkbe. Az M0 azt mutatja, hogy a petefészekrák nem adott áttéteket a távoli szervekbe, míg az M1 kategória azt jelenti, hogy a rák szétterjedt a szervezet különböző szerveiben. Az M kategóriák az AJCC/TNM stádiumbeosztási rendszerben szintén tartalmaznak Tx és Nx alkategóriákat, ami arra utal, hogy egy daganat kiterjedése nem írható le pontosan, mivel az adatok nem elégségesek annak leírásához, hogy a nyirokcsomók milyen mértékben érintettek. A petefészekrák stádiumbeosztása a TNM kategóriák kombinációjával a következőképpen történik:
- I. Stádium: T1+N0+M0
- IA: T1a+N0+M0
- IB: T1b+N0+M0
- IC: T1c+N0+M0
- II.Stádium: T2+N0+M0
- IIa: T2a+N0+M0
- IIB: T2b+N0+M0
- IIC: T2c+N0+M0
- III. Stádium: T3+ N0+M0
- IIIA: T3a+ N0+M0
- IIIB: T3b+ N0+M0
- IIIC: T3c+ N0+M0 or Any T+N1+M0
- IV. Stádium: Bármelyik T+ Bármelyik N+M1
A petepészekrákot – hasonlóan más ráktípusokhoz – a stádiumbeosztáson kívül fokozatokba is sorolják. A kórszövettani fokozat azt jelzi, hogy milyen a rosszindulatú tumoros sejtek mikroszkópos kinézete.[42] Négy fokozatot különböztetnek meg, amelyek azt mutatják, hogy milyen a valószínűsége a daganat továbbterjedésének. A magasabb fokozat nagyobb továbbterjedési valószínűséget jelent. A 0-ás fokozat a nem invazív (nem tovaterjedő) daganatokat jelenti. A 0-ás fokozatot használják a határesetei tumorokra is.[42] Az 1-es fokozatú tumorok olyan sejtekből állnak, amelyek jól differenciáltak (nagyon hasonlítanak a normál szövetekre), ezek a legjobb prognózisúak. A 2-es fokozatú daganatok szintén mérsékelten jól differenciáltak, és a normál szövetekre hasonlító sejtekből állnak. A 3-as fokozatú daganatok prognózisa a legrosszabb, sejtjeik abnormálisak, nagyon kevéssé differenciáltak.
Epidemiologia



A betegség általánosabb az iparilag fejlett nemzeteknél, kivéve Japánt. Az Egyesült Államokban a nők 1,4-2,5%-ának (egynek 40-60 közül) van esélye arra, hogy élete folyamán petefészekrák alakuljon ki nála. Az idősebb nőknél a kockázat nagyobb.[45] A petefészekrák okozta elhalálozások több mint fele az 55 és 74 éves életkor közötti nőknél következik be, és mintegy negyede a 35 és 54 éves életkorok között. Az Amerikai Egyesült Államokban a statisztikák szerint 2010-ben 21 880 új esetet diagnosztizáltak és 13 850 nő halt meg petefészekrákban. A kockázat az életkorral nő, a terhességek számának növekedésével viszont csökken. Az életkori kockázat 1,6% körül van, de azoknál a nőknél, akiknél közvetlen rokonok érintettek ez az arány 5%-os. Azoknál a nőknél, akiknél a BRCA1 vagy a BRCA2 gének estek át mutáción, a kockázat 25% és 60% között van, attól függően, hogy a mutáció mennyire volt specifikus.[46]
A petefészekrák gyakoriságban a második a nők között (70 közül egy nőt érint), ugyanakkor a vezető halálok a nőgyógyászati rákok közül, és a leginkább halálos kimenetelű (az összes nő 1%-a ebben hal meg). A nők rák okozta halálozásában az ötödik leggyakoribb halálok, statisztikák szerint 15 000 elhalálozást okozott 2008-ban. Az incidencia magasabb a fejlett országokban. [47] 2004 és 2008 között a petefészekrák diagnózis életkori eloszlásának mediánja a 63 éves korra esett. Az életkorra korrigált incidencia ráta 12,8 volt 100 000 nőre egy évre számítva. Ezek az adatok 17 SEER földrajzi egységben megállapított diagnózisokra alapultak.[48]
Szűrés
A nők rutinszerű szűrését petefészekrákra egyik szakmai egyesület sem javasolja. Ezekhez tartozik az „U.S. Preventive Services Task Force” (Az Egyesült Államok Prevenciós Köteléke), „ American Cancer Society” (Az Ameriaki Rákellenes Egyesület), az „American College of Obstetricians and Gynecologists” (A Szülészek és Nőgyógyászok Amerikai Kollégiuma), és a „National Comprehensive Cancer Network” (Nemzeti Átfogó Rákbetegségeket Felügyelő Hálózat).[49] Ez amiatt van, hogy semmilyen kutatási eredmény nem mutatta azt, hogy jobb lett volt a túlélés a szűrt nőkön.[49] Bármilyen rákféleség szűrésének pontosnak és megbízhatónak kell lennie – szükséges követelmény, hogy pontosan kimutassa a betegséget, és nem szabad , hogy fals pozitív eredményeket adjon azoknál az egyéneknél, akiknél nincs rákos elváltozás. Eddig a petefészekrák szűrésének olyan technikája még nincs, amelyről kimutatható lett volna, hogy megfelel ezeknek a kritériumoknak. Mindamellett egyes országokban, mint pl. az Egyesült Királyságban (UK) az olyan nőknek, akiknél valószínűsíthető a petefészekrák magasabb kockázata (mert pl. kimutatható családjukban a betegség halmozódása), orvosaik megajánlhatják az egyéni szűrővizsgálatot, ugyanakkor ez a vizsgálat nem tudja biztosan kimutatni a betegséget korai stádiumban. A kutatók keresik a petefészekrák szűrésének különböző módjait. A szűrő tesztvizsgálatok, amelyek potenciálisan használhatók lehetnek önmagukban, vagy kombinációkban a rutinszerű szűrésre jelenleg a CA-125 markert és a hüvelyen keresztüli (transzvaginális) ultrahang vizsgálatokat foglalják magukba. Az orvosok megmérhetik a CA-125 fehérje szintjét a nők vérében, és annak magas szintje utalhat petefészekrákra, de nem minden esetben. Emellett nem minden petefészekrákban szenvedő nőnél emelkedik meg a CA-125 szintje. A transzvaginális ultrahang a petefészkek ultrahangos vizsgálatát jelenti a hüvely belseje felől, ami tisztább képet ad, mint a hasi ultrahang. Az Egyesült Királyságban (UK) egy Petefészekrák Szűrésre irányuló Kollaborációs Vizsgálati programban tesztelnek egy eljárást, ami a CA-125 vérteszt és a transzvaginális ultrahang kombinációján alapul. A szűrés célja a petefészekrák diagnózisa korai stádiumban, amikor nagyobb a valószínűsége a sikeres kezelésnek. Ugyanakkor a betegség kifejlődése nem teljesen ismert, és vannak olyan vélemények, hogy a petefészekrák korai stádiumaiból nem mindig alakulnak ki késői stádiumú kórképek.[49] Minden szűrési módszernek vannak kockázatai és előnyei, amelyeket gondosan mérlegelni kell, és az egészségügyi szerveknek ezeket ki kell értékelniük, mielőtt bármilyen petefészekrák szűrővizsgálatokat bevezetnének. A petefészekrák szűrésének az volna a célja, hogy a betegséget már az I. stádiumban felismerjék[50] Számos nagyléptékű vizsgálat van folyamatban, de még egyik sem talált egy valóban hatékony eljárást.[51] 2009-ben azonban az Egyesült Királyság Petefészekrák Szűrésre irányuló Kollaborációs Vizsgálati programjának (UKCTOCS) korai eredményei kimutatták, hogy az évenkénti CA-125 tesztek kombinálása az ultrahangos képalkotással segített a betegségnek egy korai stádiumban történő diagnosztizálásában.[52] Ugyanakkor még nem világos, hogy ez a megközelítés jelenleg már segít-e életek megmentésében, mivel az egész vizsgálati sorozat anyaga csak 2015-ben kerül publikálásra.[53]
Kezelés


A kezelésben általában kemoterápiát és műtéti eljárást alkalmaznak, valamint esetenként sugárkezelést.[54]
A sebészeti kezelés elegendő lehet azoknál a rosszindulatú daganatoknál, amelyek jól differenciáltak és csak a petefészke korlátozódnak. A petefészekre korlátozódó, de agresszívabb daganatok esetében kiegészítő kemoterápiára van szükség. A betegség előrehaladottabb stádiumaiban szenvedő betegeknél a kombinált sebészeti beavatkozás és a kombinált kemoterápiás kezelés együttese a standard. A határeseti (borderline) daganatok, még ha továbbterjedtek is a petefészekről, sebészeti beavatkozással jól kezelhetőek, és a kemoterápia nem látszik szükségesnek.
A sebészeti beavatkozás az előnyben részesített kezelés, és gyakran szükség van a műtét során kinyert szövetmintára is a kórszövettani úton megállapítható pontos differenciáldiagnózis érdekében. A nőgyógyászati onkológus specialisták által végzett műtétek általában jobb eredményekhez vezetnek.[55] A jobb túlélési eredményeket annak tulajdonítják, hogy a nőgyógyászati onkológus pontosabban tudja meghatározni a kórkép stádiumát, emellett sokkal radikálisabban tudja kimetszeni a daganatos szövetet, mint az erre nem specializált nőgyógyász, vagy az általános sebész. A sebészeti beavatkozás típusa attól függ, hogy milyen kiterjedésű a rák a diagnosztizálásakor (stádium), valamint, hogy milyen a rák feltételezett típusa és fokozata. A sebész eltávolíthatja csak az egyik oldali (unilateralis oophorectomia), vagy mindkét oldali (bilateralis oophorectomia) petefészket, a méhkürtöket (salpingectomia), és a méhet (hysterectomia). Bizonyos nagyon korai daganatoknál (I.stadium, alacsony fokozatú vagy alacsony kockázatú elváltozás), csak az érintett petefészeket és méhkürtöt távolítják el. (ez az „unilaterális (egyoldali) salpingo-oophorectomia’’, USO), különös jelentősége van fiatal nőknél, akik meg kívánják őrizni termékenységüket.
Előrehaladott rosszindulatú daganatoknál, amelyeknél a teljes eltávolítás már nem végezhető el, olyan sok tumorszövetet kell eltávolítani, amennyit csak lehetséges (en: „debulking surgery”). Azokban az esetekben amelyekben ez sebészeti beavatkozási típus sikeres (azaz <1 cm átmérőjű daganat marad vissza „optimal debulking”; optimális daganatszövet-mennyiség csökkentés), a prognózis javul azokhoz a páciensekhez képest, akiknél nagy daganat-szövetmennyiség (azaz >1 cm átmérő) marad vissza. A minimalisan invazív (károsító, megterhelő) sebészeti technikák elősegítik a nagyon nagy méretű (nagyob mint 10 cm) daganatok eltávolítását is kevesebb sebészeti kockázat mellett.[56] A kemoterápia évtizedeken keresztül általános standard volt a petefészekrákoknál, bár nagyon változó protokollokkal (kezelési sémákkal).[57] A kemoterápiát ma a műtétek után használják a visszamaradt részekre, ha megfelelő. Ez függ a tumor kórszövettani típusától; egyes tumorok (különösen a teratómák) nem érzékenyek a kemoterápiára. Egyes esetekben indokolt a kemoterápiát a sebészeti beavatkozás előtt alkalmazni.
Azoknál a IIIC stádiumú epitheliális petefészek adenocarcinómás pacienseknél, akiknél eredményes optimális daganatszövet-tömeg eltávolítást végeztek, újabb klinikai vizsgálatok kimutatták, hogy a medián túlélési idő szignifikánsan hosszabb, mint azoknál, akik „intraperitóneális” (IP) kemoterápiában részesültek.[58]
Ebben a klinikai vizsgálatban a páciensek kevésbé kedvelték az IP kemoterápiát, és kevesebb, mint fele a pacienseknek kapta meg az IP kemoterápia mind a hat ciklusát. A magas arányú „kiesés” ellenére az egész csoport (azokat is beleértve, akik nem kapták meg a teljes kemoterápiás kezelést) hosszabb túlélést értek el átlagban, mint azok a páciensek, akik csak intravénás kemoterápiában részesültek. Néhány szakember úgy véli, hogy az IP kemoterápia toxicitásával és egyéb komplikációival nem kell számolni a javított, kifejlesztés alatt álló IV típusú hatóanyagoknál. A sugárterápia nem hatásos az előrehaladott stádiumokban, mivel életfontos szervek vannak a sugár útjában, így magas sugáradagokat nem lehet biztonságosan alkalmazni. A sugárterápiát többnyire nem is használják ezekben a stádiumokban, mivel a sugár útjába kerülő életfontos szervek súlyosan károsodnak az ilyen petefészekrákkezelési eljárás során.[59]
Kórjóslat/Prognózis
A petefészekrák kórjóslata általában kedvezőtlen. Aránytalanul halálos kimenetelű, mert nincs bármiféle korai szűrési eljárása, ami azt jelenti, hogy az esetek többsége akkor kerül felismerésre, amikor már elérte az előrehaladott stádiumokat. A petefészekrákkal jelentkező nők több 60%-a már a rák III vagy IV stádiumában van, amikor a rosszindulatú tumor már kirajzott a petefészekből. A petefészekrákokból sejtek válnak le a hasüregben normálisan meglévő folyadékba. Ezek a sejtek beágyazódnak más hasi (hashártyai) képletekbe, így a méhbe, a húgyhólyagba a bélbe és a belet borító csepleszbe (omentum), ezzel új daganatok kiindulási helyeit teremtik meg, még mielőtt a petefészekrákot egyáltalán gyanítanák. A petefészekrák a második leggyakoribb nőgyógyászati rák és a leginkább halálos az abszolút képet tekintve.[60] Egyedül küzel 14 000 elhalálozást okozott az Egyesült Államokban 2010-ben. Míg az átlagos öt éves túlélési idő minden ráktípusnál szignifikánsan javult: a 2001-es egész populációra számított (68%-os arány az 1970-es évek 50%-os arányával[61] , míg a petefészekráké alig változott: 47% túlélési arány az 1970-es évek 50%-ához képest.[62]
Komplikációk
- A rák ráterjedése más szervekre
- A különböző szervek fokozatos funkcióromlása
- Ascites (folyadék a hasüregben)
- A belek átjárhatóságának csökkenése/Bélelzáródások
Állatokban
Petefészekdaganatokról beszámoltak három évesnél öregebb kancákon. A talált daganatok típus szerint teratómák [63][64] cystadenocarcinomák,[65] és leginkább granulosa sejt tumorok voltak.[66][67][68][69][70]
Jegyzetek
- ↑ a b c d WSJ: WSJ.com A New Test to See If Ovarian Masses Are Cancerous - WSJ.com
- ↑ "Ovarian Cancer Facts - Signs, Symptoms and Treatment". The Merck Manual for Healthcare Professionals.
- ↑ Piek JM, van Diest PJ, Verheijen RH (2008). „"Ovarian carcinogenesis: an alternative hypothesis".”. Adv. Exp. Med. Biol..
- ↑ Piek, J.M.J. (2004. October). „Hereditary serous ovarian carcinogenesis, a hypothesis.”. Doctoral Theses — Medicine, Kiadó: Vrije Universiteit Amsterdam.
- ↑ Mount Sinai Hospital. Mount Sinai Hospital
- ↑ National Institute of Health. Surveillance, Epidemiology and End Results: SEER6215ch16
- ↑ National Cancer Institute, National Institute of Health. Surveillance, Epidemiology and End Results SEER - providing information on cancer statistics to help reduce the cancer burden on the US population
- ↑ Goff, BA; Mandel, L, Muntz, HG, Melancon, CH.: (2000. November). „"Ovarian carcinoma diagnosis.".”. Cancer 89 (10), 2068–75.. o.
- ↑ Bankhead CR, Kehoe ST, Austoker J.: ((July 2005).). „"Symptoms associated with diagnosis of ovarian cancer: a systematic review".”. BJOG 112 (7), 857–65.. o.
- ↑ Ryerson AB, Eheman C, Burton J, et al.: (2005. July). „"Symptoms, diagnoses, and time to key diagnostic procedures among older U.S. women with ovarian cancer".”. Obstet Gynecol 109 (5).
- ↑ a b Goff BA, Mandel LS, Melancon CH, Muntz HG (2004. june). „"Frequency of symptoms of ovarian cancer in women presenting to primary care clinics".” 291 (22), 2705–12. doi:10.1001/jama.291.22.2705. PMID 15187051. http://jama.ama-assn.org/cgi/pmidlookup?view=long&pmid=15187051. o.
- ↑ "Ovarian Cancer", 2010.
- ↑ Goff BA, Mandel LS, Drescher CW, et al.: (2007). „"Development of an ovarian cancer symptom index: possibilities for earlier detection"” (angol nyelven). Cancer 109 ((2)), 221–7.. o.
- ↑ Cancer.org: /Cancer/OvarianCancer/OverviewGuide/ovarian-cancer-overview-what-causes
- ↑ a b c Vo C, Carney ME: (2007. December). „"Ovarian cancer hormonal and environmental risk effect".”. Obstet. Gynecol. Clin. North Am. 34 (4), 687–700, viii. o.
- ↑ a b Bandera CA: (2005. June). „"Advances in the understanding of risk factors for ovarian cancer"”. J Reprod Med 50 (6), 399–406.. o.
- ↑ Lakhani SR, Manek S, Penault-Llorca F, et al. (2004. April). „"Pathology of ovarian cancers in BRCA1 and BRCA2 carriers"”. Clin. Cancer Res. 10 (7), 2473–81. o.
- ↑ Northwestern Memorial Hospital. "Ovarian Cancer Risk for Ashkenazi Women". Northwestern Memorial Hospital
- ↑ Wooster R, Weber BL (2003. june). „"Breast and Ovarian Cancer"”. N Engl J Med 348 (23), 2339-47. o.
- ↑ "Breast-cancer". Mayoclinic
- ↑ Hjartåker, A; Meo, MS, Weiderpass, E.: (2010. January). „"Alcohol and gynecological cancers: an overview"”. European journal of cancer prevention : the official journal of the European Cancer Prevention Organisation(ECP) 19 (1), 1–10. o.
- ↑ (2004. November) „"Milk link to ovarian cancer risk"”. BBC, Kiadó: BBC News.
- ↑ Lefkowitz ES, Garland CF.: (1994. December). „"Sunlight, vitamin D, and ovarian cancer mortality rates in US women"”. Int J Epidemiol 23 (6), 1133–6. o.
- ↑ Parenting: "Babysafety"
- ↑ Cancer.org: "Talcum powder"
- ↑ a b "Risk and causes"
- ↑ Dana-Farber, Harvard center, Daniel Cramer. „"Mumps Parotitis and Ovarian Cancer: modern significance of an historic association"”, Kiadó: Harvard Center.
- ↑ Finch A, Beiner M, Lubinski J, et al.: (2006). „"Salpingo-oophorectomy and the risk of ovarian, fallopian tube, and peritoneal cancers in women with a BRCA1 or BRCA2 Mutation"”. JAMA 296 (2), 185–92. o.
- ↑ "What are the risk factors for ovarian cancer?"
- ↑ "Ektomy". Univ California
- ↑ "Fallopian"
- ↑ Bast RC, Brewer M, Zou C, et al.: (2007). „"Prevention and early detection of ovarian cancer: mission impossible?"”. Recent Results Cancer Res 174, 91–100. o.
- ↑ {{Rossing, Mary Anne; Wicklund, Kristine G.; Cushing-Haugen, Kara L.; Weiss, Noel S. (2010-01-28). "Predictive Value of Symptoms for Early Detection of Ovarian Cancer". J Natl Cancer Inst. 102 (4): djp500v1. doi:10.1093/jnci/djp500. PMC 2826180. PMID 20110551. http://jnci.oxfordjournals.org/cgi/content/full/djp500v1
- ↑ FDA Clears a Test for Ovarian Cancer
- ↑ Dunn, J. D. (Ed.). Associated Title(s): PROTEOMICS – Clinical Applications. Online ISSN: 1615-9861
- ↑ {{Kosary, Carol L. (2007). "Chapter 16: Cancers of the Ovary". In Lin, LAG; Young, JL; Keel, GE et al.. SEER Survival Monograph: Cancer Survival Among Adults: US SEER Program, 1988-2001, Patient and Tumor Characteristics. SEER Program. NIH Pub. No. 07-6215. Bethesda, MD: National Cancer Institute. pp. 133–144. http://seer.cancer.gov/publications/survival/surv_ovary.pdf.}}
- ↑ Nincs adat
- ↑ Search "Krukenberg tumor" "Krukenberg". MedicineNet
- ↑ Bridda, A., Padoan, I., Mencarelli, R., Frego, M.:. „"Peritoneal mesothelioma: A review"”. MedGenMed. 9 (2), 32. o.
- ↑ FIGO. „http://www.cancerstaging.org/staging/index.html”. American Joint comittee on Cancer.
- ↑ How is ovarian cancer staged?. (Hozzáférés: 2011. augusztus 10.)
- ↑ a b c d Diagnosis and Staging. (Hozzáférés: 2010. július 27.)
- ↑ WHO Disease and injury country estimates. World Health Organization, 2009
- ↑ a b Jemal A, Siegel R, Ward E et al. (2008). „Cancer statistics, 2008”. CA Cancer J Clin 58 (2), 71–96. o. DOI:10.3322/CA.2007.0010. PMID 18287387.
- ↑ Stöppler, Melissa Conrad; Lee, Dennis; Shiel, William C. Jr., MD, FACP, FACR: "Ovarian cancer symptoms, early warning signs, and risk factors". (Hozzáférés: 2011. augusztus 8.)
- ↑ Robert C. Young.szerk.: Jameson JN, Kasper DL, Harrison TR, Braunwald E, Fauci AS, Hauser SL, Longo DL: Ch. 83, Gynecologic Malignancies, Harrison's principles of internal medicine, 16th, New York: McGraw-Hill Medical Publishing Division (2005). ISBN 0-07-140235-7
- ↑ b "Ovarian Cancer". The Merck Manual for Healthcare Professionals. November 2008. http://www.merckmanuals.com/professional/sec18/ch254/ch254b.html
- ↑ Surveillance, Epidemiology and End Results: SEER6215ch16
- ↑ a b c Clarke-Pearson DL (2009. July). „Clinical practice. Screening for ovarian cancer”. N. Engl. J. Med. 361 (2), 170–7. o. DOI:10.1056/NEJMcp0901926. PMID 19587342.
- ↑ Kurman RJ, Visvanathan K, Roden R, Wu TC, Shih IeM (2008. April). „Early detection and treatment of ovarian cancer: shifting from early stage to minimal volume of disease based on a new model of carcinogenesis”. Am. J. Obstet. Gynecol. 198 (4), 351–6. o. DOI:10.1016/j.ajog.2008.01.005. PMID 18395030.
- ↑ Partridge E, Kreimer AR, Greenlee RT, et al. (2009. April). „Results from four rounds of ovarian cancer screening in a randomized trial”. Obstet Gynecol 113 (4), 775–82. o. DOI:10.1097/AOG.0b013e31819cda77. PMID 19305319.
- ↑ Menon U, Gentry-Maharaj A, Hallett R, et al. (2009. April). „Sensitivity and specificity of multimodal and ultrasound screening for ovarian cancer, and stage distribution of detected cancers: results of the prevalence screen of the UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS)”. Lancet Oncol. 10 (4), 327–40. o. DOI:10.1016/S1470-2045(09)70026-9. PMID 19282241.
- ↑ Menon U, Gentry-Maharaj A, Hallett R, et al. (2009. April). „Sensitivity and specificity of multimodal and ultrasound screening for ovarian cancer, and stage distribution of detected cancers: results of the prevalence screen of the UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS)”. Lancet Oncol. 10 (4), 327–40. o. DOI:10.1016/S1470-2045(09)70026-9. PMID 19282241.
- ↑ Chobanian N, Dietrich CS (2008. April). „Ovarian cancer”. Surg. Clin. North Am. 88 (2), 285–99, vi. o. DOI:10.1016/j.suc.2007.12.002. PMID 18381114.
- ↑ Junor EJ, Hole DJ, McNulty L, Mason M, Young J (1999. November). „Specialist gynaecologists and survival outcome in ovarian cancer: a Scottish national study of 1866 patients”. Br J Obstet Gynaecol 106 (11), 1130–6. o. DOI:10.1111/j.1471-0528.1999.tb08137.x. PMID 10549956.
- ↑ Ehrlich, P.F., Teitelbaum, D.H., Hirschl, R.B., Rescorla, F. (2007). „Excision of large cystic ovarian tumors: combining minimal invasive surgery techniques and cancer surgery—the best of both worlds”. J. Pediatr. Surg. 42 (5), 890–3. o. DOI:10.1016/j.jpedsurg.2006.12.069. PMID 17502206.
- ↑ McGuire WP, Markman M (2003. December). „Primary ovarian cancer chemotherapy: current standards of care”. Br. J. Cancer 89 (Suppl 3), S3–8. o. DOI:10.1038/sj.bjc.6601494. PMID 14661040.
- ↑ Armstrong DK, Bundy B, Wenzel L, Huang HQ, et al. (2006. January). „Intraperitoneal Cisplatin and Paclitaxel in Ovarian Cancer”. NEJM 354 (1), 34–43. o. DOI:10.1056/NEJMoa052985. PMID 16394300.
- ↑ Ovarian Cancer Treatments Available. (Hozzáférés: 2010. augusztus 13.)
- ↑ b "Ovarian Cancer". The Merck Manual for Healthcare Professionals. November 2008. http://www.merckmanuals.com/professional/sec18/ch254/ch254b.html
- ↑ ^ a b c A New Test to See If Ovasses Are Cancerous - WSJ.com
- ↑ ^ a b c A New Test to See If Ovasses Are Cancerous - WSJ.com
- ↑ Catone G, Marino G, Mancuso R, Zanghì A (2004. April). „Clinicopathological features of an equine ovarian teratoma”. Reprod. Domest. Anim. 39 (2), 65–9. o. DOI:10.1111/j.1439-0531.2003.00476.x. PMID 15065985.
- ↑ Lefebvre R, Theoret C, Doré M, Girard C, Laverty S, Vaillancourt D (2005. November). „Ovarian teratoma and endometritis in a mare”. Can. Vet. J. 46 (11), 1029–33. o. PMID 16363331.
- ↑ Son YS, Lee CS, Jeong WI, Hong IH, Park SJ, Kim TH, Cho EM, Park TI, Jeong KS (2005. May). „Cystadenocarcinoma in the ovary of a Thoroughbred mare”. Aust. Vet. J. 83 (5), 283–4. o. DOI:10.1111/j.1751-0813.2005.tb12740.x. PMID 15957389.
- ↑ Frederico LM, Gerard MP, Pinto CR, Gradil CM (2007. May). „Bilateral occurrence of granulosa-theca cell tumors in an Arabian mare”. Can. Vet. J. 48 (5), 502–5. o. PMID 17542368.
- ↑ Hoque S, Derar RI, Osawa T, Taya K, Watanabe G, Miyake Y (2003. June). „Spontaneous repair of the atrophic contralateral ovary without ovariectomy in the case of a granulosa theca cell tumor (GTCT) affected mare” (– Scholar search). J. Vet. Med. Sci. 65 (6), 749–51. o. DOI:10.1292/jvms.65.749. PMID 12867740. [halott link]
- ↑ Sedrish SA, McClure JR, Pinto C, Oliver J, Burba DJ (1997. November). „Ovarian torsion associated with granulosa-theca cell tumor in a mare”. J. Am. Vet. Med. Assoc. 211 (9), 1152–4. o. PMID 9364230.
- ↑ Moll HD, Slone DE, Juzwiak JS, Garrett PD (1987). „Diagonal paramedian approach for removal of ovarian tumors in the mare”. Vet Surg 16 (6), 456–8. o. DOI:10.1111/j.1532-950X.1987.tb00987.x. PMID 3507181.
- ↑ Doran R, Allen D, Gordon B (1988. January). „Use of stapling instruments to aid in the removal of ovarian tumours in mares”. Equine Vet. J. 20 (1), 37–40. o. DOI:10.1111/j.2042-3306.1988.tb01450.x. PMID 2835223.
Kapcsolódó cikkek
- Cannistra SA (2004. December). „Cancer of the ovary”. N. Engl. J. Med. 351 (24), 2519–29. o. DOI:10.1056/NEJMra041842. PMID 15590954.
Külső linkek
- Ovarian cancer at the Open Directory Project
- Ovarian Cancer at American Cancer Society
- GeneReviews/NCBI/NIH/UW entry on BRCA1 and BRCA2 Hereditary Breast/Ovarian Cancer
- WebMD: Ovarian Cancer Health Center
- Medical Encyclopedia MayoClinc: Ovarian Cancer
- Interactive Health Tutorials Medline Plus: Ovarian cancer Using animated graphics and you can also listen to the tutorial
Fordítás
Ez a szócikk részben vagy egészben az Ovarian cancer című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.


