Klór-dioxid
| Klór-dioxid | |||
A klór-dioxid szerkezeti képlete |
 A klór-dioxid kalotta-modellje | ||

| |||
| IUPAC-név | klór-dioxid | ||
| Szabályos név | Dioxo-λ4-klorán (szubsztitutív) vagy dioxidoklór(•) (additív) | ||
| Más nevek | klór(IV)-oxid Kloril | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 10049-04-4 | ||
| PubChem | 24870 | ||
| ChemSpider | 23251 | ||
| EINECS-szám | 233-162-8 | ||
| MeSH | Chlorine+dioxide | ||
| ChEBI | 29415 | ||
| RTECS szám | FO3000000 | ||
| |||
| |||
| InChIKey | OSVXSBDYLRYLIG-UHFFFAOYSA-N | ||
| Gmelin | 1265 | ||
| UNII | 8061YMS4RM | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | ClO2 | ||
| Moláris tömeg | 67,45 g/mol | ||
| Megjelenés | sárgás-vöröses gáz | ||
| Szag | szúrós | ||
| Sűrűség | 2,757 g/dm³[1] | ||
| Olvadáspont | -59 °C | ||
| Forráspont | 11 °C | ||
| Oldhatóság (vízben) | 8 g/l (20 °C-on) | ||
| Oldhatóság | oldódik lúgokban és kénsavban | ||
| Savasság (pKa) | 3,0(5) | ||
| kH | 4,01·10−2 atm-cu m/mol | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH |
104,60 kJ/mol | ||
| Standard moláris entrópia S |
257,22 J K−1 mol−1 | ||
| Veszélyek | |||
| MSDS | ICSC 0127 | ||
| EU osztályozás | Oxidáló (O) Ártalmas (Xn) Nagyon mérgező (T+) Robbanásveszélyes (C) Veszélyes a környezetre (N) | ||
| EU Index | 017-026-00-3 | ||
| NFPA 704 | |||
| R mondatok | R6, R8, R26, R34, R50 | ||
| S mondatok | (S1/2), S23, S26, S28, S36/37/39, S38, S45, S61 | ||
| LD50 | 292 mg/kg (patkány, szájon át) | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A klór-dioxid szervetlen vegyület, képlete ClO2. Sárgászöld színű gáz, de −59 °C-on narancsszínű kristályokká fagy. A klór számos oxidjának egyike, hasznos és erős oxidálószer. A vizet is kezelik vele, de fehérítő hatása miatt is használják.[2] A vegyületben a klór +4-es oxidációs számú.
Szerkezete és kötései[szerkesztés]
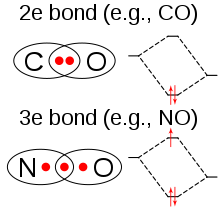

A klór-dioxid molekulában páratlan számú vegyértékelektron található, ezért paramágneses. Elektronszerkezetét a vegyészek sokáig nem értették, mert a Lewis-struktúrák közül egyik sem volt alkalmazható. 1933-ban Lawrence O. Brockway javaslata volt egy addig ismeretlen, háromelektronos kötésre vonatkozó hipotézis.[3] Az ötletet Linus Pauling kémikus fejlesztette tovább, és két rezonancia szerkezethez jutott, melyekben az egyik oldalon egy kettős kötés, a másikon egy egyszeres és egy háromelektronos kötés található.[4] Pauling úgy vélte, hogy az utóbbi némileg gyengébb a kettős kötésnél. A molekulapálya-elméletben ez a feltevés nyilvánvalónak látszik, ha a harmadik elektron lazítópályán helyezkedik el. A későbbi munkák megerősítették, hogy a legmagasabb betöltött molekulapálya valóban részlegesen betöltött pálya.[5]
Előállítása[szerkesztés]
A klór-dioxid rendkívül heves bomlásra képes, ha elválasztják az azt oldatban tartó anyagoktól (például víztől). Emiatt előállítása során gyakran előnyben részesítik azokat az eljárásokat, melyek révén oldatot nyernek, és nem jár gázállapotú termék keletkezésével. Használat közben is fokozott odafigyelést igényel.
Laboratóriumban nátrium-klorit klórral történő oxidációjával állítják elő:[6]
Napjainkban a klór-dioxid előállítása 95%-ban nátrium-klorátból (nátrium-hipokloritból) indul ki, és a papírgyártásban fehérítésre használják. Nagy hatékonyságú a nátrium-klorát redukciójának folyamata. Ehhez a nátrium-kloráthoz – erősen savas oldatban – megfelelő redukálószert, például metanolt, hidrogén-peroxidot, sósavat vagy kén-dioxidot adnak.[7] A modern technológiák metanolt vagy hidrogén-peroxidot használnak, egyrészt mert gazdaságos, másrészt mert nem képződik melléktermékként elemi klór. A teljes reakciót így írhatjuk fel:
klorátion + sav + redukálószer → klór-dioxid + melléktermékek
Klórsav és sósav reakciója az alábbi módon történik:
A kereskedelmi célra gyártott, jó minőségű klór-dioxid készítésekor a redukálószer metanol, a sav pedig kénsav. A klorid-alapú folyamatok mellőzésének előnyei, hogy a reakcióban nem képződik elemi klór, illetve hogy nátrium-szulfát, a cellulózüzemek számára értékes vegyszer lesz a melléktermék. Ez a metanol-alapú folyamat nagyon hatékony és biztonságos.[7]
Sokkal kisebb mennyiségben, de fertőtlenítőszerként is felhasználják a klór-dioxidot. 1999 óta a vízkezelésre és más, kisüzemi alkalmazásokra világszerte gyártott klór-dioxid egyre inkább a klorátos, hidrogén-peroxidos és kénsavas eljárással készül, mellyel klórmentes terméket lehet gyártani. Hagyományosan, a fertőtlenítésre használt klór-dioxid előállítása három módon történhet: nátrium-kloritból vagy a nátrium-kloritos és -hipokloritos eljárással:
Vagy egyszerűbben, nátrium-hipoklorit nélkül is, egy másik reakcióval.
Mindhárom folyamattal jó klór-dioxid kitermelés érhető el, de a klorit–sósav eljárásban – a többivel ellentétben – teljesen klórmentes klór-dioxid képződik, viszont azonos mennyiség előállításához 25%-kal több klorit felhasználását igényli. Kisüzemi alkalmazásra hidrogén-peroxiddal is hatékonyan előállítható.[7] Nagyon tiszta klór-dioxid nyerhető klorit-sók, például nátrium-klorit oldatának elektrolízisével.
Nagy tisztaságú klór-dioxid gáz állítható elő, ha kis koncentrációjú klórgázt reagáltatunk szilárd nátrium-klorittal. Az így nyert gáz – levegőre vagy nitrogénre vonatkoztatva – 7,7%-os töménységű.[8]
Kezelési útmutató[szerkesztés]
Ha a gázfázisú klór-dioxid és a levegő normál állapotú keverékében a klór-dioxid a aránya meghaladja a 30 térfogat%-ot (pontosabban ha a parciális nyomása 10 kPa fölé emelkedik[7]), robbanásszerűen szétbomolhat alkotóelemeire, klórra és oxigénre. A robbanást kiválthatja például fény, forró felület, lökéshullám, vagy akár kémiai reakció is. Ennélfogva, klór-dioxidot sohasem szabad nagy koncentrációban tárolni! A legtöbb esetben vízben oldva tárolják, viszont ez is literenkénti 0,5-10 grammban van korlátozva. Oldhatósága a hőmérséklet csökkenésével növekszik, ezért általában a vizet először lehűtik, és a hűtött vízben (5 °C) oldják fel, ha 3 gramm/liternél nagyobb koncentrációban akarják tárolni. Sok országban, például az USA-ban a klór-dioxidot semmiféle módon nem szabad szállítani, az előállítás helyszínén fel is kell használni. Erre használnak klór-dioxid generátorokat.[7] Néhány országban a klór-dioxid a törvények értelmében csak vízben oldva szállítható szárazföldön, koncentrációja maximum 3 gramm/liter, de ez viszonylag instabil, és gyorsan elbomlik. A klór-dioxid generátorok használata folyamatosan „megy ki a divatból” ipari szinten, mivel ezek a rendszerek a működésükhöz erős savakat használnak, órákat vesznek igénybe, a teljes hozamuk mégis csekély.
Felhasználásai[szerkesztés]
A klór-dioxidot elsősorban (>95%) a papírgyártás köztes termékének, az úgynevezett fapépnek a kifehérítésére, és a városi ivóvizek fertőtlenítésére (klórozására) használják.[9][10]
Fehérítés[szerkesztés]
A fapép (amiből később a papír készül) fehérítésére is használnak klórgázzal kevert klór-dioxidot. Klórmentes változatát (ECF / Elemental Chlorine-Free / Elemi klórtól mentes) is használják az anyagfehérítésre, néhol színtelenítésre. Mérsékelten savas kémhatás (pH 3,5–6) mellett használják. A klór-dioxid minimálisra csökkenti a klórtartalmú szerves vegyületek termelődését.[11] A klór-dioxid (az ECF technológia) világszerte a legelterjedtebb módszer a fehérítésre. A világon a nátroncellulóz előállítására több, mint 95%-ban az ECF-es fehérítést alkalmazzák.[12] Időnként lisztet is fehérítenek klór-dioxiddal.
Víz klórozása[szerkesztés]
A Niagara Fallsban, egy New York állami vízkezelő telep használt először klór-dioxidot az ivóvíz kezelésére 1944-ben, hogy lebontsák a vízben levő fenolt.[10] Az ivóvíz fertőtlenítésére 1956-tól terjedt el, amikor Brüsszelben (Belgium) áttértek a klór helyett a klór-dioxid használatára. Legáltalánosabban a klórozást megelőzően, előzetes oxidálószerként használják, hogy megsemmisítsék a természetes vizek szennyezőit, melyekből a szabad klór hatására trihalogénmetánok keletkeznének.[13][14][15] A trihalogénmetánok feltételezett rákkeltők, melyek a víz fertőtlenítése során melléktermékként keletkeznek[16] a nyersvízben található szerves anyagok klórozása során.[15] A klórnál hatásosabb 7-es pH felett,[10] ammónia és aminok jelenlétében,[forrás?] és/vagy a vízelosztó rendszerekben képződött biofilmek eltávolításában.[15] Számos ipari vízkezelési eljárásban alkalmazzák biocidként, például hűtőtornyokban, szennyvizek kezelésében és élelmiszerek feldolgozásában.[17]
A klórnál kevésbé korrozív, és a legionella baktériumok ellen hatásosabb szer.[18][19] Más másodlagos vízfertőtlenítési eljárásokhoz képest a klór-dioxid több előnnyel is rendelkezik: 1) az EPA által engedélyezett biocid, 2) hatását nem befolyásolja a pH 3) hatásossága nem csökken az idő múlásával (a baktériumok nem válnak rá rezisztenssé) és 4) nem csökkenti hatását a szilikátok és a foszfátok jelenléte, melyeket gyakran használnak korróziógátló inhibitorként az ivóvízben.
A legtöbb esetben a klórnál hatásosabb fertőtlenítő a víz által terjesztett patogén mikrobák, például a vírusok,[20] baktériumok és protozoák ellen.[10]
Egyéb felhasználások[szerkesztés]
Oxidálószerként használják szennyvizek fenoltartalmának lebontására, valamint az állati termékeket feldolgozó üzemek gáztisztító tornyaiban szagtalanításra.
Óvintézkedések és kiegészítések[szerkesztés]
A klór-dioxid mérgező, ezért határt kell szabni vele kapcsolatban, hogy a biztonságos felhasználását biztosítsák. Az Egyesült Államok Környezetvédelmi Hivatala az ivóvíz megengedhető klór-dioxidot tartalmát literenként legfeljebb 0,8 mg-ban maximálta. Az Egyesült Államok Munkaügyi Minisztériumának alárendelt Foglalkozás-biztonsági és Egészségvédelmi Hivatal (Occupational Safety and Health Administration), előírta, hogy a klór-dioxid megengedett, 8 órás foglalkozási expozíciós határértéke maximum 0,1 ppm (vagyis köbméterenként 0,3 milligramm) lehet a levegőben, az ilyen anyaggal szennyezett munkahelyeken.
Jegyzetek[szerkesztés]
- ↑ Haynes, William M.. Handbook of Chemistry and Physics, 91, Boca Raton, Florida: CRC Press, 4–58. o. (2010). ISBN 978-1439820773
- ↑ Chemistry of the Elements, 2nd, Butterworth-Heinemann, 844–849. o. (1997). ISBN 0080379419
- ↑ Brockway LO (1933. március 1.). „The Three-Electron Bond in Chlorine Dioxide”. Proc. Natl. Acad. Sci. U.S.A. 19 (3), 303–7. o. DOI:10.1073/pnas.19.3.303. PMID 16577512.
- ↑ Pauling, Linus. General chemistry. Mineola, NY: Dover Publications, Inc (1988). ISBN 0-486-65622-5
- ↑ (2006) „Core-level excitation and fragmentation of chlorine dioxide”. International Journal of Mass Spectrometry 249-250, 68–76. o. DOI:10.1016/j.ijms.2005.12.046.
- ↑ Derby, R. I.; Hutchinson, W. S. "Chlorine(IV) Oxide" Inorganic Syntheses, 1953, IV, 152-158.
- ↑ a b c d e Chlorine Oxides and Chlorine Oxygen Acids, Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. DOI: 10.1002/14356007.a06_483.pub2 (2010)
- ↑ White, George W.; Geo Clifford White. The handbook of chlorination and alternative disinfectants, 4th, New York: John Wiley (1999). ISBN 0-471-29207-9
- ↑ Thomas Wilson Swaddle. Inorganic chemistry: an industrial and environmental perspective. Academic Press, 198–199. o. (1997). ISBN 0-12-678550-3
- ↑ a b c d EPA Guidance Manual, chapter 4: Chlorine dioxide, US Environmental Protection Agency, <http://www.epa.gov/ogwdw/mdbp/pdf/alter/chapt_4.pdf>. Hozzáférés ideje: 2009-11-27
- ↑ E. Sjöström. Wood Chemistry: Fundamentals and Applications. Academic Press (1993). ISBN 0-12-647480-X. OCLC 58509724
- ↑ Archivált másolat. [2017. július 30-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. február 26.)
- ↑ (2005) „Trihalomethane formation during chemical oxidation with chlorine, chlorine dioxide and ozone of ten Italian natural waters”. Desalination 176 (1–3), 103–111. o. DOI:10.1016/j.desal.2004.10.022.
- ↑ (1996) „A pilot study on trihalomethane formation in water treated by chlorine dioxide (translated from Chinese)”. Zhonghua Yu Fang Yi Xue Za Zhi (Chinese journal of preventive medicine) 30 (1), 10–13. o. PMID 8758861.
- ↑ a b c (2002) „Implementation of chlorine dioxide disinfection: Effects of the treatment change on drinking water quality in a full-scale distribution system”. J. Environ. Eng. Sci. 1, 323–330. o. [2014. december 29-i dátummal az eredetiből archiválva]. DOI:10.1139/SO2-026. (Hozzáférés: 2009. november 27.)
- ↑ (1982) „Trihalomethanes as initiators and promoters of carcinogenesis”. Environ Health Perspect 46, 151–156. o. DOI:10.2307/3429432. PMID 7151756.
- ↑ (2002) „Chlorine dioxide wash of shrimp and crawfish an alternative to aqueous chlorine”. Food Microbiology 19 (4), 261–267. o. DOI:10.1006/fmic.2002.0493.
- ↑ Seymour Stanton Block. Disinfection, sterilization, and preservation, 5th, Lippincott Williams & Wilkins, 215. o. (2001). ISBN 0-683-30740-1
- ↑ (2007) „Safety and Efficacy of Chlorine Dioxide for Legionella control in a Hospital Water System”. Infection Control and Hospital Epidemiology 28 (8). [2011. július 19-i dátummal az eredetiből archiválva]. (Hozzáférés: 2009. november 27.)
- ↑ Ogata N, Shibata T (2008. január 1.). „Protective effect of low-concentration chlorine dioxide gas against influenza A virus infection”. J. Gen. Virol. 89 (Pt 1), 60–7. o. [2012. július 20-i dátummal az eredetiből archiválva]. DOI:10.1099/vir.0.83393-0. PMID 18089729. (Hozzáférés: 2014. május 13.)
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Chlorine dioxide című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.








