„Aszparagin” változatai közötti eltérés
| [ellenőrzött változat] | [ellenőrzött változat] |
kis korr, fordítás |
|||
| 1. sor: | 1. sor: | ||
{{chembox |
{{chembox |
||
| Watchedfields = changed |
|||
| verifiedrevid = 443663559 |
|||
| Name = <small>L</small>-Aszparagin |
| Name = <small>L</small>-Aszparagin |
||
| ImageFile = L-Asparagin - L-Asparagine.svg |
| ImageFile = L-Asparagin - L-Asparagine.svg |
||
| ImageSize = 200px |
| ImageSize = 200px |
||
| ImageAlt = |
| ImageAlt = Az L-aszparagin szerkezeti képlete |
||
| ImageFile1 = L-Asparagin phys.svg |
| ImageFile1 = L-Asparagin phys.svg |
||
| ImageSize1 = 220 |
| ImageSize1 = 220 |
||
| ImageAlt1 = |
| ImageAlt1 = Az ikerionos L-aszparagin molekulájának pálcika modellje |
||
| IUPACName = Asparagine |
| IUPACName = Asparagine |
||
| OtherNames = 2-amino-3- |
| OtherNames = 2-amino-3-karbamoilpropánsav |
||
|Section1={{Chembox Identifiers |
|Section1={{Chembox Identifiers |
||
| IUPHAR_ligand = 4533 |
| IUPHAR_ligand = 4533 |
||
| 41. sor: | 39. sor: | ||
| C=4 | H=8 | N=2 | O=3 |
| C=4 | H=8 | N=2 | O=3 |
||
| Appearance = színtelen kristályok |
| Appearance = színtelen kristályok |
||
| Density = 1 |
| Density = 1,543 g/cm<sup>3</sup> |
||
| MeltingPtC = 234 |
| MeltingPtC = 234 |
||
| BoilingPtC = 438 |
| BoilingPtC = 438 |
||
| Solubility = 2 |
| Solubility = 2,94 g/100 ml |
||
| SolubleOther = vízben, savakban, bázisokban oldódik, szerves oldószerekben nem |
| SolubleOther = vízben, savakban, bázisokban oldódik, szerves oldószerekben nem |
||
| pKa=2 |
| pKa=2,02 (karboxil), 8,80 (amino)<ref>{{Cite book|editor1=R. M. C. Dawson |editor2=Daphne Elliott |editor3=W. H. Elliott |editor4=K. M. Jones. Clarendon |title=Data for Biochemical Research|location=Oxford|publisher= Clarendon Press|year=1959|oclc=644267041}}</ref> |
||
| LogP = −3 |
| LogP = −3,82 |
||
}} |
}} |
||
|Section3={{Chembox Structure |
|Section3={{Chembox Structure |
||
| CrystalStruct = |
| CrystalStruct = rombos |
||
}} |
}} |
||
|Section4={{Chembox Thermochemistry |
|Section4={{Chembox Thermochemistry |
||
| DeltaHf = −789 |
| DeltaHf = −789,4 kJ/mol |
||
}} |
}} |
||
|Section7={{Chembox Hazards |
|Section7={{Chembox Hazards |
||
| 63. sor: | 61. sor: | ||
}} |
}} |
||
Az '''aszparagin''' (rövidítése '''Asn''' vagy '''N''') |
Az '''aszparagin''' (rövidítése '''Asn''' vagy '''N''') [[Aminosavak|α-aminosav]], egyike a [[Fehérje|fehérjéket]] felépítő húsz aminosavnak. [[Genetikai kód|Genetikai kódja]] AAU vagy AAC. |
||
A többi biológiailag aktív aminosavhoz hasonlóan az α-szénatomhoz kapcsolódik egy [[Karbonsavak|karboxil]] és egy [[Aminok|aminocsoport]], amelyek fiziológiás körülmények között ionos állapotban vannak. Oldallánca egy rövid karboxamid-csoport, amely a szervezet pH-ján nem ionos, de erősen poláros és hajlamos hidrogénkötések kialakítására. Hasonló szerkezetű, de egy szénatommal hosszabb oldalláncú molekula a [[glutamin]]. Az aszparagin nem esszenciális aminosav, vagyis az emberi szervezet képes előállítani. |
A többi biológiailag aktív aminosavhoz hasonlóan az α-szénatomhoz kapcsolódik egy [[Karbonsavak|karboxil-]] és egy [[Aminok|aminocsoport]], amelyek fiziológiás körülmények között ionos állapotban vannak. Oldallánca egy rövid karboxamid-csoport, amely a szervezet pH-ján nem ionos, de erősen poláros és hajlamos hidrogénkötések kialakítására. Hasonló szerkezetű, de egy szénatommal hosszabb oldalláncú molekula a [[glutamin]]. Az aszparagin nem esszenciális aminosav, vagyis az emberi szervezet képes előállítani. |
||
Az aszparagin a redukáló cukormolekulákkal magas hőmérsékleten [[ |
Az aszparagin a redukáló cukormolekulákkal magas hőmérsékleten [[Akrilamid|akrilamidot]] képez. A gyakorlatban ez azt jelenti, hogy a 120 °C fölött sütött szalmaburgonya, burgonyaszirom vagy pirítós kis mennyiségben rákkeltő akrilamidot tartalmazhat.<ref>http://www.cancer.gov/about-cancer/causes-prevention/risk/diet/acrylamide-fact-sheet#q7 Acrylamide in Food and Cancer Risk] ''National Cancer Isntitute''</ref> |
||
==Felfedezése== |
==Felfedezése== |
||
[[File:Gemuesespargel Klasse II 2008-05.jpg|thumb|left|Spárga]] |
[[File:Gemuesespargel Klasse II 2008-05.jpg|thumb|left|Spárga]] |
||
Az aszparagint először a francia [[Louis Nicolas Vauquelin]] és [[Pierre Jean Robiquet]] kristályosította ki a [[Közönséges spárga|spárga]] levéből 1806-ban.<ref>{{cite journal |title=La découverte d'un nouveau principe végétal dans le suc des asperges |vauthors=Vauquelin LN, Robiquet PJ |journal=Annales de Chimie |year=1806 |volume=57 |pages=88–93}}</ref><ref>{{cite book |author= R.H.A. Plimmer |editor1=R.H.A. Plimmer |editor2=F.G. Hopkins |title= The chemical composition of the proteins |url= http://books.google.com/?id=7JM8AAAAIAAJ&pg=PA112 |accessdate= January 18, 2010 |edition= 2nd |series= Monographs on biochemistry |volume= Part I. Analysis |origyear= 1908 |year= 1912 |publisher= Longmans, Green and Co. |location= London|page= 112}}</ref> Innen kapta az anyag a nevét is (''Asparagus'' = spárga). Az aszparagin volt az első izolált aminosav. Három évvel később Robiquet az [[Igazi édesgyökér| |
Az aszparagint először a francia [[Louis Nicolas Vauquelin]] és [[Pierre Jean Robiquet]] kristályosította ki a [[Közönséges spárga|spárga]] levéből 1806-ban.<ref>{{cite journal |title=La découverte d'un nouveau principe végétal dans le suc des asperges |vauthors=Vauquelin LN, Robiquet PJ |journal=Annales de Chimie |year=1806 |volume=57 |pages=88–93}}</ref><ref>{{cite book |author= R.H.A. Plimmer |editor1=R.H.A. Plimmer |editor2=F.G. Hopkins |title= The chemical composition of the proteins |url= http://books.google.com/?id=7JM8AAAAIAAJ&pg=PA112 |accessdate= January 18, 2010 |edition= 2nd |series= Monographs on biochemistry |volume= Part I. Analysis |origyear= 1908 |year= 1912 |publisher= Longmans, Green and Co. |location= London|page= 112}}</ref> Innen kapta az anyag a nevét is (''Asparagus'' = spárga). Az aszparagin volt az első izolált aminosav. Három évvel később Robiquet az [[Igazi édesgyökér|édesgyökérben]] talált nagyon hasonló vegyületet, amelyről [[Auguste-Arthur Plisson]] 1828-ban bebizonyította, hogy azonos az aszparaginnal.<ref>{{Cite book|url=http://www.henriettes-herb.com/eclectic/kings/glycyrrhiza.html|chapter=Glycyrrhiza (U. S. P.)—Glycyrrhiza|title=King's American Dispensatory|year=1898|author=Harvey Wickes Felter, M.D., and John Uri Lloyd, Phr. M., Ph. D.|publisher=Henriette's Herbal Homepage}}</ref> |
||
A szervezet képes előállítani de jelentősebb mennyiségben megtalálható a tejtermékekben, a húsban, a tojásban; a növények között a spárgában, burgonyában, hüvelyesekben, dióban, szójában és a teljes kiőrlésű lisztben. |
A szervezet képes előállítani de jelentősebb mennyiségben megtalálható a tejtermékekben, a húsban, a tojásban; a növények között a spárgában, burgonyában, hüvelyesekben, dióban, szójában és a teljes kiőrlésű lisztben. |
||
== Biokémiai jelentősége == |
== Biokémiai jelentősége == |
||
Az aszparagin oldallánca képes hidrogénkötést kialakítani a polipeptidek főláncával (gerincével) ezért a fehérjék másodlagos szerkezetében az alfa-hélixek és a béta-síkok végén visszaforduló hurokként (ún. asx-motívum) a struktúrák lezárásában játszik szerepet. |
Az aszparagin oldallánca képes hidrogénkötést kialakítani a polipeptidek főláncával (gerincével), ezért a fehérjék másodlagos szerkezetében az alfa-hélixek és a béta-síkok végén visszaforduló hurokként (ún. asx-motívum) a struktúrák lezárásában játszik szerepet. |
||
Az aszparaginoldallánc aminocsoportja a fehérjék glikozilálásának (poliszacharidlánccal való összekötésének) egyik színhelye. A glikozilációs pontok jellemzően olyan aszparaginok, amelynek C-oldali szomszédjai [[szerin]] vagy [[treonin]].<ref>{{cite book|last1=Brooker|first1=Robert|last2=Widmaier|first2=Eric|last3=Graham|first3=Linda|last4=Stiling|first4=Peter|last5=Hasenkampf|first5=Clare|last6=Hunter|first6=Fiona|last7=Bidochka|first7=Michael|last8=Riggs|first8=Daniel|title=Biology|date=2010|publisher=McGraw-Hill Ryerson|location=United States of America|isbn=978-0-07-074175-1|pages=105–106|edition=Canadian|chapter=Chapter 5: Systems Biology of Cell Organization}}</ref> |
Az aszparaginoldallánc aminocsoportja a fehérjék glikozilálásának (poliszacharidlánccal való összekötésének) egyik színhelye. A glikozilációs pontok jellemzően olyan aszparaginok, amelynek C-oldali szomszédjai [[szerin]] vagy [[treonin]].<ref>{{cite book|last1=Brooker|first1=Robert|last2=Widmaier|first2=Eric|last3=Graham|first3=Linda|last4=Stiling|first4=Peter|last5=Hasenkampf|first5=Clare|last6=Hunter|first6=Fiona|last7=Bidochka|first7=Michael|last8=Riggs|first8=Daniel|title=Biology|date=2010|publisher=McGraw-Hill Ryerson|location=United States of America|isbn=978-0-07-074175-1|pages=105–106|edition=Canadian|chapter=Chapter 5: Systems Biology of Cell Organization}}</ref> |
||
=== Bioszintézise === |
=== Bioszintézise === |
||
Az aszparagin a sejtekben [[Oxálecetsav|oxálecetsavból]] képződik, amire a [[transzamináz]] enzim egy [[glutaminsav]] |
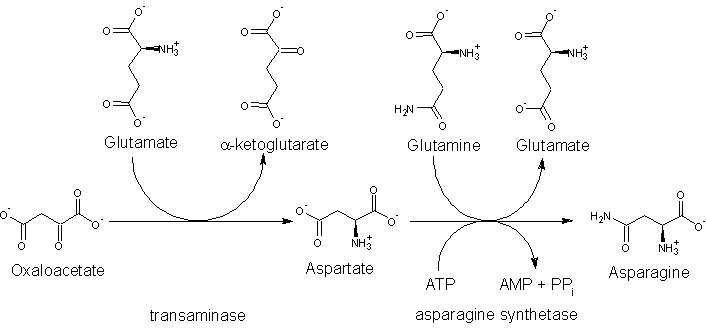
Az aszparagin a sejtekben [[Oxálecetsav|oxálecetsavból]] képződik, amire a [[transzamináz]] enzim egy [[glutaminsav]]molekuláról átviszi az aminocsoportot és ezáltal [[aszparaginsav]] (és [[α-ketoglutársav]]) keletkezik. Ezután az [[aszparagin-szintetáz]] enzim [[Adenozin-trifoszfát|ATP]] felhasználásával egy [[Glutamin|glutaminról]] helyez át egy aminocsoportot az aszparaginsavra, és a reakció eredményeképpen glutaminsav és aszparagin jön létre. |
||
[[Image:Asn biosynthesis.gif|frame|706px|center|Az aszparagin bioszintézise]] |
[[Image:Asn biosynthesis.gif|frame|706px|center|Az aszparagin bioszintézise]] |
||
== Lebontása == |
== Lebontása == |
||
Lebontása a szintézis fordítottjaként történik. Először az [[aszparagináz]] enzim eltávolítja róla az oldallánc aminocsoportját és aszparaginsav keletkezik. A következő lépésben másik aminocsoportja egy α-ketoglutársavra kerül át, és |
Lebontása a szintézis fordítottjaként történik. Először az [[aszparagináz]] enzim eltávolítja róla az oldallánc aminocsoportját és aszparaginsav keletkezik. A következő lépésben másik aminocsoportja egy α-ketoglutársavra kerül át, és oxálecetsav és glutamin keletkezik. Az oxálecetsav számos más folyamatba (például a [[Citromsavciklus|citrát-ciklusba]]) bekerülhet. |
||
== Források == |
== Források == |
||
A lap 2016. augusztus 23., 22:47-kori változata
| L-Aszparagin | |||

| |||

| |||
| IUPAC-név | Asparagine | ||
| Más nevek | 2-amino-3-karbamoilpropánsav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 70-47-3 | ||
| PubChem | 236 | ||
| ChemSpider | 6031 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C4H8N2O3 | ||
| Moláris tömeg | 132,12 g/mol | ||
| Megjelenés | színtelen kristályok | ||
| Sűrűség | 1,543 g/cm3 | ||
| Olvadáspont | 234 °C | ||
| Forráspont | 438 °C | ||
| Oldhatóság (vízben) | 2,94 g/100 ml | ||
| Oldhatóság | vízben, savakban, bázisokban oldódik, szerves oldószerekben nem | ||
| Savasság (pKa) | 2,02 (karboxil), 8,80 (amino)[1] | ||
| Megoszlási hányados | −3,82 | ||
| Kristályszerkezet | |||
| Kristályszerkezet | rombos | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH |
−789,4 kJ/mol | ||
| Veszélyek | |||
| NFPA 704 | |||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Az aszparagin (rövidítése Asn vagy N) α-aminosav, egyike a fehérjéket felépítő húsz aminosavnak. Genetikai kódja AAU vagy AAC.
A többi biológiailag aktív aminosavhoz hasonlóan az α-szénatomhoz kapcsolódik egy karboxil- és egy aminocsoport, amelyek fiziológiás körülmények között ionos állapotban vannak. Oldallánca egy rövid karboxamid-csoport, amely a szervezet pH-ján nem ionos, de erősen poláros és hajlamos hidrogénkötések kialakítására. Hasonló szerkezetű, de egy szénatommal hosszabb oldalláncú molekula a glutamin. Az aszparagin nem esszenciális aminosav, vagyis az emberi szervezet képes előállítani.
Az aszparagin a redukáló cukormolekulákkal magas hőmérsékleten akrilamidot képez. A gyakorlatban ez azt jelenti, hogy a 120 °C fölött sütött szalmaburgonya, burgonyaszirom vagy pirítós kis mennyiségben rákkeltő akrilamidot tartalmazhat.[2]
Felfedezése

Az aszparagint először a francia Louis Nicolas Vauquelin és Pierre Jean Robiquet kristályosította ki a spárga levéből 1806-ban.[3][4] Innen kapta az anyag a nevét is (Asparagus = spárga). Az aszparagin volt az első izolált aminosav. Három évvel később Robiquet az édesgyökérben talált nagyon hasonló vegyületet, amelyről Auguste-Arthur Plisson 1828-ban bebizonyította, hogy azonos az aszparaginnal.[5]
A szervezet képes előállítani de jelentősebb mennyiségben megtalálható a tejtermékekben, a húsban, a tojásban; a növények között a spárgában, burgonyában, hüvelyesekben, dióban, szójában és a teljes kiőrlésű lisztben.
Biokémiai jelentősége
Az aszparagin oldallánca képes hidrogénkötést kialakítani a polipeptidek főláncával (gerincével), ezért a fehérjék másodlagos szerkezetében az alfa-hélixek és a béta-síkok végén visszaforduló hurokként (ún. asx-motívum) a struktúrák lezárásában játszik szerepet.
Az aszparaginoldallánc aminocsoportja a fehérjék glikozilálásának (poliszacharidlánccal való összekötésének) egyik színhelye. A glikozilációs pontok jellemzően olyan aszparaginok, amelynek C-oldali szomszédjai szerin vagy treonin.[6]
Bioszintézise
Az aszparagin a sejtekben oxálecetsavból képződik, amire a transzamináz enzim egy glutaminsavmolekuláról átviszi az aminocsoportot és ezáltal aszparaginsav (és α-ketoglutársav) keletkezik. Ezután az aszparagin-szintetáz enzim ATP felhasználásával egy glutaminról helyez át egy aminocsoportot az aszparaginsavra, és a reakció eredményeképpen glutaminsav és aszparagin jön létre.
Lebontása
Lebontása a szintézis fordítottjaként történik. Először az aszparagináz enzim eltávolítja róla az oldallánc aminocsoportját és aszparaginsav keletkezik. A következő lépésben másik aminocsoportja egy α-ketoglutársavra kerül át, és oxálecetsav és glutamin keletkezik. Az oxálecetsav számos más folyamatba (például a citrát-ciklusba) bekerülhet.
Források
- ↑ Data for Biochemical Research. Oxford: Clarendon Press (1959). OCLC 644267041
- ↑ http://www.cancer.gov/about-cancer/causes-prevention/risk/diet/acrylamide-fact-sheet#q7 Acrylamide in Food and Cancer Risk] National Cancer Isntitute
- ↑ (1806) „La découverte d'un nouveau principe végétal dans le suc des asperges”. Annales de Chimie 57, 88–93. o.
- ↑ R.H.A. Plimmer. The chemical composition of the proteins, 2nd, Monographs on biochemistry, London: Longmans, Green and Co., 112. o. [1908] (1912). Hozzáférés ideje: 2010. január 18.
- ↑ Harvey Wickes Felter, M.D., and John Uri Lloyd, Phr. M., Ph. D.. Glycyrrhiza (U. S. P.)—Glycyrrhiza, King's American Dispensatory. Henriette's Herbal Homepage (1898)
- ↑ Chapter 5: Systems Biology of Cell Organization, Biology, Canadian, United States of America: McGraw-Hill Ryerson, 105–106. o. (2010. május 11.). ISBN 978-0-07-074175-1
Ez a szócikk részben vagy egészben az Asparagine című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.

