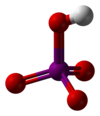
Perjódsav
| perjódsav | |||
 |

| ||

| |||
 |
| ||
| Más nevek | jód(VII) sav, hidrogén-perjodát | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 10450-60-9 | ||
| ChemSpider | 23622 | ||
| |||
| |||
| UNII | AK1D44L87G | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | HIO4 (metaperjódsav) H5IO6 (ortoperjódsav) | ||
| Moláris tömeg | 227,941 g/mol (H5IO6) 190.91 g/mol (HIO4) | ||
| Megjelenés | színtelen kristályok | ||
| Olvadáspont | 128,5 °C | ||
| Oldhatóság | oldódik vízben, alkoholokban | ||
| Veszélyek | |||
| EU osztályozás | oxidálószer (O), mérgező (T), korrozív (C) | ||
| NFPA 704 | |||
| R mondatok | R23 R24 R25 R34 R41 | ||
| Rokon vegyületek | |||
| Azonos kation | perklórsav HClO4, perbrómsav HBrO4, permangánsav HMnO4, tellúrsav Te(OH)6, perxenonsav Xe(OH)6 | ||
| Azonos anion | nátrium-perjodát, kálium-perjodát | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A perjódsav a jód legmagasabb oxidációs számú oxosava, benne a jód oxidációs száma VII. A perjodátokhoz hasonlóan két formája létezik: ortoperjódsav, ennek kémiai képlete H5IO6, illetve a metaperjódsav, HIO4.
Heinrich Gustav Magnus és C. F. Ammermüller fedezte fel 1833-ban.[2]
Szintézise[szerkesztés]
A modern ipari eljárás a jódsav elektrokémiai oxidációja PbO2 anódon:
Az ortoperjódsav 100 °C-ra történő melegítéssel metaperjódsavvá dehidratálható:
- HIO4 + 2 H2O ⇌ H5IO6
További, mintegy 150 °C-ra történő melegítés hatására nem a várt dijód-heptoxid (I2O7) anhidrid, hanem jód-pentoxid (I2O5) keletkezik. Metaperjódsav különböző ortoperjodátokból is előállítható híg salétromsavas kezeléssel.[4]
- H5IO6 → HIO4 + 2 H2O
Tulajdonságai[szerkesztés]
Az ortoperjódsavnak több savi disszociációs állandója is van.[5][6] A metaperjódsav pKa-ja nem ismert.
- H5IO6 ⇌ H4IO−6 + H+, pKa = 3,29
- H4IO−6 ⇌ H3IO2−6 + H+, pKa = 8,31
- H3IO2−6 ⇌ H2IO3−6 + H+, pKa = 11,60
Mivel a perjódsavnak két formája van, ebből következően kétféle perjodát sót képez. A nátrium-metaperjodát (NaIO4) például HIO4-ból állítható elő, míg a nátrium-ortoperjodát (Na5IO6) szintézise H5IO6-ból valósítható meg.
Szerkezete[szerkesztés]
Az ortoperjódsav monoklin kristályokat alkot (tércsoportja P21/n), melyekben a kissé deformált IO6 oktaédereket hídhelyzetű hidrogének kapcsolják össze.[7] A metaperjódsav kristályaiban is IO6 oktaéderek találhatók, ezek azonban közös cisz-élek révén kapcsolódó hídhelyzetű oxigénatomokkal egydimenziós végtelen láncot alkotnak.[8]
Reakciói[szerkesztés]
Mint minden perjodát, a perjódsav is felhasználható különböző 1,2-difunkciós vegyületek felhasítására (Malaprade-reakció). Ezek közül az egyik legnevezetesebb a vicinális diolok két aldehidre vagy ketonra történő hasadása.

Ez a reakció felhasználható a szénhidrátok szerkezetének meghatározására, mivel a perjódsav fel tudja nyitni a szacharidok gyűrűit. Ezt az eljárást gyakran használják a szacharidok fluoreszcens vagy más molekulával, például biotinnal történő megjelöléséhez. Mivel a reakciót vicinális diolok adják, a perjodátos oxidációt gyakran felhasználják az RNS 3′-végének szelektív megjelölésére (a ribóz vicinális diol, ugyanakkor a DNS-ben levő dezoxiribózban nincs vicinális diol funkció).
A perjódsavat ezen kívül közepes erősségű oxidálószerként is használják.
Más oxosavak[szerkesztés]
A perjódsav egyike a jód oxosavainak, melyekben a jód oxidációs száma +1, +3, +5 vagy +7 lehet. A jódnak számos semleges oxidja is létezik.
| A jód oxidációs száma | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Név | hidrogén-jodid | hipojódossav | jódossav | jódsav | perjódsav |
| Képlet | HI | HIO | HIO2 | HIO3 | HIO4 vagy H5IO6 |
Jegyzetek[szerkesztés]
- ↑ Aylett, founded by A.F. Holleman ; continued by Egon Wiberg ; translated by Mary Eagleson, William Brewer ; revised by Bernhard J.. Inorganic chemistry, 1st English ed., [edited] by Nils Wiberg., San Diego, Calif. : Berlin: Academic Press, W. de Gruyter., 453. o. (2001). ISBN 0123526515
- ↑ Ammermüller, F. (1833). „Ueber eine neue Verbindung des Jods mit Sauerstoff, die Ueberjodsäure” (german nyelven). Annalen der Physik und Chemie 104 (7), 514–525. o. DOI:10.1002/andp.18331040709.
- ↑ Parsons, Roger. Handbook of electrochemical constants. Butterworths Scientific Publications Ltd, 71. o. (1959)
- ↑ Riley, edited by Georg Brauer; translated by Scripta Technica, Inc. Translation editor Reed F.. Handbook of preparative inorganic chemistry. Volume 1, 2nd, New York, N.Y.: Academic Press, 323–324. o. (1963). ISBN 012126601X
- ↑ Aylett, founded by A.F. Holleman; continued by Egon Wiberg; translated by Mary Eagleson, William Brewer; revised by Bernhard J.. Inorganic chemistry, 1st English ed., [edited] by Nils Wiberg., San Diego, Calif. : Berlin: Academic Press, W. de Gruyter., 454. o. (2001). ISBN 0123526515
- ↑ Burgot, Jean-Louis. Ionic equilibria in analytical chemistry. New York: Springer, 358. o.. ISBN 1441983821
- ↑ Feikema, Y. D. (1966. június 10.). „The crystal structures of two oxy-acids of iodine. I. A study of orthoperiodic acid, H5IO6, by neutron diffraction”. Acta Crystallographica 20 (6), 765–769. o. DOI:10.1107/S0365110X66001828.
- ↑ Kraft, Thorsten (1997. szeptember 1.). „Crystal Structure Determination of Metaperiodic Acid, HIO4, with Combined X-Ray and Neutron Diffraction”. Angewandte Chemie International Edition in English 36 (16), 1753–1754. o. DOI:10.1002/anie.199717531.
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben a Periodic acid című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.

