Benzil
| Benzil | |||
 Benzil | |||
| |||
| |||
| IUPAC-név | 1,2-difeniletán-1,2-dion | ||
| Más nevek | dibenzoil bibenzoil difenilglioxál | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 134-81-6 | ||
| PubChem | 8651 | ||
| ChemSpider | 8329 | ||
| ChEBI | 51507 | ||
| |||
| |||
| InChIKey | WURBFLDFSFBTLW-UHFFFAOYSA-N | ||
| ChEMBL | 189886 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C14H10O2 | ||
| Moláris tömeg | 210,23 g/mol | ||
| Megjelenés | sárga kristályok vagy por | ||
| Sűrűség | 1,23 g/cm³ (szilárd) (1,255 g/cm³, röntgen) | ||
| Olvadáspont | 94-96 °C, 401-402 K | ||
| Forráspont | 346–348 °C, 619–621 K | ||
| Oldhatóság (vízben) | oldhatatlan | ||
| Oldhatóság (etanol) | oldódik | ||
| Oldhatóság (dietil-éter) | oldódik | ||
| Oldhatóság (benzol) | oldódik | ||
| Kristályszerkezet | |||
| Kristályszerkezet | P31,221[1] | ||
| Dipólusmomentum | 3,8 D[2] | ||
| Veszélyek | |||
| Főbb veszélyek | irritáló | ||
| NFPA 704 | |||
| Rokon vegyületek | |||
| Rokon diketonok | diacetil | ||
| Rokon vegyületek | benzofenon glioxál bibenzil | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A benzil (szisztematikus nevén 1,2-difeniletán-1,2-dion) szerves vegyület, képlete (C6H5CO)2, melyet gyakori rövidítéssel (PhCO)2-nek is írnak. Ez a sárga színű anyag az egyik legelterjedtebb diketon. Főként a polimerkémiában használják fotoiniciátorként.[3]
Szerkezete[szerkesztés]
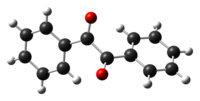
A benzil legfigyelemreméltóbb szerkezeti sajátossága a hosszú (154 pm-es) szén–szén kötés, mely azt jelzi, hogy a két karbonil szén között nincs pi-kötés. A PhCO centrumok síkalkatúak, de a benzoilcsoportok egymáshoz képest el vannak fordulva, a diéderes szög 117°.[4] Sztérikusan kevésbé gátolt analógok esetén (glioxál, diacetil, oxálsav-származékok) a két (RCO)2-csoport síkalkatú anti-konformációt vesz fel.
Felhasználása[szerkesztés]
A benzilt nagyrészt polimerek gyökös térhálósítására használják. A benzil ultraibolya sugárzás hatására bomlik, így az anyagban szabad gyökök keletkeznek, melyek elősegítik a keresztkötések kialakulását. Nemrégiben kimutatták, hogy a benzil hatásosan gátolja az emberi karboxilészteráz enzimeket, melyek a karbonsav-észterek és számos klinikailag használt gyógyszer hidrolízisében vesznek részt.[5]
Reakciói[szerkesztés]
A benzilt a szerves szintézisekben használják. Aminokkal kondenzációs reakcióban diketimin ligandumokká alakul. A benzil egyik klasszikus szerves kémiai reakciója a benzilsav-átrendeződés, ez a benzil benzilsavvá történő báziskatalizált átrendeződése. Ezt a reakciót használják ki a fenitoin nevű gyógyszer-hatóanyag gyártásában. A benzil 1,3-difenilacetonnal aldolkondenzációs reakcióba lép, ennek során tetrafenilciklopentadienon keletkezik.
Előállítása[szerkesztés]
A benzilt benzoinból állítják elő, a benzoint benzaldehidből lehet nyerni benzoin kondenzáció révén.[6]
- PhC(O)CH(OH)Ph + 2 Cu2+ → PhC(O)C(O)Ph + 2 H+ + 2 Cu+
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Benzil című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások[szerkesztés]
- ↑ Acta Cryst. B43 398 (1987)
- ↑ Spectrochim. Acta A60 (8-9) 1805 (2004)
- ↑ Hardo Siegel, Manfred Eggersdorfer "Ketones" in Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, 2002 by Wiley-VCH, Weinheim. doi:10.1002/14356007.a15_077
- ↑ Quang. Shen, Kolbjoern. Hagen "Gas-phase molecular structure and conformation of benzil as determined by electron diffraction" J. Phys. Chem., 1987, 91 (6), pp 1357–1360. doi:10.1021/j100290a017.
- ↑ Wadkins. R. M. et al "Identification and characterization of novel benzil (diphenylethane-1,2-dione) analogues as inhibitors of mammalian carboxylesterases. J. Med. Chem., 2005 48 pp 2906–15.
- ↑ Clarke, H. T.; Dreger.E. E. (1941). „Benzil”. Org. Synth.. ; Coll. Vol. 1: 87

