Fenilalanin
| Fenilalanin | |||
 |

| ||
| IUPAC-név | (S)-2-amino-3-fenilpropánsav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| Rövidítés | Phe, F | ||
| CAS-szám | 63-91-2 | ||
| EINECS-szám | 200-568-1 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C9H11NO2 | ||
| Moláris tömeg | 165,19 g/mol | ||
| Sűrűség | 1,29 g/cm³ | ||
| Olvadáspont | 283 °C | ||
| Savasság (pKa) | 2,20 9,09 | ||
| Izoelektromos pont | 5,48 | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A fenilalanin egy aminosav, melynek α-helyzetű szénatomjához egy benzil oldallánc kapcsolódik.


Az l-fenilalanin (l-Phe) a fehérjéket alkotó 22 aminosav egyike. Enantiomer párja a d-fenilalanin (d-Phe), mesterségesen állítható elő.
(Érdekes megemlíteni, hogy a fehérjealkotó l-Phe keserű ízű, a d-Phe pedig édes.)
Esszenciális aminosav, vagyis nem rendelkezünk az előállításához szükséges enzimekkel, a táplálékból kell felvennünk. Megtalálható a fehérjékben, például a tej kazeinje. Antidepresszáns és fájdalomcsillapító hatása miatt táplálékkiegészítőként is forgalmazzák.
Az l-fenilalanin (l-Phe) szubsztrátja a Phe-hidroxiláz enzimnek, mely enzim a Phe aromás oldalláncát hidroxilálja, így képez l-para-tirozint (l-p-Tyr), amely, amellett, hogy szintén fehérjealkotó aminosav, a pajzsmirigyhormonok, a melaninpigmentek, a katekolamin hormonok előanyaga. A Phe-hidroxiláz nem képes a d-Phe-t felhasználni. A Phe aromás oldallánca szabad gyökös reakciókban is módosulhat, ekkor a para- (p-) izoforma mellett meta- (m-) és orto-tirozin (o-Tyr) is képződik. Mivel az l-p-Tyr enzimatikusan is képződhet, a másik két sztereoizomer, illetve a d-Phe-ból képződő d-p-Tyr, d-m-Tyr, d-o-Tyr használhatók szabad gyökös folyamatok markereként.
A fenilketonuria (PKU) betegségben szenvedőknél hiányzik vagy nem működik a Phe-hidroxiláz enzim. Ennek hiányában a Phe hidroxileződés helyett lassú transzaminálódáson megy keresztül, aminek a terméke a fenilpiroszőlősav, amely vagy a jellegzetes illatú fenilecetsavvá dekarboxileződik vagy feniltejsavvá redukálódik. Ők nem fogyaszthatnak fenilalanint, illetve fenilalanin-forrást jelentő anyagokat (például Aspartam/Nutra Sweet).
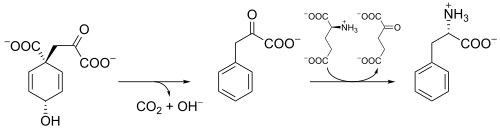
Bioszintézis[szerkesztés]