p-toluolszulfonsav
| p-toluolszulfonsav[1] | |||
 p-toluolszulfonsav | |||
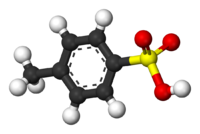
| |||
| IUPAC-név | 4-metilbenzolszulfonsav | ||
| Más nevek | tozilsav PTSA | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 104-15-4, 6192-52-5 (monohidrát) | ||
| PubChem | 6101 | ||
| ChemSpider | 5876 | ||
| DrugBank | DB03120 | ||
| KEGG | C06677 | ||
| ChEBI | 27849 | ||
| |||
| |||
| InChIKey | JOXIMZWYDAKGHI-UHFFFAOYSA-N | ||
| ChEMBL | 541253 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | CH3C6H4SO3H | ||
| Moláris tömeg | 172,20 g/mol (anhidrát) 190,22 g/mol (monohidrát) | ||
| Megjelenés | színtelen (fehér) szilárd anyag | ||
| Sűrűség | 1,24 g/cm³ | ||
| Olvadáspont | 38 °C, 311 K (anhidrát)[2] 103–106 °C, 376–379 K (monohidrát) | ||
| Forráspont | 140 °C (20 Hgmm nyomáson) | ||
| Oldhatóság (vízben) | 67 g/100 ml | ||
| Savasság (pKa) | −2,8 (vízben),[3] 8,5 (acetonitrilben)[4] | ||
| Kristályszerkezet | |||
| Molekulaforma | a kénatom körül torzult tetraéderes | ||
| Veszélyek | |||
| MSDS | External MSDS | ||
| Főbb veszélyek | a bőrt irritálja | ||
| R mondatok | R36/37/38 | ||
| S mondatok | S26 | ||
| Rokon vegyületek | |||
| Rokon szulfonsavak | benzolszulfonsav szulfanilsav | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A p-toluolszulfonsav vagy tozilsav (TsOH) az aromás szulfonsavak közé tartozó szerves vegyület, képlete CH3C6H4SO3H. Vízben, alkoholokban és más poláros szerves oldószerekben oldódó fehér szilárd anyag. A 4-CH3C6H4SO2– csoportot tozilcsoportnak is nevezik és gyakran Ts vagy Tos rövidítéssel jelölik. A TsOG többnyire a monohidrátot (TsOH·H2O) jelöli.
A TsOH erős szerves sav, a benzoesavnál mintegy egymilliószor erősebb sav. Egyike a kisszámú szilárd erős savaknak, így mennyisége egyszerűen (tömegméréssel) mérhető. Ugyanakkor néhány erős szervetlen savtól (például salétromsav, kénsav és perklórsav) eltérően a TsOH nem oxidálószer.
Előállítása és kezelése[szerkesztés]
A TsOH-t ipari léptékben a toluol szulfonálásával állítják elő. Könnyen hidratálódik. Gyakori szennyezői a benzolszulfonsav és a kénsav. A szennyezők eltávolítása tömény vizes oldatból történő újrakristályosítással majd azt követő toluolos azeotróp szárítással történhet.[5]
A toluolszulfonsavat a szerves kémiai szintézisekben mint szerves anyagokban oldódó savkatalizátort alkalmazzák. Példák a felhasználására:
- Acetál előállítása aldehidből.[6]
- Karbonsavak észteresítése.[7]
- Észter átészteresítése.[8]
Tozilát-észterek[szerkesztés]

A tozilát-észtereket alkilezőszerként használják, mivel a tozilcsoport elektronszívó hatása miatt a tozilát anion jó távozó csoport. A tozilcsoportot alkoholok és aminok védésére is használják. Az alkoholt 4-toluolszulfonil-kloriddal reagáltatják, rendszerint aprotikus oldószerben, többnyire piridinben, melynek bázikussága segíti a reakciót.[9] A toluolszulfonát-észterek nukleofil szubsztitúciós vagy eliminációs reakciókban vesznek részt. A tozilát-észterek redukciójával a megfelelő szénhidrogén keletkezik. Ily módon az alkoholok tozilálásával, majd azt követő redukcióval az alkoholból eltávolítható az oxigénatom.
Reakciói[szerkesztés]
A p-toluolszulfonsav foszfor-pentoxiddal történő hevítéssel p-toluolszulfonsav-anhidriddé alakítható.[10] Ha a TsOH-t (bármely izomert) savval és vízzel forraljuk, toluol keletkezik:
- CH3C6H4SO3H + H2O → C6H5CH3 + H2SO4
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a P-Toluenesulfonic acid című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások[szerkesztés]
- ↑ Merck Index, 11th Edition, 9459.
- ↑ Armarego, Wilfred. Purification of Laboratory Chemicals. Elsevier Science, 370. o. (2003). ISBN 0-7506-7571-3
- ↑ Guthrie, J. P. Hydrolysis of esters of oxy acids: pKa values for strong acids. Can. J. Chem. 1978, 56, 2342-2354.
- ↑ Eckert, F.; Leito, I.; Kaljurand, I.; Kütt, A.; Klamt, A.; Diedenhofen, M. Prediction of Acidity in Acetonitrile Solution with COSMO-RS. J. Comput. Chem. 2009, 30, 799-810. doi:10.1002/jcc.21103
- ↑ Perrin, D. D. and Armarego, W. L. F., Purification of Laboratory Chemicals, Pergamon Press: Oxford, 1988.
- ↑ H. Griesser, H.; Öhrlein, R.; Schwab, W.; Ehrler, R.; Jäger, V. (2004). „3-Nitropropanal, 3-Nitropropanol, and 3-Nitropropanal Dimethyl Acetal”. Org. Synth.. ; Coll. Vol. 10: 577
- ↑ Furuta, K. Gao, Q.-z.; Yamamoto, H. (1998). „Chiral (Acyloxy)borane Complex-catalyzed Asymmetric Diels-Alder Reaction: (1R)-1,3,4-Trimethyl-3-cyclohexene-1-carboxaldehyde”. Org. Synth.. ; Coll. Vol. 9: 722
- ↑ Imwinkelried, R.; Schiess, M.; Seebach, D. (1993). „Diisopropyl (2S,3S)-2,3-O-isopropylidenetartrate”. Org. Synth.. ; Coll. Vol. 8: 201
- ↑ Nucleophilic Substitution
- ↑ L. Field and J. W. McFarland (1963). „p-Toluenesulfonic Anhydride”. Org. Synth.. ; Coll. Vol. 4: 940
