Glutársav
| glutársav | |||
| |||

| |||
| Más nevek | glutársav propán-1,3-dikarbonsav 1,3-propándikarbonsav pentándisav n-piroborkősav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 110-94-1 | ||
| PubChem | 743 | ||
| ChemSpider | 723 | ||
| EINECS-szám | 203-817-2 | ||
| DrugBank | DB03553 | ||
| KEGG | C00489 | ||
| ChEBI | 17859 | ||
| |||
| |||
| InChIKey | JFCQEDHGNNZCLN-UHFFFAOYSA-N | ||
| ChEMBL | 1162495 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C5H8O4 | ||
| Moláris tömeg | 132,12 g/mol | ||
| Megjelenés | színtelen, szilárd anyag | ||
| Sűrűség | 1,42 g·cm−3[1] | ||
| Olvadáspont | 97,5 °C[1] | ||
| Forráspont | 303 °C[1] | ||
| Oldhatóság (vízben) | 640 g·l−1 (20 °C-on)[1] | ||
| Oldhatóság | etanol, dietil-éter, kloroform, benzol | ||
| Savasság (pKa) | pKs1 = 4,32 (18 °C)[3] pKs2 = 5,42 (25 °C)[3] | ||
| Törésmutató (nD) | 1,4188 (106 °C)[4] | ||
| Gőznyomás | 2,2 Pa (18,5 °C)[2] | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
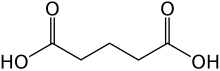
A glutársav szerves vegyület, alifás dikarbonsav, képlete C3H6(COOH)2. Míg a hozzá hasonló, a szénlánc hosszában egy szénatommal különböző adipin- és borostyánkősav vízben szobahőmérsékleten csak néhány százalékban oldódik, a glutársav oldhatósága 50% (m/m) feletti.
A szó a latin gluten (enyv) és tartarum (üledék, borkő), közvetve a görög tartaron (τάρταρον) szó összetételéből származik.[5]
Biokémiája[szerkesztés]
A testben természetes úton keletkezik egyes aminosavak, például a lizin és a triptofán lebontása során.
Előállítása[szerkesztés]
Butirolakton kálium-cianiddal történő gyűrűnyitásával állítható elő, melynek során a vegyes kálium karboxilát-nitrilből hidrolízissel nyerhető a dikarbonsav.[6] Másik lehetőségként dihidropirán hidrolízisét követő oxidációval is előállítható. Előállítható még 1,3-dibrómpropánból kiindulva nátrium- vagy kálium-cianidos kezeléssel, majd az így kapott dinitril hidrolízisével.
Felhasználása[szerkesztés]
- polimerek, például poliészterek, poliolok, poliamidok gyártásához
- hidrogénezéssel 1,5-pentándiol állítható elő belőle, melyet lágyítószerként és poliészterek gyártásához használnak fel[7]
Jegyzetek[szerkesztés]
- ↑ a b c d A 110-94-1 CAS-számhoz tartozó bejegyzés az IFA GESTIS adatbázisából. (JavaScript szükséges) (angolul).
- ↑ Biztonságtechnikai adatlap (német nyelven) [1]
- ↑ a b David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Edition. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Dissociation Constants of Organic Acids and Bases, 8-44. o.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Edition. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, 3-268. o.
- ↑ Fülöp József: Rövid kémiai értelmező és etimológiai szótár. Celldömölk: Pauz–Westermann Könyvkiadó Kft. 1998. 57. o. ISBN 963 8334 96 7
- ↑ G. Paris, L. Berlinguet, R. Gaudry, J. English, Jr. and J. E. Dayan (1963). „Glutaric Acid and Glutaramide”. Org. Synth.. ; Coll. Vol. 4: 496
- ↑ Peter Werle and Marcus Morawietz "Alcohols, Polyhydric" in Ullmann's Encyclopedia of Industrial Chemistry: 2002, Wiley-VCH: Weinheim. doi:10.1002/14356007.a01_305
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Glutaric acid című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
