„Difénsav” változatai közötti eltérés
Új oldal, tartalma: „{{Chembox | ImageFile = Diphenic Acid Structural Formula V.1.svg | ImageSize = | ImageAlt = | PIN = [1,1′-Bifenil]-2,2′-dikarbonsav | OtherNames = 2,2'-dibenzoesav |Section1={{Chembox Identifiers | CASNo = 482-05-3 | PubChem = 10210 | EC_number = 207-576-4 | UNII = QY5X735ZIM | ChEBI = 23837 | ChEMBL = 79411 | Gmelin = 536420 | ChemSpiderID = 9795 | StdInChI=1S/C14H10O4/c15-13(16)11-7-3-1-5-9(11)10-6-2-4-8-12(10)14(17)18/h1-8H,(H,15,16)(H,17,18) | StdInChIKe…” |
(Nincs különbség)
|
A lap 2023. október 2., 09:05-kori változata
| Difénsav | |||
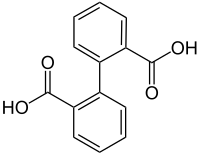
| |||
| Más nevek | 2,2'-dibenzoesav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 482-05-3 | ||
| PubChem | 10210 | ||
| ChemSpider | 9795 | ||
| ChEBI | 23837 | ||
| |||
| InChIKey | GWZCCUDJHOGOSO-UHFFFAOYSA-N | ||
| Gmelin | 536420 | ||
| UNII | QY5X735ZIM | ||
| ChEMBL | 79411 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C14H10O4 | ||
| Moláris tömeg | 242,23 g/mol | ||
| Megjelenés | white solid | ||
| Sűrűség | 1,2917 g/cm3 | ||
| Olvadáspont | 235,5 °C | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A difénsav szerves vegyület, képlete (C6H4COOH)2. Ez a bifenil dikarbonsavai közül a leginkább tanulmányozott. Fehér szilárd anyag, mely antranilsavból állítható elő diazóniumsóból.[1] A fenantrén mikrobák általi metabolizmusának terméke.[2]
Koordinációs polimereket alkot.[3] Atropizomériát mutat. Anhidridjében 7 tagú gyűrű csatlakozik a benzolgyűrűkhöz.
Előállítás
A difénsav antranilsavból állítható elő diazotálással, melyet réz(I)-gyel való redukció követ.[4]

Fenantrén perecetsavval való oxidációjával is előállítható, mely ecetsav és 90%-os hidrogén-peroxidból állítható elő:[5]
A fenantrén más oxidálószerekkel (például hidrogén-peroxiddal, króm-trioxiddal, kálium-dikromáttal vagy kálium-permanganáttal) is kezelhető, mely előbb fenantrénkinont ad, további oxidációval difénsavat.[6][7] A fenantrénkinon alkoholos kálium-hidroxid-oldatban is reagálhat, ekkor kálium-difenát keletkezik,[8] vagy fotooxidálható difénsavvá.[9]
Jegyzetek
- ↑ (1927) „Diphenic Acid”. Organic Syntheses 7, 30. o. DOI:10.15227/orgsyn.007.0030.
- ↑ (2001) „Degradation of Phenanthrene and Anthracene by Cell Suspensions of Mycobacterium sp. Strain PYR-1”. Applied and Environmental Microbiology 67 (4), 1476–1483. o. DOI:10.1128/AEM.67.4.1476-1483.2001. PMID 11282593.
- ↑ (2009) „A Series of Lead(II) Complexes with π−π Stackings: Structural Diversities by Varying the Ligands”. Crystal Growth & Design 9 (4), 1894–1911. o. DOI:10.1021/cg801085d.
- ↑ (1927) „DIPHENIC ACID”. Organic Syntheses 7, 30. o. DOI:10.15227/orgsyn.007.0030.
- ↑ O'Connor, William F. (1953). „2,2′-Diphenic Acid from Phenanthrene” (angol nyelven). Industrial & Engineering Chemistry 45 (2), 277–281. o. DOI:10.1021/ie50518a020. ISSN 0019-7866.
- ↑ Noller, Carl R.. Kondensierte aromatische Kohlenwasserstoffe und ihre Derivate, Lehrbuch der Organischen Chemie (német nyelven). Springer Berlin Heidelberg, 614–639. o.. DOI: 10.1007/978-3-642-87324-9_28 (1960). ISBN 978-3-642-87325-6
- ↑ Meyer, Hans. Synthese der Kohlenstoffverbindungen: Erster Teil: Offene Ketten und Isocyclen (német nyelven), 1170. o. (1938). ISBN 978-3-7091-3245-6. OCLC 913683350
- ↑ Gustav, Schultz. Die Chemie des Steinkohlentheers: Bd. Die Rohmaterialen. Friedrich Vieweg und Sohn (1886)
- ↑ Photochemie und Photographische Chemikalienkunde (német nyelven). Vienna: Springer Vienna, 136. o.. DOI: 10.1007/978-3-7091-5403-8 (1926). ISBN 978-3-7091-5255-3



