Nitrálás
A szerves kémiában nitrálásnak nevezik azt a kémiai folyamatot, melynek során egy szerves vegyületbe nitrocsoport épül be.
A nitrálásnak számos fontos ipari alkalmazása létezik, ebből mennyiségileg legjelentősebb az aromás nitrovegyületek, például a nitrobenzol gyártása. A nitrálási reakciók egyik ismert felhasználása a robbanóanyagok gyártása, például nitroguanidin előállítása guanidinból vagy trinitrotoluol (TNT) gyártása toluolból. Ezeken túl azonban széles körben jelentős a kémiai köztitermékek és prekurzorok gyártásában is. Évente több millió tonna aromás nitrovegyületet állítanak elő.[1]
Aromás nitrálás[szerkesztés]
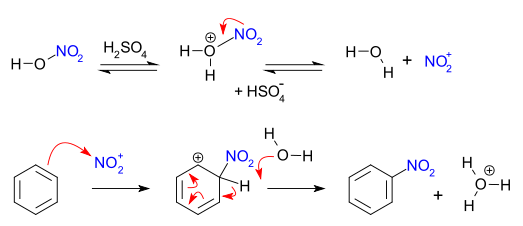
A nitrálást jellemzően „nitrálósavval”, tömény salétromsav és tömény kénsav 1:2 mólarányú elegyével szokták végezni.[2] A nitrálósavban nitróniumion (NO2+) keletkezik, ez a részecske az aromás nitrálási reakció indítója. A nitróniumion sóként is izolálható nitrónium-tetrafluoroborát formájában,[3] és nitrálósav nélkül is képes a nitrálási reakciót végbevinni. A nitrálósavas reakciókban a kénsav nem használódik el, hanem mint katalizátor és vízelvonószer vesz részt. A benzol nitrálását melegen, de 50 °C-ot meg nem haladó hőmérsékleten végzik.[4] Maga a folyamat aromás elektrofil szubsztitúció, melyben az elektronban gazdag benzolgyűrű támadja a nitróniumiont:
Alternatív mechanizmusokat, köztük egyelektron-átmeneteset (single electron transfer, SET) is javasoltak.[5][6]
Felhasználás[szerkesztés]
A nitrálási reakcióknál problémát okozhat a szelektivitás, mivel általában többféle termék is keletkezhet, de közülük csak egy kívánatos, így a melléktermékek szennyezésként jelentkeznek vagy hulladékként megszabadulnak tőlük. Emiatt érdemes a szintézist úgy megtervezni, hogy az kellően szelektív legyen: a fluorenon például szelektíven trinitrálható[7] vagy tetranitrálható.[8]
Az aromás gyűrű szubsztituensei befolyásolják az aromás elektrofil szubsztitúciós reakció sebességét. A dezaktiváló csoportok, például más nitrocsoportok elektronszívó hatásúak. Az ilyen csoportok dezaktiválják (lassítják) a reakciót, és az elektrofil nitróniumiont meta helyzetbe irányítják. Dezaktiváló, meta-irányító csoportok például a szulfonil-, ciano-, ketocsoportok, észterek és karboxilátok. A nitrálást gyorsítják az aktiváló csoportok, mint az amino-, hidroxil- és metilcsoportok, vagy az amidok és éterek, ezek para és orto izomereket eredményeznek.
Az anilin közvetlen nitrálása salétromsavval és kénsavval – az egyik forrás szerint[9] – 50/50 százalékban ad para- és meta-nitroanilin izomereket. Ebben a reakcióban a gyorsan reagáló, aktiváló anilin (ArNH2) egyensúlyban van a nagyobb mennyiségben jelen lévő, de kevésbé reakcióképes (dezaktivált) anilíniumionnal (ArNH3+), ami megmagyarázhatja, hogy miért ilyen a termékek megoszlása. Egy másik forrás szerint[10] az anilin jobban kontrollált nitrálását az anilin – ecetsav-anhidriddel végzett – acetaniliddé történő átalakításával kezdik, majd ezt követően hajtják végre a tényleges nitrálást. Mivel az amidcsoport szokványos aktiváló csoport, termékként a para- és orto-izomerek keletkeznek. A reakcióelegy melegítésével az amid visszahidrolizál a nitrált anilinné.
A Wolffenstein–Böters-reakcióban benzolból salétromsav és higany(II)-nitrát reakciójában pikrinsav keletkezik.
Ipszo-nitrálás[szerkesztés]
Aril-kloridokkal, -triflátokkal és -nonaflátokkal ipszo helyzetű szubsztitúció is történhet, ezt nevezik ipszo-nitrálásnak.[11] Ezt a kifejezést elsőként Perrin és Skinner használta 1971-ben a klóranizol nitrálásának vizsgálatakor.[12] Az egyik esetben 4-klór-n-butilbenzolt reagáltattak nátrium-nitrittel t-butanolban, 0,5 mol% Pd2(dba)3 (trisz(dibenzilidénaceton)dipalládium(0)) fázistranszfer-katalizátor és biarilfoszfin ligandum jelenlétében, termékként 4-nitro-n-butilbenzol keletkezett.[13]
Jegyzetek[szerkesztés]
- ↑ Gerald Booth. Nitro Compounds, Aromatic, Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI: 10.1002/14356007.a17_411 (2007)
- ↑ Antus Sándor, Mátyus Péter. Szerves kémia II.[halott link]
- ↑ George A. Olah and Stephen J. Kuhn. „Benzonitrile, 2-methyl-3,5-dinitro-”. Org. Synth.. ; Coll. Vol. 5: 480
- ↑ https://www.chemguide.co.uk/organicprops/arenes/nitration.html
- ↑ (2003) „Unified Mechanism Concept of Electrophilic Aromatic Nitration Revisited: Convergence of Computational Results and Experimental Data”. J. Am. Chem. Soc. 125 (16), 4836–49. o. DOI:10.1021/ja021307w. PMID 12696903.
- ↑ (2006) „Electrophilic Aromatic Nitration: Understanding Its Mechanism and Substituent Effects”. J. Org. Chem. 71 (16), 6192–203. o. DOI:10.1021/jo0609475. PMID 16872205.
- ↑ E. O. Woolfolk and Milton Orchin. „2,4,7-Trinitrofluorenone”. Org. Synth.. ; Coll. Vol. 3: 837
- ↑ Melvin S. Newman and H. Boden. „2,4,5,7-Tetranitrofluorenone”. Org. Synth.. ; Coll. Vol. 5: 1029
- ↑ Web resource: warren-wilson.edu Archiválva 2012. március 20-i dátummal a Wayback Machine-ben
- ↑ Mechanism and synthesis Peter Taylor, Royal Society of Chemistry (Great Britain), Open University
- ↑ (2010) „Ipso-Nitration of Arenes”. Angewandte Chemie International Edition in English 49 (10), 1726–1728. o. DOI:10.1002/anie.200906940. PMID 20146295.
- ↑ (1971) „Directive effects in electrophilic aromatic substitution ("ipso factors"). Nitration of haloanisoles”. Journal of the American Chemical Society 93 (14), 3389. o. DOI:10.1021/ja00743a015.
- ↑ (2009) „Pd-Catalyzed Conversion of Aryl Chlorides, Triflates, and Nonaflates to Nitroaromatics”. DOI:10.1021/ja905768k. PMID 19737014.
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Nitration című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.