Melanin
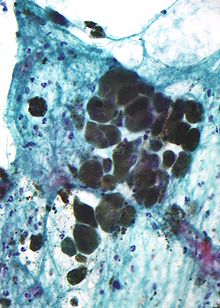
A melanin (a görög mélasz, fekete szóból) az élőlények szinte minden csoportja (a pókfélék kivételével) által termelt sötét színű pigmentek összefoglaló neve. Az állatokban az anyagot a melanociták termelik a tirozin és cisztein aminosavak oxidációjával, majd polimerizációjával.
A melaninoknak három alapvető típusa létezik: az eumelanin, feomelanin és neuromelanin; közülük az első a leggyakoribb. Az eumelaninnak két változata van, a barna és a fekete. A feomelanin vörös színű benzotiazin-polimer, amely a haj vörös színéért felelős, ha csak belőle van. Ez a két melanin a hajban és bőrben együtt alkot polimert, és a színt a monomerjeik egymáshoz polimerben való arányuk adja. A neuromelanin az agyban található, funkciója nem ismert.
A melanin hatékonyan nyeli el a fényt, a bejövő UV-sugárzás 99,9%-át abszorbeálja[1] és képes megvédeni a sejtek DNS-ét a káros sugárzástól, csökkentve ezzel a bőrrák kialakulásának esélyét.
Melanin az emberben
[szerkesztés]
Az emberekben a melanin határozza meg a bőr, a haj és a szem színét, de a belső fülben, agyban (feketeállomány és locus coeruleus) és a mellékvesében is találhatóak melanintartalmú sejtek.
A bőrben az epidermisz bazális rétegében elhelyezkedő melanociták termelik a melanint. A melanociták száma nagyjából mindenkinél azonos, de az egyes rasszokban más-más mennyiségű pigmentet termelnek, így ezek bőrszíne különbözik. Vannak akik egyáltalán nem termelnek melanint (vagy csak nagyon keveset), ők az albínók.
A bőr- és hajszínt az eumelanin és feomelanin aránya és elhelyezkedése határozza meg. Mindkettő megtalálható a bőrben és hajban is, de az eumelaninból jóval több van és az albinizmust is főleg ennek a hiánya okozza.
Eumelanin
[szerkesztés]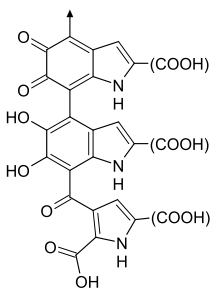
Az eumelanin kémiailag 5,6-dihidroxiindol és 5,6-dihidroxiindol-2-karbonsav polimerje. Két változata, a barna és fekete eumelanin a monomerek elhelyezkedési mintázatában különbözik egymástól. A hajban kis mennyiségű fekete eumelanin önmagában ősz (szürke) hajat eredményez, míg kevés barna eumelaninnak a hatása a szőke haj.
Feomelanin
[szerkesztés]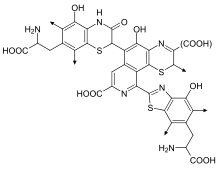
A feomelanin mennyiségtől függően rózsaszín-vörös árnyalatú. A bőrben nagyobb mennyiség található belőle az ajkakon, mellbimbókon, a pénisz makkján és a hüvelyen.[2][3] Ha a hajban a barna eumelanin (ami önmagában szőke hajat eredményezne) mellett feomelanin is találhat, az eredmény vörös haj lesz.[4]
A feomelanin kémiailag abban különbözik az eumelanintól, hogy monomerjei a ciszteinből képződő benzotiazin és benzotiazol molekulák.[5]
A fenti két nagyobb csoporton kívül a vörös haj egyes árnyalataiért az alacsony molekulasúlyú trichokrómok is felelősek, amelyek ugyanazon bioszintetikus útvonalon jönnek létre, mint az eu- és feomelaninok.[6]
Neuromelanin
[szerkesztés]A neuromelanint az agy katekolaminerg neuronjai termelik. A legtöbb az emberi agyban található, az emberszabásúakban kevesebb van, egyéb fajokban pedig teljesen hiányzik.[7] Biológiai hatása nem ismert, bár kimutatták, hogy megköt egyes fémionokat (mint a vas) vagy más, potenciálisan toxikus molekulákat. Lehetséges, hogy szerepe van az apoptózisban és a Parkinson-kór kialakulásában.[8]
Egyéb élőlényekben
[szerkesztés]A melaninnak változatos szerepe lehet a különböző élőlényekben. A fejlábúak a melanin egy formáját lövellik ki ("tinta"), hogy védekezzenek a ragadozók ellen. A baktériumok és gombák is használják az ultraibolya sugárzás és szabad gyökök DNS-károsító hatása elleni védekezésül. Szerepe van a magas hőmérséklet, káros kémiai anyagok (nehézfémek, oxidálószerek) és az immunrendszer támadásai elleni védekezésben is, ezért sok patogén mikroorganizmus (mint pl. a Cryptococcus neoformans gomba) betegségokozó képessége függ a melanintermelésétől.[9] A gerinctelenekben éppen ellenkezőleg, a patogének elleni védekezést segíti. A fertőzés után perceken belül melaninnal veszik körbe a behatolót (melanizáció) és feltehetőleg ennek során szabad gyökök képződnek, amelyek segítenek a kórokozó legyőzésében.[10] Feltételezik, hogy egyes, radioaktivitást toleráló gombák a melaninnal abszorbeálják a gamma-sugárzást és hasznosítani képesek annak energiáját.[11][12]
Az emlősök és madarak kültakarójának színe a melanintól függ.[13] Megfigyelések szerint a melanintartalmú fekete madártollakat a baktériumok kevésbé bontják le, mint a fehéreket vagy karotinokkal színezetteket.[14] A madarak szemében a dúsan erezett fésűszerv (pecten oculi) is melaninban gazdag. Funkciója bizonytalan, talán a szem melegítésében játszik szerepet a fényelnyelés révén, ami meggyorsítja a tápanyagok áramlását a véredények nélküli retinához.
Egyes esetekben a pigmenteloszlás eredményez színárnyalatokat. Az egerek aguti színváltozatban a szőrszálakon fekete eumelaninos és sárga feomelaninos szakaszok váltják egymást, ami összhatásban barna színű lesz; azonban akár egyetlen mutáció képes teljesen fekete vagy sárga egeret létrehozni.
A növények a gyümölcsök (pl. alma, banán) enzimatikus barnulása során hoznak létre tirozinból és katekolaminból melaninszerű katekolmelanint.[15]
Bioszintézise
[szerkesztés]
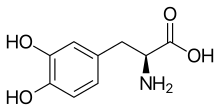



Az eumelanin és feomelanin szintézisének első lépését a tirozináz enzim katalizálja:
A dopakinon a ciszteinnel kétféleképpen reagálhat:
- dopakinon + cisztein → 5-S-ciszteinildopa → benzotiazin köztitermék → feomelanin
- dopakinon + cisztein → 2-S-ciszteinildopa → benzotiazin köztitermék → feomelanin
A dopakinonból leukodopakrómon keresztül eumelanin is képződhet:
- dopakinon → leukodopakróm → dopakróm → 5,6-dihidroxiindol-2-karboxilsav → kinon → eumelanin
- dopakinon → leukodopakróm → dopakróm → 5,6-dihidroxiindol → kinon → eumelanin
Genetikai és egyéb betegségek
[szerkesztés]Ma 36 különféle melaninhoz vagy annak szintéziséhez köthető betegséget ismerünk. Ezek kihatnak a bőrszínre, szemizmokra, véralvadásra, immunrendzerre, idegrendszerre, a hajra, rézháztartásra, valamint a zsigeri szervekre. (de ugye ez nem mind a melanin hiánya követhető vissza, hanem a betegség maga melaninra és ezekre a gondokra) Több öröklődő betegség is kapcsolatos a melanin alacsony szintjével vagy hiányával. Az albinizmusnak nyolc válfaja ismeretes: 7 fajta okulokután és 1 okuláris;[16] többségük autoszomális és recesszíven öröklődik. A leggyakoribb az elsősorban afrikai eredetű emberekben előforduló 2. típusú okulokután albinizmus (okozója az OCA2 gén mutációja), amely születéstől kezdve fennáll és a bőrben, szemben és hajban is csökkent melaninszint vagy annak teljes hiánya jellemzi. Az afrikai eredetű amerikaiakban gyakorisága 1 a 10 ezerhez, míg ez európai származásúaknál ez az arány 1:36 ezer.[17] Egyes afrikai népeknél az elfordulása akár 1 a 2 ezerhez vagy 1 az 5 ezerhez is lehet.[18] A betegség másik fajtája, a sárga okulokután albinizmus főleg a németországi és svájci eredetű, Amerikában élő amishoknál gyakori. Ennél a formánál az újszülötteknek fehér haja és bőre van, de csecsemőkorban gyorsan kialakul a normális bőrpigmentáció.[18]
A szemet érintő albinizmus(okuláris albinizmus) a látás élességét is negatívan befolyásolhatja, mert az erősebb fény visszaverődik a retinán és egy fénysugár több helyen tudatosul, így az albínók a látásvizsgálatokon rosszabbul teljesítenek az átlagnál. Ez a betegség a GPR143 gén mutációjához köthető. Jól ismert az albinizmus és süketség kapcsolata is, bár a pontos mechanizmusát még nem értjük. Darwin is leírta A fajok eredetében, hogy "a teljesen fehér és kék szemű macskák általában süketek".[19] Embereknél az észak-amerikai hopi indiánoknál ritkán előforduló Waardenburg-szindrómában figyelhető meg az alulpigmentáltság és süketség. A hopik között az albinizmus előfordulása 1 a 200-hoz. Hasonló kapcsolódást figyeltek meg a kutyák és a rágcsálók esetében is. A melaninhiány azonban nem jár feltétlenül a hallás károsodásával, a legtöbb albínó hallásával nincsen gond.
A Parkinson-kórban szenvedő betegekben megfigyelhető a feketeállomány (substantia nigra) és a locus coeruleus neuromelanintartalmának csökkenése, amit a pigmentált sejtek hiánya okoz. Ennek eredményeképpen visszaesik a dopamin és a noradrenalin termelése. Az emberi rasszok között nincs különbség a neuromelanin mennyiségében; mégis az afrikaiakban jóval alacsonyabb a Parkinson-kór előfordulása, ami talán a bőrben lévő melanin protektív hatására utalhat.[20][21] Újabban feltételezik, hogy a melaninnak nem csak fényvédő szerepe van,[22] hanem karboxil- és hidroxilcsoportjai révén hatékonyan megköti a potenciálisan toxikus fémionokat. A Parkinson-kórban a neuromelaninszint csökkenése együtt jár a vas mennyiségének növekedésével az agyban.
A melaninhiány mellett a melaninpolimer molekulatömege is csökkenhet, például oxidatív stressz, ultraibolya fény, pH-változás, fémionok koncentrációjának esése következtében. Az ilyen állapotú melanin a feltételezések szerint antioxidáns tulajdonság helyett pro-oxidáns lehet és a szemben makuladegenerációt, a bőrben melanómát okozhat.[23] A magas eumelaninszint a bőrben megnöveli a D-vitamin szintéziséhez szükséges fénymennyiséget is, valamint csökkenti a bőrfoltok lézeres eltávolításának hatékonyságát.
Fényvédő szerepe
[szerkesztés]A melanint a melanociták termelik, amelyekben melanoszómának nevezett vezikulumokba gyűlik. A melanoszómák átadódnak a többi bőrsejtnek is, ahol a sejtmag fölött helyezkednek el, hogy védjék a kromoszómákat a napfény káros, mutagén hatásaitól. A régóta napfényes területeken élő emberi rasszok bőre nagy mennyiségű eumelanint tartalmaz, emiatt barna vagy fekete színű. Így a bőrrák (különösen annak agresszív formája, a melanóma) előfordulása náluk alacsonyabb, mint a világos bőrű rasszoknál.[24]
A D-vitamin szintéziséhez napfényre is szükség van, ezért a sötét bőrű emberek a mérsékelt és sarki éghajlati zónákban D-vitamin hiányában szenvedhetnek. A jelenleg általánosan elfogadott elmélet szerint minden mai ember Afrikából származik, vagyis eredetileg valószínűleg fekete bőrű volt.[25] Ahogyan a korai emberek megtelepedtek Európa és Ázsia hidegebb éghajlatán, a világosabb bőr szelekciós előnyt jelenthetett. Két általánosan elterjedt génmutáció okozza a világos bőrt, az Mc1r[26] és az SLC24A5;[27] az utóbbiról kimutatták, hogy pozitív szelekciós hatás érte. A délebbre költöző világos bőrű emberek erősebb napfénynek vannak kitéve; ez ellen bőrük barnulással, eumelanin-termeléssel védekezik. A szemben, a szivárványhártyában található melanin a retinát védi az UV-fény és a magas energiájú normál fény ellen. A kék, zöld, szürke szemű emberekben ez a védelem kevésbé hatékony, mint a barna szeműekben.
Jegyzetek
[szerkesztés]- ↑ Meredith P, Riesz J (2004. február 1.). „Radiative relaxation quantum yields for synthetic eumelanin”. Photochemistry and Photobiology 79 (2), 211–6. o. DOI:10.1111/j.1751-1097.2004.tb00012.x. PMID 15068035.
- ↑ http://www.metacyc.org/META/NEW-IMAGE?type=COMPOUND&object=CPD-12380
- ↑ Vincent J. Hearing and Katsuhiko Tsakamoto (1991), "Enzymatic control of pigmentation in mammals", The FASEB Journal 5 (14): 2902–2909, <http://www.fasebj.org/content/5/14/2902.full.pdf>
- ↑ V.Krishnaraj, M.D, Skin Layers
- ↑ Greco G, Panzella L, Verotta L, d'Ischia M, Napolitano A (2011. április 1.). „Uncovering the structure of human red hair pheomelanin: benzothiazolylthiazinodihydroisoquinolines as key building blocks”. Journal of Natural Products 74 (4), 675–82. o. DOI:10.1021/np100740n. PMID 21341762.
- ↑ G. Prota and A. G. Searle (1978), "Biochemical sites of gene action for melanogenesis in mammals", Annales de génétique et de sélection animale 10 (1): 1–8, doi:10.1186/1297-9686-10-1-1, <http://www.gsejournal.org/content/pdf/1297-9686-10-1-1.pdf>
- ↑ Fedorow H, Tribl F, Halliday G, Gerlach M, Riederer P, Double KL (2005). „Neuromelanin in human dopamine neurons: comparison with peripheral melanins and relevance to Parkinson's disease”. Prog Neurobiol 75 (2), 109–124. o. DOI:10.1016/j.pneurobio.2005.02.001. PMID 15784302.
- ↑ Double KL (2006). „Functional effects of neuromelanin and synthetic melanin in model systems”. J Neural Transm 113 (6), 751–756. o. DOI:10.1007/s00702-006-0450-5. PMID 16755379.
- ↑ Hamilton AJ, Gomez BL (2002. március 1.). „Melanins in fungal pathogens”. Journal of Medical Microbiology 51 (3), 189–91. o. [2018. február 11-i dátummal az eredetiből archiválva]. DOI:10.1099/0022-1317-51-3-189. PMID 11871612. (Hozzáférés: 2015. szeptember 16.)
- ↑ Cerenius L, Söderhäll K (2004. április 1.). „The prophenoloxidase-activating system in invertebrates”. Immunological Reviews 198, 116–26. o. DOI:10.1111/j.0105-2896.2004.00116.x. PMID 15199959.
- ↑ Castelvecchi, Davide (2007. május 26.). „Dark Power: Pigment seems to put radiation to good use”. Science News 171 (21), 325. o. DOI:10.1002/scin.2007.5591712106.
- ↑ (2007) „Ionizing radiation changes the electronic properties of melanin and enhances the growth of melanized fungi”. Plos One 2 (5), e457. o. DOI:10.1371/journal.pone.0000457. PMID 17520016.
- ↑ (1976. július 1.) „Some aspects of melanin biology: 1950-1975.”. The Journal of investigative dermatology 67 (1), 72–89. o. DOI:10.1111/1523-1747.ep12512500. PMID 819593.
- ↑ Grande, Juan Manuel, Negro, Juan José; María Torres, José (2004). „The evolution of bird plumage colouration; a role for feather-degrading bacteria?”. Ardeola 51 (2), 375–83. o. DOI:10.1007/s00114-008-0462-0.
- ↑ (2005. május 15.) „Tyrosinase inhibitors from natural and synthetic sources: structure, inhibition mechanism and perspective for the future”. Cellular and Molecular Life Sciences 62 (15), 1707–1723. o. DOI:10.1007/s00018-005-5054-y.
- ↑ https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7503925/
- ↑ Oculocutaneous Albinism. [2008. december 23-i dátummal az eredetiből archiválva]. (Hozzáférés: 2008. december 23.)
- ↑ a b "Ocular Manifestations of Albinism"
- ↑ Archivált másolat. [2006. szeptember 23-i dátummal az eredetiből archiválva]. (Hozzáférés: 2006. szeptember 18.)
- ↑ Lewy Body Disease. [2009. július 21-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. február 6.)
- ↑ Nicolaus BJ (2005). „A critical review of the function of neuromelanin and an attempt to provide a unified theory”. Med. Hypotheses 65 (4), 791–6. o. DOI:10.1016/j.mehy.2005.04.011. PMID 15949901.
- ↑ Liu Y, Hong L, Kempf VR, Wakamatsu K, Ito S, Simon JD (2004. június 1.). „Ion-exchange and adsorption of Fe(III) by Sepia melanin”. Pigment Cell Research 17 (3), 262–9. o. DOI:10.1111/j.1600-0749.2004.00140.x. PMID 15140071.
- ↑ Meyskens FL, Farmer P, Fruehauf JP (2001. június 1.). „Redox regulation in human melanocytes and melanoma”. Pigment Cell Research 14 (3), 148–54. o. DOI:10.1034/j.1600-0749.2001.140303.x. PMID 11434561.
- ↑ Smithsonian Human Skin Color Variation Archiválva 2016. március 6-i dátummal a Wayback Machine-ben The Smithsonian National Museum of Natural History
- ↑ (2009. május 1.) „The genetic structure and history of Africans and African Americans”. Science 324 (5930), 1035–44. o. DOI:10.1126/science.1172257. PMID 19407144.
- ↑ Harding RM (2000. április 1.). „Evidence for variable selective pressures at MC1R”. American Journal of Human Genetics 66 (4), 1351–61. o. DOI:10.1086/302863. PMID 10733465.
- ↑ (2005. december 1.) „SLC24A5, a putative cation exchanger, affects pigmentation in zebrafish and humans”. Science 310 (5755), 1782–6. o. DOI:10.1126/science.1116238. PMID 16357253.
Fordítás
[szerkesztés]- Ez a szócikk részben vagy egészben a Melanin című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
