Kalcium-klorid
| Kalcium-klorid | |

| |
| |
| IUPAC-név | kalcium-klorid |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 10043-52-4 |
| EINECS-szám | 233-140-8 |
| RTECS szám | EV9800000 |
| ATC kód | A12AA07, B05XA07, G04BA03 |
| Gyógyszer szabadnév | calcium chloride |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | CaCl2 |
| Moláris tömeg | 110,98 g/mol |
| Megjelenés | fehér, szilárd, nedvszívó anyag |
| Sűrűség | 2,15 g/cm³ vízmentes, 1,835 g/cm³ dihidrát, 1,71 g/cm³ hexahidrát |
| Olvadáspont | 772 °C |
| Forráspont | > 1600 °C |
| Oldhatóság (vízben) | 740 g/l (20 °C) |
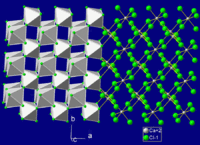
| Kristályszerkezet | |
| Kristályszerkezet | Oktaéder |
| Termokémia | |
| Std. képződési entalpia ΔfH |
−796 kJ/mol |
| Standard moláris entrópia S |
76,2 J/(mol·K) |
| Veszélyek | |
| EU osztályozás | Irritatív (Xi) |
| EU Index | 017-013-00-2 |
| R mondatok | R36[1] |
| S mondatok | (S2) S22, S24[1] |
| Lobbanáspont | nem gyúlékony |
| Rokon vegyületek | |
| Azonos kation | A kalcium vegyületei |
| Azonos anion | Kloridok |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
A kalcium-klorid (CaCl2) a kalciumnak a klórral alkotott ionos vegyülete. Vízben nagyon jól oldódik. Szobahőmérsékleten szilárd sót alkot. Alkalmazása nagyon sokrétű, például az utak síkosságmentesítéséhez és cement-adalékanyagként is használják. Nagy mennyiségben mészkőből lehet előállítani, ugyanakkor fontos forrása a Solvay-eljárás, melynek melléktermékeként keletkezik. Higroszkopikus tulajdonsága miatt (nagy intenzitással köti meg a vizet) zárt, jól szigetelt tartályban kell tárolni, szállítani. A VIII. Magyar Gyógyszerkönyvben Calcii chloridum dihydricum és Calcii chloridum hexahydricum néven hivatalos.
Kémiai tulajdonságok[szerkesztés]
A kalcium-kloridot egy oldatban kalcium-ionok forrásához alkalmazzák. Sok kalciumvegyület nem vízoldékony, ezért a folyamat során kicsapódik.
Olvadt CaCl2-t elektrolízisnek alávetve kalciumot kapunk.
- CaCl2(l) → Ca(s) + Cl2(g)
Előállítása[szerkesztés]
Előállításának többféle módja is ismert:
- 2 CH3COOH + CaCO3 → CO2 + H2O + 2 CH3COO- + Ca2+
- majd a keletkezett oldathoz Nátrium-klorid oldatot adagolva a lejátszódó reakció:
- 2 CH3COO- + Ca2+ + 2 Na+ + 2 Cl- → CaCl2 + 2 CH3COONa
Továbbá:
- CaCO3 + 2 HCl → CaCl2(Aq) + H2O(I) + CO2(g)
Mindkét előállítási mód esetén nehézséget okoz a keletkező CaCl2 exoterm oldódása.
Felhasználási területei[szerkesztés]
Az évente előállított több millió tonna kalcium-kloridot rendkívül sok területen alkalmazzák:
- Erősen higroszkopikus hatása miatt a levegőben vagy bármilyen egyéb gázban jelenlévő vízpára eltávolítására használják oly módon, hogy a gázt átáramoltatják egy erre a célra készített, kalcium-kloridot tartalmazó csövön. Az egyes oldatokban található nem kívánt vízmennyiség eltávolítására is használják. Ezen tulajdonsága miatt a kalcium-klorid kiváló „szárítószer”.
- CaCl2 + 2 H2O → CaCl2·2H2O
A víz megkötése, valamint a vízben történő oldódás erősen exoterm, és a környezet hőmérséklete igen hamar 60 °C fölé ugrik. Emiatt könnyen égési sérüléseket okozhat.
- Mivel feloldódás közben intenzíven hőt termel, ezért jégolvasztásra is alkalmazzák. Az utakra szórva hatékonyan felolvasztja a jégpáncélt, és oldott állapotban kevésbé káros a növényekre, mint a nátrium-klorid, valamint alacsonyabb hőmérsékleten is használható.
- Betonkeverékekben elősegíti a gyors megszilárdulást, de erősen korrodáló hatása miatt vasbetonszerkezetekben nem alkalmazható.[2]
- Néhány autópályán a szálló por visszaszorítására is használják, mert az útra szórva ott megköti a vizet, ezáltal egy vékony folyadékréteg kerül az út felszínére, mely megköti a port.[3]
- A kalcium-klorid nagyon sós ízű, ezért néhány ételben adalékanyagként (ízszabályozásra és szilárdítóanyagként) alkalmazzák E-száma 509. Savanyúságokban és egyes paradicsomsűrítményekben, egyes sajtfélék elkészítése során, és konzervzöldségekben előszeretettel használják. Az étel sós ízét a nagy mennyiségben káros nátrium-klorid alternatívájaként kalcium-kloriddal is szokták korrigálni.
- Műanyagokhoz is adagolják.
- A szennyvíztisztítás során hátramaradt üledék víztartalmának csökkentésére is használják.
- Mivel növeli a sejtmembrán permeabilitását (a sejtmembrán meggátolja a nagy molekulák be- és kijutását a membránon keresztül), vizes oldatát előszeretettel alkalmazzák genetikai módosítások során, mert a csökkentett ellenállás segítségével a DNS-fragmentumok nagyobb valószínűséggel jutnak be a sejtbe, és épülnek be a sejt DNS-ébe.
- Poroltókban használt adalékanyag.
- Kohókban is alkalmazzák.
- „Álkaviár” előállítása során a zöldség- vagy gyümölcskivonathoz adagolják.[4]
- Sürgősségi ellátásban a blokkolt kalciumcsatornák okozta zavar helyreállítására, valamint a kalcium-glukonáttal együtt az elektrolitegyensúly beállítására is alkalmazzák.
Elővigyázatossági tanácsok[szerkesztés]
A kalcium-klorid erősen irritáló szer, használata során kesztyű és védőszemüveg viselése ajánlott, valamint kerülni kell a közvetlen belélegzést.
Bár kezelése különösebb körültekintést nem igényel, a szervezetbe légzés folyamán vagy a szájon át bekerülve égési sérüléseket okozhat.
Jegyzetek[szerkesztés]
- ↑ a b c A kalcium-klorid vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2010. augusztus 22. (JavaScript szükséges) (angolul)
- ↑ Accelerating Concrete Set Time, 1999. június 1. [2007. január 17-i dátummal az eredetiből archiválva]. (Hozzáférés: 2007. január 16.)
- ↑ Dust: Don't Eat It! Control It!. Road Management & Engineering Journal. US Roads (TranSafety Inc.), 1998. június 1. [2007. október 29-i dátummal az eredetiből archiválva]. (Hozzáférés: 2006. augusztus 9.)
- ↑ Apple Caviar Technique. StarChefs Studio. StarChefs.com, 2004. április 1. (Hozzáférés: 2006. augusztus 9.)
Források[szerkesztés]
- Handbook of Chemistry and Physics, 71st edition, CRC Press, Ann Arbor, Michigan, 1990.
- International Chemical Safety Card 1184
- Calcium Chloride Handbook from Dow Chemical (pdf 1.6MB)
- Report on steel corrosion by chloride including CaCl2[halott link]
