Béta-oxidáció
A biokémiai metabolizmusban a béta-oxidáció az a katabolikus folyamat, melyben a zsírsavak lebontása történik.[1] A prokarióták esetében a citoszolban, míg az eukarióták esetében a mitokondriumban zajlik acetil-CoA termelése céljából, ami a citrátkörbe lép, és NADH/FADH2 koenzimekké alakul, melyeket az elektrontranszportlánc használ fel ATP előállításához. A folyamat nevét (béta-oxidáció) onnan kapta, hogy a zsírsav béta szénatomja oxidálódik karbonilcsoporttá. A béta-oxidáció első három lépését egy mitokondriális enzim-komplex (MTP) katalizálja, amely a belső mitokondrális membránhoz kapcsolódik. Egyes zsírsavak eltérő helyen, a peroxiszómában is oxidálódhatnak.

Áttekintés
[szerkesztés]A zsírsav lebontás a következő lépésekből áll:
- A szabad zsírsavak aktivációja koenzim-A-val, majd membrántranszportja.
- A béta szénatom oxidációja karbonilcsoporttá.
- Két szénatomos csoportok lehasítása, mely acetil-CoA-t eredményez.
- Az acetil-CoA oxidációja szén-dioxiddá a citrátkörben.
- A felszabadult elektronok transzportja elektronszállító molekulák (NADH, FADH2) által az elektrontranszportláncba, ahol az oxidatív foszforiláció zajlik.
Aktiváció és membrántranszport
[szerkesztés]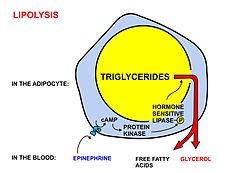


A szabad zsírsavak nem tudnak áthatolni a biológiai membránokon negatív töltésük miatt. Emiatt specifikus transzporterek (például az SLC27 családba tartozó transzporter) segítségével jutnak át a sejtmembránon.[2][3] A citoszolba érkezés után, a következő folyamatok juttatják a zsírsavakat a mitokondriális mátrixba, ahol a béta-oxidáció zajlik.
- A hosszú-láncú-zsírsav-CoA ligáz katalizálja a reakciót a zsírsav és egy ATP között, melynek során zsíracil-adenilát valamint inorganikus pirofoszfát keletkezik. Utóbbi szabad koenzim-A-val reagál, így zsíracil-CoA észter és AMP keletkezik.
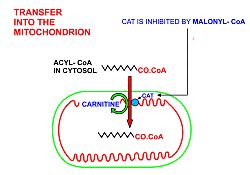
- Ha a zsíracil-CoA hosszú lánccal rendelkezik, akkor a karnitin inga lép működésbe:
- Az acil-CoA a karnitin hidroxilcsoportjára kerül a karnitin-palmitoil-transzferáz I reakció során. Ez az enzim a belső mitokondriális membrán citoszolikus oldalán lokalizálódik.
- Az acil-karnitin a mitokondriális mátrixba transzportálódik a karnitin-acilkarnitin transzlokáz által, míg a karnitin ugyanezen az útvonalon elhagyja a mátrixot.
- Az acil-karnitin visszaalakul acil-CoA-vá a karnitin-palmitoil-transzferáz II reakció során. Ez az enzim a belső mitokondriális membrán mátrix felé tekintő oldalán lokalizálódik.
- Ha a zsíracil-CoA rövid lánccal rendelkezik, akkor ezek a rövid láncú zsírsavak egyszerű diffúzióval jutnak át a belső mitokondriális membránon.[4]
Általános mechanizmus
[szerkesztés]Ha a zsírsav a mitokondriális mátrixba került, megkezdődik a béta-oxidáció, melynek során minden ciklusban két szénatomos csoportok hasítódnak le a zsírsavról acetil-CoA formájában. A folyamat négy lépésből áll.
- A hosszú láncú zsírsav dehidrogenizálódik, így egy transz konfigurációjú kettős kötés jön létre a C2 és C3 pozíciójú szénatomok között. Ezt a lépést az acil-CoA-dehidrogenáz katalizálja. Végeredményként transz-Δ2-enoil-CoA keletkezik. A reakciót katalizáló enzim FAD molekulát használ, mint elektronakceptort, ami FADH2 molekulává alakul.
- A transz-Δ2-enoil-CoA hidratálódik a kettős kötésnél, mely egy L-β-hidroxiacil-CoA-t eredményez. A folyamatot az enoil-CoA-hidratáz katalizálja.
- Az L-β-hidroxiacil-CoA-t egy újabb dehidrogenizációs reakció alakítja β-ketoacil-CoA-vá. Ezt a reakciót a β-hidroxiacil-CoA dehidrogenáz katalizálja. Az enzim NAD molekulát használ elektronakceptorként.
- A β-ketoacil-CoA tiolízise a C2 és C3 pozíciójú (alfa és béta) szénatomok között jön létre. A folyamatot az acetil-CoA-aciltranszferáz-β-ketotioláz enzim katalizálja. A reakció során egy új koenzim-A molekula nukleofil támadása következik be a C3 pozíciójú szénatomon. Ezáltal két szénatom leválik acetil-CoA-t kialakítva, míg a visszamaradó acil-CoA két szénatommal rövidebb lesz.
A testben lévő szövetek legnagyobb része képes a zsírsavak oxidációjára. Azonban néhány sejt, például a vörösvérsejtek (nem tartalmaznak mitokondriumot), valamint a központi idegrendszer sejtjei (a zsírsavak nem tudnak átjutni a vér-agy gáton) nem zsírsavakat használnak az energiaigényeik kielégítésére, hanem szénhidrátokat.
Mivel sok zsírsav nem teljesen telített, vagy nem páros szénatomszámú, egyéb mechanizmusok is kialakultak, lásd alább.
Páros szénatomszámú, telített zsírsavak
[szerkesztés]Amint a zsírsav bekerült a mitokondrium mátrixába, minden ciklus béta-oxidáció során egy acetil-CoA molekula szabadul fel, valamint az eredeti zsíracil-CoA két szénatommal rövidebb lesz. Egy béta-oxidációs ciklus a következő négy lépésből áll:
| Leírás | Egyenlet | Enzim | Végtermék |
| Dehidrogenizáció a FAD által: Az első lépés acil-CoA-dehidrogenáz által katalizált oxidációs reakció. Az elektronakceptor a FAD, mely FADH2-vé alakul. A reakció során egy kettős kötés jön létre a C2 és C3 pozíciójú szénatomok között. |
 |
acil-CoA-dehidrogenáz | transz-Δ²-enoil-CoA |
| Hidratáció: A következő lépés a C2 és C3 pozíciójú szénatomok közötti kötés hidratációja. A reakció sztereospecifikus, csak L izomer keletkezik. |
 |
enoil-CoA-hidratáz | L-β-hidroxiacil-CoA |
| Oxidáció a NAD+ által: A harmadik lépés az L-β-hidroxiacil-CoA oxidációja NAD+ által. Ezáltal a hidroxilcsoport ketocsoporttá alakul. |  |
3-hidroxiacil-CoA- dehidrogenáz | β-ketoacil-CoA |
| Tiolízis: Az utolsó lépés a β-ketoacil-CoA hasítása egy másik koenzim-A molekula tiolcsoportja által. A tiolízis a C2 és C3 pozíciójú szénatomok között történik |
 |
β-ketotioláz | Egy acetil-CoA molekula, és egy acil-CoA molekula, amely immáron két szénatommal rövidebb. |
Ez a folyamat addig folytatódik, amíg a teljes lánc feldarabolódik acetil-CoA egységekké. Az utolsó ciklus két különálló acetil-CoA molekulát eredményez, egy acil-CoA és egy acetil-CoA molekula helyett. Minden ciklus során a kiindulási acil-CoA molekula hossza két szénatommal rövidül, valamint egy molekula FADH2, NADH és acetil-CoA keletkezik.
Páratlan szénatomszámú, telített zsírsavak
[szerkesztés]Általánosan, a páratlan szénatomszámú zsírsavak a növények, és néhány tengeri élőlény lipidjeiben találhatók meg. Számos kérődző állat termel nagy mennyiségű három szénatomos propionátot a szénhidrátok fermentációja során a bendőjükben.[5]
Azok a zsírsav láncok, amelyek páratlan szénatomszámot tartalmaznak, ugyanazon folyamatrendszer során oxidálódnak, mint a páros szénatomszámú zsírsavak. A különbség abban rejlik, hogy végeredményként propionil-CoA és szukcinil-CoA keletkezik.
A propionil-CoA egy bikarbonát ion által D-metilmalonil-CoA-vá alakul egy biotin kofaktort alkalmazó reakcióban. Ezt a reakciót a propionil-CoA-karboxiláz katalizálja, és egy ATP felhasználása történik. A bikarbonát ion szénatomja a propionil-CoA középső szénatomjához kapcsolódik, ezáltal kialakítva a D-metilmalonil-CoA-t. Azonban, a D konformáció enzimatikus úton L konformációvá alakul. Ezt az átalakulást a metilmalonil-CoA-epimeráz katalizálja. Ezután a metilmalonil-CoA-mutáz az L konformációjú intermediert átalakítja szukcinil-CoA-vá (B12 vitamin szükséges a folyamathoz). A keletkezett szukcinil-CoA a citrátkörbe tud lépni.
Azonban, míg az acetil-CoA egy meglévő molekula oxálacetáttal kondenzálódva lép be a citrátkörbe, addig a szukcinil-CoA képes önállóan belépni a folyamatba. Ebből kifolyólag a szukcinát direkt növeli a citromsavciklusban cirkuláló molekulák számát. Ha az előbb említett forrásból érkező citrátköri intermedierek száma meghaladja a kataplerotikus szükségletet (pl. aszpartát, illetve glutamát szintézis esetében), akkor a feleslegben lévő intermedierek beléphetnek a glükoneogenezis útvonalába (a májban és a vesékben), a foszfoenol-piruvát-karboxikináz enzimen keresztül, így végeredményként szabad glükóz keletkezik.[6]
Telítetlen zsírsavak
[szerkesztés]A telítetlen zsírsavak béta-oxidációja problémában ütközik, mivel a cisz kötés lokalizációja megakadályozhatja a transz-Δ2 kötés kialakítását. Ezen szituációk során két másik enzim is működik: az enoil-CoA-izomeráz és a 2,4-dienoil-CoA-reduktáz.

Bármilyen konformációjú is legyen a szénhidrogén lánc, a β-oxidáció normálisan zajlik addig, amíg acil-CoA megfelelő szubsztrátja (a kettős kötés konfigurációja megfelelő) az acil-CoA-dehidrogenáznak, illetve az enoil-CoA-hidratáznak.
- Ha az acil-CoA tartalmaz egy cisz-Δ3 kötést, akkor a cisz-Δ3-Enoil-CoA izomeráz|enoil-CoA-izomeráz enzim átalakítja a kötést egy transz-Δ2 konfigurációjú kötéssé, ezáltal megfelelő szubsztrát keletkezik.
- Ha az acil-CoA egy cisz-Δ4 kettős kötést tartalmaz, akkor a dehidrogenizáció 2,4-dienoil intermediert ad, ami nem megfelelő szubsztrátja az enoil-CoA-hidratáznak. Azonban a 2,4-dienoil-CoA-reduktáz enzim redukálja az intermediert, NADPH felhasználásával, transz-Δ3-enoil-CoA-vá. Ezután a folyamat úgy folytatódik, mint a fent említett másik eset: a 3,2-enoil-CoA-izomeráz megfelelő szubsztráttá alakítja a molekulát.
Összefoglalva:
- A páratlan szénatomszámú zsírsavak kettős kötéseit az izomeráz alakítja tovább.
- A páros szénatomszámú zsírsavak kettős kötéseit a reduktáz alakítja tovább.
Peroxiszomális béta-oxidáció
[szerkesztés]A zsírsav oxidáció a peroxiszómákban is zajlik, abban az esetben, ha a zsírsav láncok túl hosszúak a mitokondrium számára. Ugyanazok az enzimek működnek a peroxiszómában, mint a mitokondriális mátrixban, a végeredmény itt is acetil-CoA. A tudomány mai állása szerint úgy vélik, hogy a nagyon hosszú láncú zsírsavak (22 szénatomnál hosszabbak), mind az elágazók,[7] mind a nem elágazók, valamint néhány prosztaglandin és leukotrién[8] egy kezdeti oxidáción esnek át a peroxiszómákban, oktanoil-CoA létrejöttéig. Ezután az oxidáció a mitokondriumban folytatódik.[9]
Egy szignifikáns különbség, hogy a peroxiszomális oxidáció nincs kapcsolva az ATP szintézissel. Ellenben, a magas-potenciálú elektronok oxigén molekulára (O2) kerülnek, így H2O2 keletkezik. Emellett hő is keletkezik a folyamat során. A kataláz nevű enzim, amely kizárólag a peroxiszómákban található, átalakítja a hidrogén-peroxidot vízzé és oxigénné.
A peroxiszomális β-oxidáció során szükség van egyéb enzimekre, melyek a peroxiszómára és a nagyon hosszú szénatomszámú zsírsavakra specifikusak. Három kulcsfontosságú különbség van a mitokondriális és a peroxiszomális β-oxidáció között:
- A NADH, ami a harmadik oxidatív lépésben keletkezik, nem oxidálható újra a peroxiszóma esetében, tehát a redukáló ekvivalensek a citoszolba exportálódnak.
- A peroxiszomális β-oxidáció során a peroxiszomális karnitin-acil-transzferáz enzim működik (míg a mitokondriumban a karnitin-acil-transzferáz I, illetve karnitin-acil-transzferáz II) az aktivált zsírsav membránon keresztüli transzportja során.
- Az első oxidációs lépést a peroxiszómában az acil-CoA-oxidáz által katalizálja.
- A β-ketotioláz, ami a peroxiszomális béta-oxidációban vesz részt, eltérő szubsztrát specificitással rendelkezik, mint a mitokondriális β-ketotioláz.
A peroxiszomális oxidáció magas zsírtartalmú étrend, valamint hypolipidemikus gyógyszerek (például Atromid-S) hatására indukálható.
Energiamérleg
[szerkesztés]Elméletileg minden béta-oxidációs ciklusban maximum 17 ATP keletkezhet, mivel egy NADH 3 ATP-t, egy FADH2 2 ATP-t és egy teljes ciklus a citrátkörben 12 ATP-t termel. Gyakorlatban azonban közelebb van a végeredmény a 14 ATP termelődéséhez, mivel egy teljes oxidációs ciklus során 2,5 ATP termelődik NADPH molekulánként, és 2 ATP termelődik FADH2 molekulánként (a P/O arány alapján), matematikailag lebontva:
ATP ={(n-1)*17+12-2}
| Forrás | ATP | Összesen |
| 1 FADH2 | x 2 ATP | = 2 ATP |
| 1 NADH | x 3 ATP | = 3 ATP |
| 1 acetil-CoA | x 12 ATP | = 12 ATP |
| Összesen | = 17 ATP |
Egy páros szénatomszámú, telített zsírsav lebontásához (C2n), n-1 oxidáció (forduló) szükséges, végeredményként eggyel több acetil-CoA képződik, mint ahány béta-oxidációs ciklus végbement. Emellett két ATP felhasználódik a zsírsav aktivációja során.
Táblázatban összefoglalva:
| Forrás | ATP | Összesen |
| 7 FADH2 | x 2 ATP | = 14ATP |
| 7 NADH | x 3 ATP | = 21 ATP |
| 8 acetil-CoA | x 12 ATP | = 96 ATP |
| Aktiváció | = -2 ATP | |
| Nettó |
= 129 ATP |
Kevesebb ATP termeléssel számolva az egyes elektronakceptor molekulák esetében (FADH2, NADH), végeredményül 106 ATP-t kapunk minden mol palmitát után. 106 ATP ={(8-1)*12+10-2}
A telítetlen zsírsavak béta-oxidációja megváltoztatja a végső ATP termelést, mivel két másik enzim működése válhat szükségessé.
Története és felfedezése
[szerkesztés]1904-ben, a német kémikus Franz Knoop megvilágította a béta-oxidáció lépéseit azáltal, hogy kutyákat páratlan szénatomszámú, valamint páros szénatomszámú ω-fenil zsírsavat (mint a ω-fenilvaleril sav és ω-fenilbutiril sav) tartalmazó eledellel etetett. A béta-oxidáció mechanizmusa, azaz a sikeres leválasztása két szénatomnak, akkor lett tisztázva, amikor kiderült, hogy a páratlan szénatomszámú ω-fenilvaleril sav hippursavvá metabolizálódott, és a páros szénatomszámú ω-fenilbutiril sav egy hasonló vegyületté (angol neve: phenaceturic acid) alakult. Ekkoriban nem ismertek olyan oxidációs reakciót a szerves kémiában, amely a béta szénatomot célozta volna meg.[10][11]
Klinikai jelentőség
[szerkesztés]Legalább 25 enzim és specifikus transzport fehérje található a β-oxidációban.[12] Ezek közül 18 molekulához kapcsolódik metabolikus rendellenesség.
Jegyzetek
[szerkesztés]- ↑ Houten, Sander Michel (2010. március 2.). „A general introduction to the biochemistry of mitochondrial fatty acid β-oxidation” (angol nyelven). Journal of Inherited Metabolic Disease 33 (5), 469–477. o. DOI:10.1007/s10545-010-9061-2. ISSN 0141-8955. PMID 20195903. PMC 2950079.
- ↑ (2004. február 1.) „A current review of fatty acid transport proteins (SLC27)”. Pflügers Archiv European Journal of Physiology 447 (5), 722–727. o. DOI:10.1007/s00424-003-1106-z. PMID 12856180. (Hozzáférés: 2015. március 2.)
- ↑ (2013. április 1.) „SLC27 fatty acid transport proteins”. Molecular Aspects of Medicine 34 (2-3), 516–528. o. DOI:10.1016/j.mam.2012.07.010. (Hozzáférés: 2015. március 2.)
- ↑ (1997. december 3.) „Nonionic diffusion of short-chain fatty acids across rat colon.”. The American Journal of Physiology 274 (3 Pt 1), G518-24. o. [2017. február 4-i dátummal az eredetiből archiválva]. PMID 9530153. (Hozzáférés: 2015. március 2.)
- ↑ Nelson, D. L. & Cox, M. M. (2005).
- ↑ King, Michael: Gluconeogenesis: Synthesis of New Glucose. Subsection: "Propionate". themedicalbiochemistrypage.org, LLC. (Hozzáférés: 2013. március 20.)
- ↑ Singh I (1997. február 1.). „Biochemistry of peroxisomes in health and disease”. Mol. Cell. Biochem. 167 (1-2), 1–29. o. DOI:10.1023/A:1006883229684. PMID 9059978.
- ↑ Peroxisomes: Biology and Importance in Toxicology and Medicine. CRC Press, 69–. o. (2013. április 8.). ISBN 978-0-203-48151-6
- ↑ (1978. március 10.) „Rat liver peroxisomes catalyze the beta oxidation of fatty acids.”. Journal of Biological Chemistry (253), 1522–1528. o. (Hozzáférés: 2015. március 2.)
- ↑ (1904. november 4.) „Der Abbau aromatischer Fettsäuren im Tierkörper”. Beitr Chem Physiol Pathol 6, 150–162. o. (Hozzáférés: 2015. március 2.)
- ↑ (2010. március 2.) „A general introduction to the biochemistry of mitochondrial fatty acid β-oxidation”. Journal of Inherited Metabolic Disease 33 (5), 469–477. o. DOI:10.1007/s10545-010-9061-2. PMID 20195903. PMC 2950079. (Hozzáférés: 2015. március 2.)
- ↑ Tein, Ingrid (2013). „Disorders of fatty acid oxidation”. Handbook of Clinical Neurology 113, 1675–1688. o. DOI:10.1016/B978-0-444-59565-2.00035-6.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Beta oxidation című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
