p53
| p53 tumorszuppresszor fehérje | |
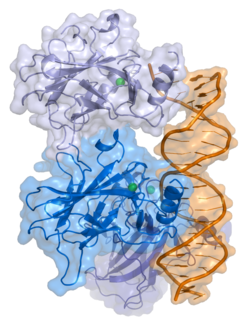 | |
| Azonosítók | |
| Jel | TP53 |
| HGNC | 11998 |
| Entrez | 7157 |
| OMIM | 191170 |
| RefSeq | NM_000546 |
| UniProt | P04637 |
| Egyéb adatok | |
| Lokusz | 17. krom. p13.1 |

A p53 gén, más néven TP53 a 2.7.1.37-es EC számú fehérjét kódolja, mely a sejtciklus szabályozója és tumorszupresszor is egyben. A soksejtű élőlények számára kulcsfontosságú, hogy visszaszorítsák a daganatok kialakulását. A p53-at a genom őrzőjének is nevezik, utalva ezzel a genom mutációk elleni védelemben játszott szerepére (Strachan and Read, 1999). A neve a molekulatömegére utal, mivel SDS-PAGE (nátrium-dodecil-szulfát – poliakrilamid-gél-elektroforézis) során annyit halad a gélen, mint egy 53 kilodalton tömegű fehérje.
Elnevezés[szerkesztés]
- Hivatalos név: Celluláris tumor antigén p53
- Szinonimák
- Tumor szupresszor p53
- Foszfoprotein p53
- Antigén NY-CO-13
Gén[szerkesztés]

A humán p53 gén a 17-es kromoszóma rövid karján található a 13.1-es pozícióban.
A helyét más állatokon is megállapították:
- Egér – 11-es kromoszóma
- Patkány – 10-es kromoszóma
- Kutya – 5-ös kromoszóma
- Sertés – 12-es kromoszóma
Szerkezet[szerkesztés]
A p53 fehérje egy foszfoprotein, mely 393 aminosavból áll.
4 egysége vagy doménje van:
- A transzkripciós faktort aktiváló domén.
- A specifikus DNS szekvenciát felismerő core (mag) domén.
- A fehérje tetramerizációjáért (négyes egységbe szerveződéséért) felelős domén.
- A sérült DNS-t, vagyis bázispárosodási hibát és egyszálú szakaszokat felismerő domén.
A vad típusú p53 nem stabilis, tartalmaz szerkezeti elemeket és a szerveződésben részt nem vevő egységeket is, melyek szinergista módon képesek funkcionálni (Bell et al. 2002).
Funkció[szerkesztés]
A p53 számos tumorellenes mechanizmussal bír:
- DNS károsodást helyreállító fehérjéket aktiválhat.
- Képes blokkolni a sejtciklust a G1/S átmenetben.
- Apoptózist, azaz sejthalált is kiválthat.
A normális p53 inaktív, az MDM-2 fehérjéhez van kötve, így működése gátolt. Ezenkívül az MDM-2 fehérje ubikvitin-ligázként működve a p53 bontásához is hozzájárul. A p53 fehérjét számos rákkeltő hatás indukálhatja, úgy mint UV-sugárzás, onkogének vagy DNS károsító vegyszerek. A DNS hibáját a sejtciklus ellenőrző pontjai érzékelik és arra serkentik az ATM (Ataxia Telangiectasia mutált), Chk1, Chk2 kinázokat, hogy foszforilálják a p53-at az MDM-2-höz közeli helyeken, ezáltal a p53 felszabadulását és lebomlásának lassítását okozzák, így szabad, aktív p53 halmozódik fel a sejtben. Hasonló módon járnak el az onkogének, melyek a p14ARF fehérje által érik el hatásukat. A p53 azáltal viszi véghez feladatát, hogy a DNS azon régiójához kötődik, mely a p21 nevű fehérjét kódolja, kifejezésre serkenti a gént, a p21 pedig a sejtciklus folytatása szempontjából fontos ciklin-ciklin-dependens kinázok gátlását képes előidézni úgy, hogy a fehérjék közé kötődik.
Kutatások kimutattak kapcsolatot a p53 és más fontos tumorellenes gének, a Retinoblastoma tumorszupresszor gén (RB) ill. a H2AX, egy speciális tumorszupresszor hisztonfehérjét termelő gén jelátviteli útvonalai között (Bates et al, 1998).
Szerepe a betegségekben[szerkesztés]
Ha a p53 gén megsérül, a tumorok visszaszorítása jelentős kárt szenved. Azok az egyének, akik a p53 génjének csak egy kópiáját öröklik, nagyobb valószínűséggel fognak szenvedni valamilyen tumortól. A p53 a sejtekben is károsodhat mutagén hatásokra, vegyszerekre, sugárzásra vagy vírusok miatt. A humán tumorok több mint 50%-ában kimutatható a p53 valamilyen mutációja.
Egészséges egyénben a p53 állandó képződésen és lebontáson megy keresztül. A lebontás kapcsoltban van az MDM-2-vel. Egy negatív visszacsatolás részeként a p53 indukálja az MDM-2-t. Így a mutáns p53 nem indukálja azt, ezzel is lehetővé téve a nagy mértékű feldúsulását. Sőt a mutáns p53 képes inaktiválni a megfelelő p53-at (Blagosklonny, 2002).
Potenciális terápiás célpont[szerkesztés]
In vitro p53 bejuttatása a p53-deficiens sejtekbe gyors tumorsejt-elhalást okozott, ezzel is növelve a hozzá fűzött reményeket. Ha egy rendszer hibás, a legtöbb kapcsolódással rendelkező pontját kell rendbehozni. A p53 ilyen a sejtben (mint a hub a számítógépes hálózatokban). Ezért a legfőbb feladat a tumorsejtekben visszaállítani a p53 gén eredeti szekvenciáját, hiszen ezen sejtekben az esetek felében találni mutációt (Vogelstein et al 2000).
Számos stratégiát kipróbáltak már a p53 funkciójának visszaállítására a rákos sejtekben. Találtak fehérjéket, melyek képesek a mutáns p53-at megjavítani azáltal, hogy konformációját addig változtatják, míg az újra funkcióképes nem lesz. Lehetséges terápiás célpont lehet a Hsp90 hősokk fehérje, mely in vivo is kapcsolatba lép a p53-mal.
Az adenovírus a gazdasejtben sokszorozódik azáltal, hogy olyan fehérjéket bocsát ki, melyek a gazdasejtet a virális DNS megkettőződésére kényszerítik. Az adenovírusok egyes tumorok kialakulásában szerepet játszanak. Fordulatot jelentett, mikor az adenovírusokat kezdték használni tumorellenes terápiákban. Az ONYX-015 egy módosított adenovírus, amely szelektíven képes sokszorozódni a p53-deficiens rákos sejtekben, de normál sejtekben nem. Annak a vírusnak a módosításából jött létre, mely az E1B fehérjét fejezi ki, ez pedig inaktiválja a p53-at. A p53 hatásának visszaszorítása fontos a vírus replikálódása szempontjából. A módosított verzióban az E1B-t törölték. Azt várták, hogy a vírus a tumorsejteket megtámadja, azokban sokszorozódik, majd továbbterjed a malignus szövetben. Azok a sejtek, melyekben a vírus többszöröződni képes, szétesnek, így a tumor is felszívódik.
Az ONYX-015-tel egereken végzett preklinikai kísérletek biztatóak. Azonban a klinikai kísérletek korántsem. Csak olyan esetben volt látható jelentős javulás, melyben a vírust kombinálva alkalmazták kemoterápiával (McCormick, 2001). A gondot az E1B okozhatja, melynek az újabb felfedezések nyomán kiderült, a vírus számára más esszenciális funkciói is vannak. A vírus használatának klinikai sikertelenségét okozhatja az is, hogy a tumort a vírus számára csak nehezen átjárható fibrotikus szövet veszi körül.
Története[szerkesztés]
A p53-at 1979-ben azonosították Arnold Levine Princeton University-ről, David Lane Imperial Cancer Research Fund-tól és Lloyd Old a Sloan-Kettering Memorial Hospital-ból. Azonban már előtte felvetették létezését, mint az SV40 tumorkeltő vírus lehetséges célpontjaként.
Habár kezdetben onkogénnek hitték, 1989-ben bebizonyosodott tumorellenes hatása.
1993-ban a Science magazin az év molekulájának választotta (lásd További információk).
Kapcsolódó szócikkek[szerkesztés]
További információk[szerkesztés]
- A p53 szerkezete
- Az év molekulája
- Swissprot: Celluláris tumor antigén p53 Archiválva 2006. augusztus 9-i dátummal a Wayback Machine-ben
- Entrez Gene: TP53
- Magyar kutatók adtak magyarázatot a rákkutatás klasszikus Peto-paradoxonjára
Hivatkozások[szerkesztés]
- Bates S, Phillips AC, Clark PA, Stott F, Peters G, Ludwig RL, Vousden KH. (1998) p14ARF links the tumour suppressors RB and p53. Nature 395:124-125
- Bell S, Klein C, Muller L, Hansen S, Buchner J. (2002). p53 contains large unstructured regions in its native state. J Mol Biol, 322:917-927
- Bischoff JR, Kirn DH, Williams A, Heise C, Horn S, Muna M, Ng L, Nye JA, Sampson-Johannes A, Fattaey A, McCormick F. (1996). An adenovirus mutant that replicates selectively in p53-deficient human tumor cells. Science, 274:373-376
- Blagosklonny, MV. (2002). P53: An ubiquitous target of anticancer drugs. International Journal of Cancer, 98:161-166
- Lacroix M, Toillon RA, Leclercq G. (2006). p53 and breast cancer, an update. Endocrine-Related Cancer, 13:293-325
- McCormick F. (2001). Cancer gene therapy: fringe or cutting edge? Nat Rev Cancer, 1:130-141
- Strachan T, Read AP. (1999). Human Molecular Genetics 2. Ch. 18, Cancer Genetics
- Vogelstein B, Lane D, Levine AJ. (2000). Surfing the p53 network. Nature, 408:307-310

