Nitrátion
| Nitrátion | |

| |
 |

|
| Szabályos név | nitrát |
| Kémiai és fizikai tulajdonságok | |
|---|---|
| Kémiai képlet | NO−3 |
| Moláris tömeg | 62,0049 g mol-1 |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
A nitrát szervetlen összetett anion, kémiai képlete NO−3, molekulatömege 62,0049 g/mol. Ugyancsak nitrát a neve a szerves vegyületekben található RONO2 funkciós csoportnak. Ezek a nitrát-észterek a robbanóanyagok különleges csoportját képezik.
Szerkezete[szerkesztés]

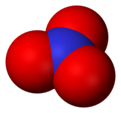
A nitrátion a salétromsav konjugált bázisa, benne a központi nitrogénatomhoz három egyenértékű oxigénatom kapcsolódik síkháromszöges elrendezésben. A nitrátion egyszeres negatív töltésű, ami a központi nitrogénatom +1, és a három oxigénatom egyenként −2⁄3 töltésének eredőjeként adódik. A nitrátion szerkezetét gyakran mutatják be a rezonancia példájaként, az izoelektronos karbonátionhoz hasonlóan az alábbi határszerkezeti képletekkel jellemezhető:
Tulajdonságai[szerkesztés]

Szinte minden szervetlen nitrát só oldódik vízben normál nyomáson és hőmérsékleten. Tipikus szervetlen nitrát például a kálium-nitrát (salétrom).
A szerves kémiában a nitrátok vagy nitrát-észterek (nem összekeverendők a nitrovegyületekkel vagy a nitritekkel) nem túl gyakori, RONO2 általános képletű vegyületek, ahol R bármilyen szerves oldallánc lehet. A nitrátok salétromsavból és alkoholokból nitroxilálás során keletkező észterek. Ilyen észter például a salétromsav és metanol reakciójában keletkező metil-nitrát,[1] a borkősav nitrátja[2] vagy a nitroglicerin (amely a neve ellenére nem nitrovegyület, hanem szerves nitrát, így helyesebb rá az 1,2,3- trinitroxipropán név).
A szerves nitrovegyületekhez (lásd alább) hasonlóan mind a szerves, mind a szervetlen nitrátok alkalmazhatók hajtóanyagként vagy robbanószerként. Mindezen alkalmazási területek alapja, hogy a hőbomlás során a nitrátokból molekuláris nitrogéngáz (N2) és jelentős mennyiségű kémiai energia szabadul fel, ami a nitrogénmolekulán belüli nagyon erős kötés következménye. Különösen a szervetlen nitrátok esetében a nitrátion oxigénjei általi oxidáció is jelentős energiafelszabadulással járó folyamat.
Előfordulása[szerkesztés]
A nitrát sók a természetben nagy üledéktelepek – elsősorban mint chilei salétrom, a nátrium-nitrát fő forrása – formájában lelhetők fel.
Nitrátokat a nitrifikáló baktériumok számos faja állít elő, a puskaporhoz szükséges nitrát vegyületeket pedig – ásványi nitrát források hiányában – különböző, vizeletet és trágyát használó fermentációs folyamatokkal állítottak elő a történelem folyamán.
Felhasználása[szerkesztés]
Nitrátokat főként a mezőgazdaság számára gyártanak, ahol jó oldhatóságuk és könnyű biológiai lebonthatóságuk miatt műtrágyaként használják. A legfontosabb nitrátok az ammónium, nátrium, kálium és kalcium sók. Erre a célra évente több millió kilogrammot gyártanak.[3]
További alkalmazások[szerkesztés]
A nitrátok második legfontosabb felhasználási területe az oxidálószerként történő alkalmazás, leginkább a robbanószerekben, melyekben a szénvegyületek gyors oxidációja révén nagy térfogatú gáz keletkezik (lásd például puskapor). A nátrium-nitrátot felhasználják a levegőbuborékok olvadt üvegből és egyes kerámiákból történő eltávolítására. A megolvasztott sók keverékét felhasználják egyes fémek keményítésére.
Kimutatása[szerkesztés]
A szabad nitrátion oldatokban nitrátion szelektív elektróddal mutatható ki. Ez az elektród a pH-szelektív elektródhoz hasonlóan működik, válaszfüggvénye részben a Nernst-egyenlettel írható le.
Toxicitás[szerkesztés]
Toxikózis[szerkesztés]
Nitrát toxikózis léphet fel a nitrát enterohepatikus metabolizmusa révén, melynek egyik köztiterméke nitrit.[4] A nitritek a hemoglobinban található vas(II)-iont vas(III)-má oxidálják, mely így oxigénszállításra alkalmatlanná válik.[5] A folyamat miatt általános oxigénhiány léphet fel a szövetekben, és súlyos állapot, methemoglobinémia alakulhat ki. Noha a nitrit ammóniává alakul át, ha több nitrit van, mint amennyi tovább tud alakulni, az állat lassan oxigénhiányos állapotba kerül.[6]
Hatása az emberre[szerkesztés]
A nitrát az ember számára mérgező, különösen a csecsemők érzékenyek a methemoglobinémiára, mivel a nitrátot metabolizáló trigliceridek e korban nagyobb koncentrációban fordulnak elő, mint a fejlődés későbbi szakaszaiban. A csecsemők esetén a methemoglobinémiát kék baba tünetként ismerik. Egy időben úgy tartották, hogy az ivóvíz nitráttartalma is járulékos tényező, a tudomány mai állása szerint már kétséges, hogy van-e okozati összefüggés.[7][8] A kék csecsemő szindrómát manapság több tényező eredményének tartják, ideértve bármit, amely gyomorrontást okozhat, például hasmenéses fertőzés, fehérje intolerancia, nehézfém toxicitás stb., és melyek közül a nitrát kevéssé játszik szerepet. Ha egy adott esetben fontos tényezőt jelent, a nitrátok leginkább magas nitráttartalmú ivóvíz fogyasztásával kerülnek a csecsemők szervezetébe, de a táplálékkal, például magas nitráttartalmú zöldségek révén is bejuthatnak. A saláta nitráttartalma magasabb lehet, ha a termesztése során kevesebb napfényt vagy molibdént és vasat kap, melyek esszenciális mikrotápanyagok. A nitrogénműtrágyák túlzott használata is hozzájárul a betakarított növények magasabb nitráttartalmához.[9]
A felnőttek egy része másoknál érzékenyebb a nitrátok hatásaira. Bizonyos egyéneknél egy örökölt mutáció révén a citokróm-b5 reduktáz enzim csökkent mennyiségben termelődik vagy hiányzik.[10] Az enzimmel rendelkezőkhöz képest az ő szervezetük nem tudja olyan gyorsan lebontani a methemoglobint, így a véráramban keringő methemoglobin mennyisége náluk magasabb (ennek révén vérük oxigénben kevésbé gazdag). A csökkent gyomorsavtermelésű emberek[10] (ideértve a vegetáriánusok és vegánok egy részét is) veszélyeztetettek lehetnek. Az ilyen étrendet gyakran a nagyobb mennyiségű zöld, leveles zöldségfogyasztás jellemzi, ami nagyobb nitrátbevitellel járhat. Sokféle egészségi probléma, például ételallergia, asztma,[11] hepatitisz és epekő összefüggésbe hozható a csökkent gyomorsavtermeléssel, az ilyen személyek is nagyon érzékenyek lehetnek a nitrát hatásaira.
A methemoglobinémia metilénkékkel kezelhető, mely az érintett vérsejtekben található vas(III)-iont vas(II)-vé redukálja.[forrás?]
Vízkárosító hatása[szerkesztés]

Az édesvizekben vagy a szárazföldhöz közeli torkolati rendszerekben a nitrát nagy mennyiségben fordulhat elő, ami akár halpusztulást is okozhat. Bár a nitrát az ammóniánál jóval kevésbé mérgező,[12] 30 ppm-et meghaladó nitrátkoncentráció gátolhatja a növekedést, károsíthatja az immunrendszert és stresszfaktor lehet egyes vízi élőlények számára.[13] A korábbi akut nitrát mérgezéses kísérleti protokollok elkerülhetetlen problémái miatt a nitrát mérgezés mértéke újabban vita tárgyát képezi.[14]
A vízrendszerek nagy nitráttartalmának elsődleges forrása a legtöbb esetben a mezőgazdaság vagy tájrendezés révén intenzíven műtrágyázott területekről származó talaj felszínén elfolyó vizek. Ez eutrofizációt okozhat, ami az algák túlszaporodásához vezethet. Azon kívül, hogy ez a vízben oxigénhiányt és halott zónákat okoz, az ökoszisztéma egyensúlyát is megbonthatja, ami egyes élőlénycsoportoknak másokkal szemben kedvezőbb feltételeket biztosíthat. Mindezek miatt, mivel a nitrátok megjelennek az összes oldottanyag-tartalomban, kiterjedten használják őket a vízminőség jellemzésére. Számos kutatás foglalkozott azzal, hogyan lehetne a (főleg a mezőgazdaságból származó) nitrát bejutását csökkenteni vagy növényfajokkal (például Panicum virgatum vagy borzhínár – Ceratophyllum demersum) eltávolítani a meglévő mezőgazdasági rendszerek fölös nitráttartalmát.[15]
A nitrát toxicitása haszonállatokban[szerkesztés]
A nitrátmérgezés főként a szarvasmarha-tenyésztők számára jelent gondot, de más kérődzők tartását is érinti. A nitrátot a növekedésben lévő növények természetes módon felveszik, azonban ha növekedésük megáll, a gyökerük továbbra is felveszi a nitrátot a talajból, és hacsak nem indul újra a növekedés, a nitrát felhalmozódik a növényben. Így a nitrát felhalmozódását követő betakarítás nagy nitráttartalmú terményt eredményez. A növényekben a nitrát felhalmozódását elősegítő tényező lehet a fagy, jégverés, aszály, forró száraz szél, peszticidek vagy herbicidek károsító hatása és bármilyen környezeti ok, amely leállítja a növekedést.[16]
A nitrátmérgezés tünetei lehetnek a szapora pulzus és légzés, előrehaladottabb esetben a vér és a szövetek kékes vagy barnás színűvé válhatnak. A takarmány nitráttartalma vizsgálható, szükség esetén a meglévő készletet alacsonyabb nitráttartalmú anyaggal kell keverni vagy ilyenre kell kicserélni. A különböző haszonállatok számára még biztonságos nitráttartalom:[17]
| Kategória | %NO3 | %NO3-N | %KNO3 | Hatása |
|---|---|---|---|---|
| 1 | <0,5 | <0,12 | <0,81 | Általában biztonságos szarvasmarha és juh számára |
| 2 | 0,5-1,0 | 0,12-0,23 | 0,81-1,63 | Figyelmet igényel - vemhes lovak, juhok és marhák esetén csekély mértékben rendellenes tünetek jelentkezhetnek |
| 3 | 1,0 | 0,23 | 1,63 | Magas nitráttartalom – húsmarhák és juhok esetén elhullás és vetélés történhet |
| 4 | <1,23 | <0,28 | <2,00 | Legmagasabb még biztonságos szint lovak számára. Vemhes kancáknak nem adható magas nitráttartalmú takarmány. |
A fenti értékek száraz (vízmentes) anyagra vonatkoznak.
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Nitrate című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Jegyzetek[szerkesztés]
- ↑ Alvin P. Black and Frank H. Babers. „Methyl nitrate”. Org. Synth.. ; Coll. Vol. 2: 412
- ↑ Snyder, H. R.; Handrick, R. G.; Brooks, L. A. (1942). „Imidazole”. Org. Synth.. ; Coll. Vol. 3: 471
- ↑ Wolfgang Laue, Michael Thiemann, Erich Scheibler, Karl Wilhelm Wiegand "Nitrates and Nitrites" in Ullmann's Encyclopedia of Industrial Chemistry, 2006, Wiley-VCH, Weinheim. doi:10.1002/14356007.a17_265
- ↑ Nitrate and Nitrite Poisoning: Introduction. The Merck Veterinary Manual. (Hozzáférés: 2008. december 27.)
- ↑ (2005) „… between nitrite and hemoglobin: the role of nitrite in hemoglobin-mediated hypoxic vasodilation”. Journal of Inorganic Biochemistry 99 (1), 237–246. o. DOI:10.1016/j.jinorgbio.2004.10.034. PMID 15598504.
- ↑ http://www.ag.ndsu.edu/pubs/ansci/livestoc/v839w.htm
- ↑ T. M. Addiscott & N. Benjamin 2004 "Nitrate and human health"
- ↑ A. A. Avery "Infant Methemoglobemia - reexamining the role of drinking water nitrates"
- ↑ Marschner H 1999 Mineral nutrition of higher plants. Academic Press, London. 889
- ↑ a b Q&A: Nitrate in Drinking Water ((angolul), (spanyolul) nyelven). Washington State Department of Health. [2013. november 3-i dátummal az eredetiből archiválva]. (Hozzáférés: 2013. június 9.)
- ↑ GERD and Asthma. webmd.com. (Hozzáférés: 2009. szeptember 2.)
- ↑ (2007) „Acute toxicity of sodium nitrate, potassium nitrate and potassium chloride and their effects on the hemolymph composition and gill structure of early juvenile blue swimmer crabs (Portunus pelagicus, Linnaeus 1758) (Decapoda, Brachyura, Portunidae)”. Environmental Toxicology and Chemistry 26, 1955–1962. o.
- ↑ Nitrates in the Aquarium. [2011. július 24-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. március 16.)
- ↑ Romano N., Zeng, C. (2007). „Effects of potassium on nitrate mediated changes to osmoregulation in marine crabs”. Aquatic Toxicology 85 (3), 202–208. o. DOI:10.1016/j.aquatox.2007.09.004. PMID 17942166.
- ↑ Larson, R.A., Marina Montez-Ellis, Karen Marley, and Gerald K. Sims (2001). „Nitrate Uptake by Terrestrial and Aquatic Plants”. Proceedings of the Illinois Groundwater Consortium 2001, 1-10. o. (Hozzáférés: 2013. június 13.)
- ↑ Archivált másolat. [2012. április 25-i dátummal az eredetiből archiválva]. (Hozzáférés: 2012. március 16.)
- ↑ http://www1.agric.gov.ab.ca/$department/deptdocs.nsf/all/faq8911


