Karbonilcsoport

A szerves kémiában a karbonilcsoport olyan funkciós csoport, amelyben egy szénatom kettős kötéssel kapcsolódik egy oxigénatomhoz: C=O.
A karbonil kifejezés jelentheti a szén-monoxidot is, mint szervetlen vagy fémorganikus komplexek ligandumát (fém-karbonilokban, például nikkel-karbonilban); ilyenkor a szén és az oxigén között hármas kötés található: C≡O.
A cikk további része a szerves kémiai értelemben vett karbonillal foglalkozik, amikor a szén- és oxigénatom között kettős kötés van.
Karbonilvegyületek[szerkesztés]
Karbonilcsoport az alábbi vegyülettípusokban fordul elő:
| Vegyület | Aldehid | Keton | Karbonsav | Észter | Amid | Enon | Savhalogenid | Savanhidrid |
| Szerkezet | 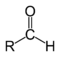 |
 |
 |
 |
 |

| ||
| Általános képlet | RCHO | RCOR' | RCOOH | RCOOR' | RCONR'R'' | RC(O)C(R')CR''R''' | RCOX | (RCO)2O |
A csoportba sorolásnál többnyire a legszűkebb meghatározás használatos. Az R(CO)O(CO)R' szerkezet például savanhidrid, nem pedig az általánosabb észter, noha jelen van benne az észterekre jellemző szerkezeti egység.

További szerves karbonilvegyületek a karbamid és a karbamátok, a kloroformátok és foszgén, melyek a savkloridok származékai, a karbonát észterek, tioészterek, laktonok, laktámok, hidroxamátok és izocianátok. Szervetlen karbonilvegyületre példa a szén-dioxid és karbonil-szulfid.
A karbonilvegyületek speciális csoportja az 1,3-dikarbonil vegyületek, melyek központi metilén részéhez savas protonok kapcsolódnak. Ilyen vegyület például a Meldrum-sav, a dietil-malonát és acetil-aceton.
Reakciókészség[szerkesztés]
Az oxigén elektronegativitása nagyobb, mint a széné, ezért a szénatomtól maga felé húzza az elektronsűrűséget, növelve ezzel a kötés polaritását. A karbonil szénatom ezért elektrofillé válik, és könnyebben lép reakcióba nukleofilekkel. Egyúttal az elektronegatív oxigén is reagálhat elektrofilekkel, például savas oldatban egy protonnal vagy más Lewis-savakkal.
A karbonilvegyületek alfa-hidrogénje sokkal (~103-szor) savasabb, mint az átlagos C−H kötés. Például az acetaldehid és aceton pKa értéke 16,7, illetve 19.[1] Ennek az az oka, hogy a karbonilvegyület rezonanciában van az enol tautomerrel. Az enol erős bázis hatására történő deprotonálódása enolátot hoz létre, amely erős nukleofil, és elektrofileket – például egy másik karbonilvegyületet – alkilezhet.
A karbonilszármazékok közül az amidok a legstabilabbak, ami a nitrogén-szén és szén-oxigén kötések közötti nagy rezonancia stabilitás eredménye.
A karbonilcsoport hidrid reagensekkel, például nátrium-borohidriddel és lítium-alumínium-hidriddel redukálható, vagy katalitikusan hidrogénezhető réz-kromit, Raney-nikkel, rénium, ruténium vagy akár ródium katalizátor alkalmazásával. Ketonok redukciója során szekunder alkohol keletkezik, aldehidekből, észterekből és karbonsavakból pedig primer alkohol.
A karbonilvegyületek alkilezhetők fémorganikus vegyületek, például lítiumorganikus és Grignard-reagens nukleofil támadásával. Az aldol-reakcióban enolátokkal is alkilezhetők.
További fontos reakciók:
- Wittig-reakció, alkén előállítása foszfónium-ilid felhasználásával
- Kizsnyer-Wolff-redukció, hidrazonná, majd telített alkánná alakítás
- Clemmensen-redukció, telített alkán előállítására
- Átalakítás tioacetállá
- Hemiacetállá és hemiketállá, majd acetállá és ketállá történő hidratáció
- Amóniával és primer aminokkal végbemenő reakció iminek előállítására
- Hidroxilaminnal végbemenő reakció oximok előállítására
- Cianid anionnal történő reakció során cianohidrinek keletkeznek
- Oxaziridinekkel végzett oxidációval aciloinok jönnek létre
- Tebbe-reagenssel és foszfónium-ilidekkel reagálva alkének állíthatók elő
- Perkin-reakció, az aldol-addíció egyik változata
- Aldolkondenzáció, enolát és karbonilvegyület közötti reakció
- Cannizzaro-reakció, aldehidek diszproporcionálódása alkohollá és karbonsavvá
- Tyiscsenko-reakció, aldehidek másik diszproporciós reakciója, melynek terméke dimer észter
α,β-telítetlen karbonilvegyületek[szerkesztés]
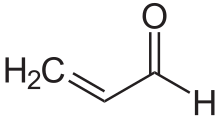
Az α,β-telítetlen karbonilvegyületek a karbonilvegyületek egyik fontos csoportja, általános képletük Cβ=Cα−(C=O)−. Ezekben a vegyületekben a karbonilcsoport egy alkénnel konjugálódik (erre utal a telítetlen jelző), ami különleges tulajdonságokat idéz elő. Telítetlen karbonilvegyület például az akrolein (propénal), mezitil-oxid, akrilsav és maleinsav. Telítetlen karbonilvegyület előállítható laboratóriumban aldol reakcióval és Perkin-reakcióval.
A karbonilcsoport elszívja az elektronokat az alkéntől, ezért az alkéncsoport az elektrofilekkel – például brómmal vagy hidrogén-kloriddal – szemben deaktiválódik.
Elektrofil addíciós reakciókban általános szabályként a nem szimmetrikus elektrofilek hidrogénje az α helyzetbe lép be. Ugyanakkor a nukleofil 1,4-addíciós reakciókban ezen vegyületek a nukleofilekkel szemben aktiváltak.
Spektroszkópia[szerkesztés]
- Infravörös spektroszkópia: a C=O kettős kötés az infravörös fényt a körülbelül 1600–1900 cm−1 hullámszámtartományban elnyeli. Az abszorpció pontos helye jól értelmezhető a molekula geometriájával. Ezt az abszorpciót a felvett infravörös spektrumon karbonil csúcsnak szokták nevezni („carbonyl stretch”).[2]
- Mágneses magrezonancia: a C=O kettős kötés – a környező atomok függvényében – különböző, általában paramágneses eltolódású rezonanciákat mutat. A karbonil szénatom kémiai eltolódása a 13C-NMR spektrumon a 160–220 ppm tartományba esik.
Lásd még[szerkesztés]
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Carbonyl című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások[szerkesztés]
- ↑ Ouellette, R.J. and Rawn, J.D. “Organic Chemistry” 1st Ed. Prentice-Hall, Inc., 1996: New Jersey. ISBN 0-02-390171-3.
- ↑ Mayo D.W., Miller F.A and Hannah R.W “Course Notes On The Interpretation of Infrared and Raman Spectra” 1st Ed. John Wiley & Sons Inc, 2004: New Jersey. ISBN 0-471-24823-1.
További olvasmány[szerkesztés]
- L.G. Wade, Jr. Organic Chemistry, 5th ed. Prentice Hall, 2002. ISBN 0-13-033832-X
- The Frostburg State University Chemistry Department. Organic Chemistry Help (2000).
- Advanced Chemistry Development, Inc. IUPAC Nomenclature of Organic Chemistry (1997).
- William Reusch. tara VirtualText of Organic Chemistry (2004).
- Purdue Chemistry Department [1] (Hozzáférés ideje: Sep 2006). Includes water solubility data.
- William Reusch. (2004) Aldehydes and Ketones Hozzáférés ideje: 23 May 2005.
- ILPI. (2005) The MSDS Hyperglossary- Anhydride.
