A Parkinson-kór kezelése
A Parkinson-kór kezelésekor – a betegség krónikus természete miatt – nagy hangsúlyt kell helyezni a beteg és a családtagok felvilágosítására, a beteg általános jólétének fenntartására, a mozgásra, az étkezésre és a segítő szervezetek bevonására is. Jelenleg nincs ismert gyógymód a betegségre, de gyógyszerekkel és sebészeti beavatkozással a tünetek megszüntethetők.
A kezelés módja a betegség stádiumától függ. A kórban szenvedő páciensek ezért gyakran számos különböző gyógyszert szednek a tünetek kezelésére.[1] Sok gyógyszer áll fejlesztés alatt, melyek a beteg mozgásképességének hirtelen változásait (motoros fluktuáció) és a nem motoros tüneteket célozzák meg, de eddig egyik sem rendelkezik a megfelelő tanúsítványokkal, hogy megjelenhessen a piacon.[2]
Gyógyszeres kezelés[szerkesztés]
A Parkinson-kór tüneteit a feketeállomány dopaminerg neuronjainak a pusztulása okozza.[3]
A mozgáskoordinációban fontos szerephez jut a corticostrialis direkt pálya és indirekt pálya.[4] A direkt pálya hatására nő az izmokhoz menő ingerület, az indirekt pálya pedig normál működésben a gátló hatásokat közvetíti. A dopaminerg neuronokból felszabuló dopamin ezt a rendszert szabályozza normális körülmények között, de ennek híján csökken a direkt pálya hatása (csökken a mozgáskészség) és nő az indirekt pálya hatása (nő a mozgás gátlása). Ez mozgásképtelenséghez (akinézia) vezet. A dopamin mellett még szabályozó szerepet betöltő kolinerg neuronok működése viszont nem módosul, így felborul a dopamin-acetilkolin egyensúly. Ez remegéshez (tremor) és merevséghez vezet.
Ennek alapján különböző gyógyszeres kezelések léteznek. Az egyik és jelenleg a legtöbbet alkalmazott, legjobban működő stratégia a dopamin pótlása. Ez a dopamin előalakjával, a levodopával, dopamin-agonistákkal vagy MAO-B-gátlókkal történhet.[5]
A másik lehetőség a kolinerg hatások gátlása centrális kolinolitikumokkal. Ugyan néha még előfordul, hogy a motoros tüneteket antikolinerg szerekkel kezelik, de ez egyre ritkább, főleg ezeknek a mellékhatásai miatt.[6]
Antihisztamin hatású vegyületeket szintén alkalmaznak azok központi antikolinerg hatása miatt a tremor és merevség ellen.[7]
Dopaminerg hatás helyreállítása[szerkesztés]
A motoros tünetek kezelésében a leginkább hasznos gyógyszerek közé tartoznak a Levodopa, a dopamin-agonisták és a MAO-B-gátlók.[5] A betegség stádiuma szabja meg, hogy ezek közül melyiket alkalmazzuk. Általában 2 fázist különböztetnek meg:[8] a bevezető szakaszt, amikor a betegnek már gyógyszeres kezelést igénylő tünetei lépnek fel és a második szakaszt, amikor a levodopa használat miatt jelennek meg motoros komplikációk. A kezdeti szakaszban a kezelés egy optimális egyensúlyra törekszik a tünetek hatékony kezelése és a felerősödött dopaminerg funkciók okozta mellékhatások között. Dopamin-agonisták és MAO-B gátlók használata megelőzheti az L-DOPA adását, azért, hogy a fellépő dyskinesia visszafordítható legyen. A második szakaszban a cél a tünetek kezelése mellett a fluktuáció ("be-ki"; "on-off" állapot) kezelése is, mely a gyógyszeres kezelésre válaszul lép fel. A gyógyszerek hirtelen elhagyásánál és magasabb dózis adása esetén nagyon körültekintően kell eljárni. Ha a gyógyszeres kezelés már nem elegendő, akkor sebészi beavatkozás, mint a "mély agyi stimuláció" tudja a mozgási problémákat enyhíteni.[9]
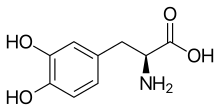
Levodopa[szerkesztés]
Az elmúlt 30 évben a levodopa (vagy L-DOPA) volt a legelterjedtebb kezelési módszer.[8] Az L-DOPA dopaminná alakul a dopaminerg neuronokban a dopa-dekarboxiláz hatására. Mivel a motoros tüneteket a substantia nigrában fellépő dopaminhiány okozza, az L-DOPA alkalmazása időlegesen megszünteti azokat. Viszont csak 5-10%-nyi levodopa jut át a vér-agy gáton. A többség máshol alakul dopaminná, sok mellékhatást, pl. hányingert, dyskinesiát és merevséget okozva. Ezért a levodopát perifériás dopa-dekarboxiláz gátlókkal együtt adják, melyek megakadályozzák annak átalakulását a periférián, így több jut be belőle a központi idegrendszerbe. Ilyen dopa-dekarboxiláz gátló a Carbidopa (co-careldopa, piaci néven Sinemet, Pharmacopa, Atamet ) és a Benserazid (co-beneldopa, piaci néven Madopar) .[8]
A levodopát kapcsolatba hozták a dopaminszabályozási zavarral (mely a kontrollálatlan túladagolásból ered) és ezenkívül kényszeres, cél nélküli cselekménysorozatokat is okozhat.[10]
Kontrollált, lassan ható Sinemet és Madopar készítmények felerősítik a levodopa hatását. A Duodopa a levodopa és carbidopa kombinációja. A motoros tünetek és komplikációk kontrollálásában a lassan ható készítmények nem mutattak nagyobb teljesítményt az azonnal hatókkal összehasonlítva.

A levodopa csökkenti a testben fiziológiásan termelődő levodopa létrejöttét és így kontraproduktívvá válik. A levodopa készítmények hosszabb távon mozgási nehézségekhez vezetnek, melyekre jellemző az akarattól független mozgás, az un. dyskinesia és a gyógyszerre való reagálás hullámzóvá válik. Ekkor a beteg állapota gyorsan változik a kevés tünettel járó "on" állapot, valamint a gyógyszeres kezelésre egyáltalán nem reagáló "off" állapot között, amikor a motoros tünetek is felerősödnek. Emiatt a levodopát minél kisebb dózisban adják. Szintén bevett gyakorlat az adás késleltetése és inkább alternatív készítmények használata. A korábbi stratégia a levodopa időleges megvonása volt, hogy csökkenjenek a motoros komplikációk, de ez ma már nem tanácsolt, mivel veszélyes mellékhatások léphetnek fel, mint a neuroleptikus malignáns szindróma. A legtöbb esetben levodopára szükség van, így végül is kialakulnak a motoros komplikációk.[8]

Az "on"-"off" jelenség szinte állandó következménye a tartós levodopa terápiának. Mozgás- és cselekvőképtelenség depresszióval párosult szakaszai váltakoznak az enyhülés kellemesebb időszakaival. Farmakokinetikus és famakodinámiás faktoroknak is szerepük van a patogenezisben, de arra is mutat bizonyíték, hogy levodopa kezelés fontossága alá volt becsülve, és a túlélő negrostriatális dopamin terminálisok tároló képességének számottevő csökkenése nem kritikus tényező. A levodopa adagolás megváltoztatása, mely jelentheti kisebb adagok gyakoribb, vagy nagyobb adagok ritkább adását hasznosnak bizonyult az állapotingadozás megállításában néhány beteg esetében. A motoros fluktuációt időlegesen kezelheti a szelegilin és a bromokriptin használata, valamint a táplálékkal bevitt fehérjék kontrollálása is.
Állatkísérletekkel készített modellek mutatták meg, hogy adenozin receptor antagonisták levodopával kombinált bevitele növeli a terápiás hatást.[11][12]
COMT-gátlók[szerkesztés]
A Tolcapone gátolja a Catechol-O-metiltranszferáz (COMT) enzimet, ami bontja a dopamint és a levodopát, ezáltal megnő a levodopa terápiás hatása. A perifériás dekarboxiláz gátlókkal együtt ezt használják az L-DOPA kiegészítésére. Azonban lehetséges mellékhatásai miatt, mint a májkárosodás, korlátozott az alkalmazhatósága. Egy másik hasonló vegyület, az entacapone nem mutatott jelentős hatást a máj funkcióira, és megfelelően gátolja a COMT enzimet is. Entacapone adható önmagában is vagy carbidopával és levodopával kombináltan.[8]
Dopamin-agonisták[szerkesztés]
A dopamin-agonistáknak az agyban a levodopához hasonló hatásuk van, mivel a dopaminerg posztszinaptikus receptorhoz kapcsolódnak. Dopamin-
agonistákat először az "on-off" jelenséget mutató betegeken és dyskinesiában alkalmazták, mint a levodopa kiegészítőit, de mostanra már önállóan használják őket a motoros tünetek elsődleges terápiájaként a motoros funkciók romlásának késleltetésére.[8]

Előrehaladott stádiumban hasznosak az "off" szakasz visszaszorítására. Ide tartozik a bromokriptin, pergolid, pramipexol, ropinirol, piribedil, kabergolin, apomorfin és a lizurid.[8] Figyelemre méltó, ámde enyhe mellékhatásokkal járnak, mint a somnolencia, hallucinációk, insomnia, hányinger és székrekedés. Néha a minimális dózis esetén is jelentkeznek ezek a mellékhatások, ezért újabb hatóanyagok után is folyik kutatás. Levodopával összehasonlítva nem csak hogy csökkentik a motoros komplikációkat, de a súlyosabb tüneteket is kezelik.[8] A kezdeti éveken általában elég hatásosak a tünetek kezelésében. De drágábbak is.[8] Adásuk esetén fiatal betegek esetében ritka a dyskinesia, de idősebbek esetében már gyakoribb és náluk más mellékhatásokkal is jár. Emiatt fiatalabbak esetében a dopamin-agonisták, idősebbeknél pedig a levodopa az elsődleges kezelési módszer.[8] A dopamin-agonisták adásakor különböző viselkedés zavarok léphetnek fel.[10]
Apomorfin - egy nem orálisan alkalmazott dopamin-agonista - alkalmas az "off" szakaszok és dyskinesia csökkentésére késői Parkinson-kórban. Mivel gyakran jár másodlagos hatásokkal, mint zavartság és hallucináció, szükség van a vele kezelt betegek szoros megfigyelésére.[8]
Egy-agonistákat a levodopával összevető tanulmány szerint a dopamin-agonistákkal kezelt betegek esetében ritkábban lépett fel dyskinesia, disztónia és motoros fluktuáció, de a negatív mellékhatások miatt (hányinger, oedémák, székrekedés) nem ritkán félbe kellett hagyni a terápiát.
MAO-B-gátlók[szerkesztés]

Monoamin-oxidáz gátlók (szelegilin, rasagilin) növelik a dopaminszintet a bazális ganglionokban, mivel gátolják a lebontását. Gátolják a MAO-B enzimet, mely bontja a dopaminerg neuronok által kibocsátott dopamint. Ezért hatásukra magasabb L-DOPA szint lép fel a striatumban. Önálló adásuk esetén a dopamin-agonistákhoz hasonlóan javítják a motoros tüneteket és lehetővé teszik a levodopa adásának eltolását, de több negatív hatásuk van, mint a levodopának és kevésbé is hatékonyak. Előrehaladott stádiumban nincs sok bizonyíték a hatékonyságukra, de az "on-off" fluktuáció csökkentésében hasznosak. Bár egy korábbi kutatás szerint a szelegilin levodopával kombináltan növeli a halál kockázatát, később ezt cáfolták.[8]
A szelegilin metabolitjai között van az L-amfetamin és L-metamfetamin is. Ezek mellékhatásokat, például insomniát okozhatnak. A kombináció másik mellékhatása stomatitis lehet.
Más gyógyszerek[szerkesztés]
Van némi bizonyíték arra, hogy az amantadin és az antikolinerg szerek hatékonyak a motoros tünetek enyhítésében a korai és késői Parkinson-kórban, de mivel az erre mutató bizonyíték hiányos, nem ezeket alkalmazzák elsődlegesen.[8] Az antikolinerg szerek kezelhetnek egyes Parkinsonizmusra jellemző tünetet, de felerősíthetnek másokat. A motoros tünetek mellett számos különböző tünete lehet a betegségnek. Ezeket különböző szerekkel próbálják kezelni.[13] Például klozapint használnak pszichózisra, kolinészteráz gátlókat demenciában, modafinilt a somnolenciára és atomoxetint a végrehajtó funkciók zavarára.[8][13][14]
Egy bevezető tanulmány szerint donepezil szedése segíthet a betegek elesésének megelőzésében. A donepezil növeli az acetilkolin neurotranszmitter szintjét, és ez egy elfogadott terápia az Alzheimer-kór kognitív tüneteinek a kezelésére.[15] A tanulmány kimutatta, hogy a donepezilt szedő résztvevők a placebót szedőkhöz képest fele olyan gyakorisággal estek el és azok mutatták a legjelentősebb javulást, akik korábban a legtöbbször estek el.[16]
A Parkinson-kór kezelésében a klozapin megjelenése jelentette az áttörést. Ennek megjelenése előtt pszichotikus tünetek kezelése a dopamin terápiának a csökkentésén alapult vagy első generációs antipszichotikumok használatával, melyek mind rontottak a motoros funkciókon. Más atípusos antipszichotikumok közé tartoznak a kvetiapin (Seroquel), a ziprazidon (Geodon), aripiprazol (Abilify) és a paliperidon (Invega). A klozapint tartják a leghatékonyabbnak és a legkevesebb extrapiramidális tünetet okozónak.[14]
Műtéti beavatkozás[szerkesztés]
A Levodopa felfedezése előtt a sebészeti beavatkozás sokkal gyakoribb volt, de ma sokkal ritkábban nyúlnak ehhez az eszközhöz.[17]
A betegek kevesebb, mint 10%-án lehetséges elvégezni a beavatkozásokat. Három létező módszer van: a roncsolásos műtét, a mély agyi stimuláció és a transzplantációs műtét.
Jegyzetek[szerkesztés]
- ↑ Resau, James (2011. június 1.). „Genetic information from archived blood spots”. Bioanalysis 3 (11), 1173–1175. o. DOI:10.4155/bio.11.84. ISSN 1757-6180.
- ↑ Medications for Parkinson's Disease: What's on the Horizon?. [2016. december 7-i dátummal az eredetiből archiválva]. (Hozzáférés: 2021. december 17.)
- ↑ Substantia nigra and Parkinson disease. (Hozzáférés: 2021. december 17.)
- ↑ Obeso, Jose A., Beatriz (2008. április 25.). „Functional organization of the basal ganglia: Therapeutic implications for Parkinson's disease: Therapeutic Implications for Parkinson's Disease” (angol nyelven). Movement Disorders 23 (S3), S548–S559. o. DOI:10.1002/mds.22062.
- ↑ a b Parkinson’s disease in adults. (Hozzáférés: 2021. december 17.)
- ↑ Ehrt, U., J. P. (2010. február 1.). „Use of drugs with anticholinergic effect and impact on cognition in Parkinson's disease: a cohort study” (angol nyelven). Journal of Neurology, Neurosurgery & Psychiatry 81 (2), 160–165. o. DOI:10.1136/jnnp.2009.186239. ISSN 0022-3050.
- ↑ Drugs.com Know more. Be sure.. (Hozzáférés: 2021. december 17.)
- ↑ a b c d e f g h i j k l m n Samii, Ali, Bruce R (2004. május 1.). „Parkinson's disease” (angol nyelven). The Lancet 363 (9423), 1783–1793. o. DOI:10.1016/S0140-6736(04)16305-8.
- ↑ Bronstein, Jeff M., Ron L. (2011. február 1.). „Deep Brain Stimulation for Parkinson Disease: An Expert Consensus and Review of Key Issues” (angol nyelven). Archives of Neurology 68 (2). DOI:10.1001/archneurol.2010.260. ISSN 0003-9942. PMID 20937936.
- ↑ a b Ceravolo, Roberto, Carlo (2009. december 1.). „Impulse control disorders in Parkinson's disease: definition, epidemiology, risk factors, neurobiology and management” (angol nyelven). Parkinsonism & Related Disorders 15, S111–S115. o. DOI:10.1016/S1353-8020(09)70847-8.
- ↑ Morelli, Micaela, Nicola (2012. április 25.). „A 2A Receptor Antagonism and Dyskinesia in Parkinson’s Disease” (angol nyelven). Parkinson's Disease 2012, 1–8. o. DOI:10.1155/2012/489853. ISSN 2090-8083. PMID 22754707.
- ↑ Armentero, Marie Therese, Sergi (2011. december 1.). „Past, present and future of A2A adenosine receptor antagonists in the therapy of Parkinson's disease” (angol nyelven). Pharmacology & Therapeutics 132 (3), 280–299. o. DOI:10.1016/j.pharmthera.2011.07.004. PMID 21810444.
- ↑ a b Warner, Carly B., Jamie N. (2018. december 1.). „The Role of Atomoxetine for Parkinson Disease–Related Executive Dysfunction: A Systematic Review” (angol nyelven). Journal of Clinical Psychopharmacology 38 (6), 627–631. o. DOI:10.1097/JCP.0000000000000963. ISSN 1533-712X.
- ↑ a b Hasnain, Mehrul, Mark S. (2009. július 1.). „Pharmacological Management of Psychosis in Elderly Patients with Parkinsonism” (angol nyelven). The American Journal of Medicine 122 (7), 614–622. o. DOI:10.1016/j.amjmed.2009.01.025.
- ↑ Donepezil (Aricept®) Reduces Falls in People with Parkinson’s. [2011. július 19-i dátummal az eredetiből archiválva]. (Hozzáférés: 2021. december 17.)
- ↑ [10.1212/WNL.0b013e3181f6128c "Effects of a central cholinesterase inhibitor on reducing falls in Parkinson disease"]. (Hozzáférés: 2021. december 17.)
- ↑ "Surgery for Parkinson's disease". ISBN 978-1-86016-283-1.
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Management of Parkinson's disease című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
