Riboflavin-5′-foszfát
Megjelenés
| Ez a szócikk nem tünteti fel a független forrásokat, amelyeket felhasználtak a készítése során. Emiatt nem tudjuk közvetlenül ellenőrizni, hogy a szócikkben szereplő állítások helytállóak-e. Segíts megbízható forrásokat találni az állításokhoz! Lásd még: A Wikipédia nem az első közlés helye. |
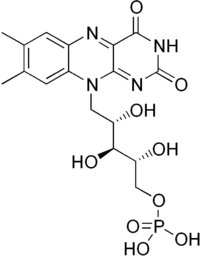
| Riboflavin-5′-foszfát | |||
| |||
| Más nevek | FMN | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 146-17-8 | ||
| PubChem | 643976 | ||
| ChemSpider | 559060 | ||
| MeSH | Flavin+mononucleotide | ||
| ChEBI | 17621 | ||
| |||
| InChIKey | FVTCRASFADXXNN-SCRDCRAPSA-N | ||
| UNII | 7N464URE7E | ||
| ChEMBL | 1201794 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C17H21N4O9P | ||
| Moláris tömeg | 456,344 g/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A riboflavin-5′-foszfát, vagy flavin-mononukleotid (FMN) a riboflavin vagy más néven B2 vitamin foszfátja. Az élő szervezetekben számos oxidoreduktáz enzim (pl.: a NADH dehidrogenáz) kofaktora.[1][2] Leggyakrabban e formában fordul elő a sejtekben és szövetekben a riboflavin (B2 vitamin), melynél több energiát igényel előállítása, de jobban oldódik vízben.[3]
Az élelmiszeriparban színezőanyagként alkalmazzák, E-kódja: E101a. Génmódosított növényekből állítják elő.
Nátriumsóját (E106) kisbabák és gyermekek számára szánt ételekben is alkalmazzák. A szervezetbe kerülése után szinte azonnal riboflavin-5′-foszfáttá alakul.[3]
Jegyzetek
[szerkesztés]- ↑ (2018. szeptember 1.) „Critical Role of Flavin and Glutathione in Complex I-Mediated Bioenergetic Failure in Brain Ischemia/Reperfusion Injury.”. Stroke 49 (5), 1223–1231. o. DOI:10.1161/STROKEAHA.117.019687. PMID 29643256. PMC 5916474.
- ↑ (2019. szeptember 1.) „Brain Ischemia/Reperfusion Injury and Mitochondrial Complex I Damage.”. Biochemistry. Biokhimiia 84 (11), 1411–1423. o. DOI:10.1134/S0006297919110154. PMID 31760927.
- ↑ a b (1998) „Covalent attachment of flavin adenine dinucleotide (FAD) and flavin mononucleotide (FMN) to enzymes: The current state of affairs”. Protein Science 7 (1), 7–20. o. DOI:10.1002/pro.5560070102. PMID 9514256. PMC 2143808.
