Szerkesztő:Fiona872/Kromatográfia
A kromatográfia, amely a görög χρώμα: kroma, szín és γραφειν: grafein írni szavak összetétele, egy keverékek elválasztására használatos laboratóriumi módszercsalád kollektív neve.
A technika lényege egy az ún. mozgó (mobil) fázisban oldott keveréknek egy álló (statikus) fázison való áthajtása, melynek során a vizsgálandó anyag elválik az elegyben található további molekuláktól.
A módszert két alapvető célra használjuk:
- preparatív vagy
- analitikai.
A preparatív kromatográfia az elválasztott vegyületek további feldolgozása a végső cél, azaz egy tisztítási műveletről beszélhetünk. Az analitikai kromatográfia általában kisebb anyagmennyiségekkel dolgozik és célja az analit relatív arányának meghatározása a keverékben. A két cél nem zárja ki egymást.
A kromatográfia története[szerkesztés]
A kromatográfia története a XIX. század közepétől a XXI. századig ível. A kromatográfia nevét a XX. század első évtizedében kapta, használata is ekkor kezdődött elsősorban növényi pigmentek, például klorofill elválasztására. Az 1930-as és 1940-es években kifejlesztett új kromatográfiás módszerek elválasztási folyamatok és kémiai analitikai feladatok széles körére tették alkalmassá a technikát, különösen a biokémia területén.
Több hasonló eljárást fejlesztettek ki a XIX. század során (sőt még korábban is), de az első igazi kromatográfia Mihail Szemjonovics Cvet orosz botanikus nevéhez köthető, aki klorofillon végzett kísérlete közben egy függőlegesen elhelyezett kalcium-karbonáttal töltött üvegcsövet használt növényi pigmentek elválasztására a XX. század első évtizedében. A módszert is ő nevezte el.
A kromatográfia modern formája Archer John Porter Martin és Richard Laurence Millington Synge az 1940-1950-es években végzett munkásságát követően alakult ki. Ők fektették le a megoszlási kromatográfia alapelveit és alapvető technikáit és munkájuk nyomán a megindult a kromatográfiás módszerek számos fajtájának (papír kromatográfia, gáz kromatográfia, valamint a manapság nagy teljesítményű folyadék kromatográfiaként ismert eljárás) gyors fejlődése. A megoszlási kromatográfia terén végzett munkásságukért Archer John Porter Martin és Richard Laurence Millington Synge 1952-ben Nobel-díjat kaptak.
Azóta a technológia gyorsan fejlődött. A kutatók megállapították, hogy a Cvet kromatofráfiáját megalapozó elvek számos módon felhasználhatók, így alakulhatott ki a kromatográfia alábbiakban bemutatott számos válfaja. Ugyanakkor a kromatográfia technikai teljesítőképessége is folyamatosan javult, egyre inkább lehetővé téve nagyon hasonló molekulák elválasztását is.
Szakkifejezések[szerkesztés]
- Analitnak nevezzük a kromatográfia során elválasztandó anyagot.
- Az analitikai kromatográfia az analit(ok) mintában való jelenlétének bizonyítását (minőségi meghatározás) valamint lehetőleg koncentrációjának meghatározását (mennyiségi elemzés) jelenti.
- Kötött vagy immobilizált fázisnak a hordozó szemcsékhez vagy az oszlop belső falához kovalens kötéssel kötött álló fázist nevezzük.
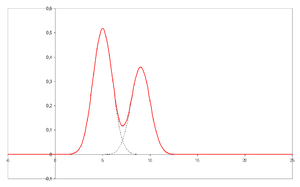
- Kromatogram a kromatográf láthatóvá tett kimeneti jele. Optimális elválasztás esetén a kromatogram különböző csúcsai vagy mintázatai az elválasztandó keverék különböző komponenseinek felelnek meg.
Az x koordináta a retenciós idő, az y koordináta pedig a rendszerből kilépő analit(ok) keltette válasz jel nagyságát. Az érzékelő berendezés lehet például spektrofotométer, tömeg spektrométer vagy számos más típusú detektor. Optimális rendszer esetén a jel arányos az elválasztott analit koncentrációjával.
- Kromatográf a készülék mellyel lehetséges a megfelelő szintű elválasztás kivitelezése, például gázkromatográf vagy folyadék kromatográf.
- A kromatográfia fizikai elválasztási módszer, ahol az elválasztandó komponensek két fázis között oszlanak meg, ezek közül az egyik helyhez kötött (álló fázis), míg a másik adott irányba mozog (mozgó fázis).
- Effluensnek nevezzük az oszlopról távozó mozgó fázist.
- A mozgó fázis egy adott irányban áramlik. Lehet folyadék (LC vagy CEC), gáz (GC) vagy szuperkritikus folyadék (szuperkritikus folyadék kromatográfia SFC). Alternatív definíció szerint a mozgó fázis az elválasztandó / vizsgálandó mintát és mintát a kolonnán átvivő oldószert tartalmazza. A mozgó fázis keresztülhalad a kromatográfiás oszlopon (az álló fázison), ahol a minta kölcsönhatásba lép az állófázissal és megtörténik az elválasztás.
- A rreparatív kromatográfia célja egy adott anyag további felhasználásra alkalmas mennyiségének tisztítása, nem pedig minőségi vagy mennyiségi meghatározása.
- A retenciós idő az adott analitnak adott körülmények között a rendszeren (a kolonna bemenettől a detektorig) való áthaladásához szükséges időtartam.
- A minta a kromatográfiával vizsgált anyag. Állhat egyetlen összetevőből vagy több komponens elegye is lehet. Ahogy a mérés során kezeljük a mintát, a vizsgált analito(ka)t tartalmazó fázist vagy fázisokat nevezzük mintának, míg a mérés során minden a vizsgált mintától elválasztott számunkra érdektelen részt hulladékként tekintünk.
- Oldott anyag megoszlási kromatográfiában a minta komponenseit jelenti
- Oldószer bármely anyag, amely képes más anyagokat oldatba vinni, különösen folyadékkromatográfiában a folyékony mozgó fázis.
- Álló fázis a kromatográfiás eljárás során helyben rögzített anyag, mint például vékonyréteg kromatográfiában a szilika réteg.
A kromatográfia fajtái a kromatográfiás ágy alakja szerint[szerkesztés]
Oszlopkromatográfia[szerkesztés]
Oszlopkromatográfiás elválasztási technika esetén az állófázis egy csőben található. A szilárd állófázis szemcséi vagy a hordozóra felvitt folyékony állófázis a cső teljes térfogatát megtöltheti (töltött oszlop) vagy a cső fala mentén koncentrálódhat nyitott, akadálymentes utat hagyva a mozgó fázisnak a cső középső részén (nyitott cső oszlop). A közegen való áthaladás sebesség különbségét a minta különböző retenciós ideiből számoljuk.
1978-ban W.C. Still új módosítását vezette be, melyet flash oszlop kromatográfiának nevezett.[2] Az eljárás nagyon hasonlít a hagyományos oszlop kromatográfiához, az eltérés csak annyi, hogy az oldószert nyomás alkalmazásával visszük át az oszlopon. Így a legtöbb elválasztás kevesebb, mint 20 perc alatt kivitelezhető, és az elválasztás is jobb, mint a hagyományos módszernél. A modern flash kromatográfiás rendszereket előre csomagolt műanyag oszlopként árulják és az oldószert a töltött oszlopon vezetik keresztül. A rendszert detektorokkal vagy frakció szedőkkel bővíthetjük lehetővé téve az automatizálást. A gradiens pumpák bevezetése gyorsabb elválasztást és kisebb oldószer felhasználást eredményezett.
Léteznek olyan segédprogramok a flash kolonnák sikeres fejlesztéséhez, melyek megbecsülik az analitok retenciós térfogatát, a sávok szélességét, az egyes analitokat tartalmazó frakciók számát és a szomszédos csúcsok közötti elválást. Így a felhasználó még a flash kolonna használatba vétele előtt kiválaszthatja a preparatív elválasztáshoz szükséges optimális paramétereket. [3]
Az expanded bed adsorption (EBA) az oszlopkromatográfia egy speciális változata, ahol a hagyományos szilárd fázisú töltött oszlop helyett, a oszlopban a szemcsék fluidizált állapotban vannak. Ezáltal lehetséges a kezdeti tisztítási lépések, mint például a centrifugálás és a szűrés elhagyása tenyészetek vagy roncsolt sejtek esetén.
Síkkromatográfia[szerkesztés]

A síkkromatográfia olyan elválasztási technika, ahol az állófázis síkban helyezkedik el vagy sík lemezre viszik fel. Ez a sík lehet papír, melyet önmagában használunk vagy melyet valamilyen anyaggal impregnálva kapjuk az állófázist (papírkromatográfia). A másik lehetőség, hogy szilárd szemcsékből álló réteget viszünk valamilyen hordozóra, például üveglemezre vagy alumínium fóliára (vékonyréteg kromatográfia). A minta elegyben levő különböző vegyületek eltérő távolságra vándorolnak attól függően, hogy milyen erősen kötődnek az állófázishoz a mozgó fázishoz viszonyítva. Az egyes vegyületekre jellemző visszatartási tényező (angolul retardation factor - Rf) segíthet az ismeretlen anyagok azonosításában.
Papírkromatográfia[szerkesztés]
Ennél az eljárásnál egy speciális kromatográfiás papírcsík egyik végére cseppentjük fel a mintaoldatot. A papírcsíkot vékony rétegben oldószert tartalmazó edénybe állítjuk, melyet ezután lefedünk. Ahogy az oldószer végighalad a papíron, áthalad a minta elegyen, amely az oldószerrel együtt vándorolni kezd. A kromatográfiás papír cellulózból készül, ami poláris anyag, így a minta kevésbé poláris komponensei messzebb vándorolnak. A polárisabb vegyületek gyorsabban kötődnek a cellulóz papírhoz, így kevésbé vándorolnak.
Vékonyréteg-kromatográfia (VRK, angolul thin layer chromatography, TLC)[szerkesztés]
A vékonyréteg kromatográfia (VRK) a papírkromatográfiához hasonlító széles körben alkalmazott laboratóriumi eljárás. Állófázisként papír helyett lapos, inert hordozóra felvitt SiO2, Al2O3 vagy cellulóz helyettesíti. Előnye a papírhoz képest a rövidebb futási idő, a jobb elválasztás és a különböző adszorbensek közötti választás lehetősége. Még jobb elválasztás és mennyiségi meghatározás érhető el nagy teljesítményű VRK angolul High Performance Thin Layer Chromatography HPTLC alkalmazásával.
A kromatográfia fajtái a mozgófázis halmazállapota szerint[szerkesztés]
Gázkromatográfia (GC)[szerkesztés]
A gázkromatográfia (GC), amelyet gáz-folyadék kromatográfiaként (GLC) is emlegetnek, olyan elválasztási technika, melynél a mozgó fázis gáz. A gázkromatográfia tetszőleges halmazállapotú, de az esetek többségében gáz- vagy folyadékminták összetételének meghatározására használt analitikai módszer. A mérés két részből áll: mérés-előkészítésből (ami esetünkben a gázelegy alkotóinak a szétválogatása) és magából a mérésből az érzékelő rendszeren.
A mérés előkészítése során először a gázneművé alakított (vagy már gáznemű) mérendő mintát egy másik, semleges gázba, a folyamatosan áramló úgynevezett vivőgázba juttatjuk. A mintát már tartalmazó vivőgáz az állófázist tartalmazó kolonnába kerül, amelyben nagy felületű anyagot tartalmazó szilárd szemcsék helyezkednek el. Az állófázis vagy egy kis átmérőjű üvegcső belső falához kötött (kapilláris kolonna) vagy valamilyen szilárd anyaggal töltött nagyobb átmérőjű fém cső (töltött kolonna). A gázkromatográfia az analit megoszlási egyensúlyán alapul a szilárd vagy szilárd hordozóra felvitt folyékony állófázis (gyakran folyékony szilikon alapú anyag) és egy áramló gáz (leggyakrabban hélium) között. Széleskörűen alkalmazzák az analitikai kémiában; gyakori biokémiai alkalmazása is, annak ellenére, hogy a GC-nél használt magas hőmérséklet miatt alkalmatlan a nagy molekulatömegű biopolimerek vagy fehérjék elemzésére, mivel ezek a hő hatására denaturálódnak. Nagyon jól használható petrokémiai, környezet monitorozási és vegyipari területen. Kémiai kutatások során is gyakran alkalmazzák.
Folyadékkromatográfia (LC)[szerkesztés]
A folyadékkromatográfia (LC) olyan elválasztási technika, melyben a mozgófázis folyadék. Folyadékkromatográfiát akár kolonnán, akár síkban végezhető. Napjainkban a folyadékkromatográfiás alkalmazásokban általában kis méretű részecskékből álló tölteteket és viszonylag nagy nyomást használnak, ezért a technikát nagy teljesítményű (vagy nagynyomású)folyadékkromatográfiának nevezik.
A HPLC avagy nagy teljesítményű folyadékkromatográfia (angolul High Performance Liquid Chromatography, vagy High Pressure Liquid Chromatography) a biokémiában és analitikai kémiában vegyületek elválasztására, azonosítására és mennyiségi meghatározására gyakran használt kromatográfiás eljárás.
A HPLC rendszer a következő alkotórészekből áll: a kromatográfiás töltetet (állófázist) tartalmazó oszlopból (kolonnából), a mobil fázist (mozgó fázist, eluenst) az oszlopon átnyomó pumpából valamint a molekulák retenciós (visszatartási) idejét jelző detektorból. A retenciós idő az álló fázis, a vizsgált molekula és a mozgó fázis közötti kölcsönhatásoktól függ.
A HPLC-s technikában a mintát a szabálytalan vagy gömb alakú szemcsékkel töltött vagy potrózus monolit rétegből készült kolonnán (álló fázis) nyomják keresztül nagy nyomáson valamilyen folyadékkal (mozgó fázis). A mozgó és álló polaritása alapján a HPLC-s alválasztásokat két csoportba sorolhatjuk. Normál fázisú folyadékkromatográfiáról (angolul normal phase liquid chromatography - NPLC) beszélünk, ha ha az állófázis polárisabb mint a mozgó fázis, míg az ellenkezőjét fordított fázisú folyadék kromatográfiának (angolul reversed phase liquid chromatography - RPLC) nevezzük.
Szuperkritikus folyadékkromatográfia (SFC)[szerkesztés]
Szuperkritikus folyadékkromatográfiában a mozgó fázis a kritikus hőmérsékletet és nyomást megközelítő vagy azt meghaladó folyadék.
A kromatográfia fajtái az elválasztás mechanizmusa szerint[szerkesztés]
Ioncserés kromatográfia (IEC)[szerkesztés]
Ioncserés kromatográfia esetén a retenció az töltéssel rendelkező ionok vagy molekulák (akár aminosavak, peptidek és fehérje|fehérjék) és az álló fázishoz kötött töltéssel rendelkező helyek között létrejövő kölcsönhatáson alapszik. Az elválasztást általában kolonnán végzik, de sikkromatográfiás megoldás is elképzelhető. A hagyományos módszereknél az állófázis töltött funkciós csoportokat hordozó ioncserélő gyanta. Az ioncserés kromatográfiát általánosan használják fehérjék tisztítására.
Méretkizárásos kromatográfia (SEC)[szerkesztés]
A méretkizárásos kromatográfia (angolul: size exclusion chromatography, rövidítve: SEC), melyet gél permeációs kromatográfiaként vagy gélszűréses kromatográfiaként is említenek, méret (vagy pontosabban hidrodinamikai átmérőjük vagy hidrodinamikai térfogatuk) alapján választja el a részecskéket. A kisebb molekulák képesek belépni az állófázis pórusaiba, így lassabban eluálódnak, míg a nagyobb molekulák ki vannak zárva a pórusokból így elúciójuk gyorsabb. Általában csak kis felbontás érhető el vele, ezért általában csak a tisztítás utolsó lépéseként használják. Hasznos még tisztított fehérjék harmadlagos vagy negyedleges szerkezetének meghatározásában. Az eljárást széleskörűen alkalmazzák poliszacharidok molekulatömegének meghatározására.
Affinitáskromatográfia[szerkesztés]
Az affinitás kromatográfia[4] biokémiai elegyek nagymértékben specifikus biológia kölcsönhatásán alapuló kromatográfiás módszer. Ilyen biológia kölcsönhatás például a az antigén és antitest vagy enzim és szubsztrát illetve receptor és ligandum közötti kapcsolat. Általában molekulák heterogén csoportját tartalmazó oldatból, pl. sejt lizátumból, vérszérumból vagy más biológiai anyagból indulunk ki. A keresett molekula egy jól ismert és definiált tulajdonságát használjuk ki az affinitásos tisztítás során. A célmolekulát megkötjük egy állófázis felületén. Mivel a többi molekula nem képes erre a specifikus kölcsönhatásra, ezek nem kötődnek meg az állófázison. Az állófázist ezután eltávolítjuk az elegyből, mossuk, majd a keresett molekulát eluáljuk az állófázisról.
Speciális technikák[szerkesztés]
Fordított fázisú kromatográfia[szerkesztés]
A fordított fázisú HPLC (Reversed phase HPLC, RP-HPLC vagy RPC) esetén az állófázis felülete apoláris, míg a mozgó fázis poláris, jellemzően víz és valamely szerves oldószer elegye. Gyakran használt álló fázis az RMe2SiCl-dal kezelt szilika, ahol R valamilyen egyenes szénláncú alkil csoport, pl. C18H37 vagy C8H17. Ilyen álló fázisokat alkalmazva az apolárosabb molekulák retenciós ideje hosszabb, míg a poláros molekulák gyorsabban eluálódnak. Apoláros oldószert adva a mozgó fázishoz növelhetjük, míg hidrofilebb oldószer hozzáadásával pedig csökkenthetjük a retenciós időt. Az RP-HPLC használata annyira elterjedt, hogy gyakran tévesen HPLC-ként emlegetik, minden további pontosítás nélkül.
Kétdimenziós kromatográfia[szerkesztés]
In some cases, the chemistry within a given column can be insufficient to separate some analytes. It is possible to direct a series of unresolved peaks onto a second column with different physico-chemical (Chemical classification) properties. Since the mechanism of retention on this new solid support is different from the first dimensional separation, it can be possible to separate compounds that are indistinguishable by one-dimensional chromatography. Sablon:Expand-section
Szimulált mozgóágyas kromatográfia[szerkesztés]
Egy elméletileg kidolgozott preparatív célra használandó mozgóágyas kromatográfiától folyamatos működtetése révén nagyobb teljesítményt várhatnánk el, mint egy rögzített ágyas készüléktől. Ennek a gyakorlati kivitelezése azonban nehéz feladat, mert ez egy igen sűrű szuszpenzió (iszap) szabályozott sebességű mozgatásával járna.
A szimulált módszer, ami a rögzített ágyas módszernek közelítő változata, ezt a problémát úgy oldja meg, hogy az ágy mozgatása helyett a minta és az oldószer betáplálási helye és az analit, valamint a hulladék (ill. a második komponens) távozási helye változik folyamatosan, ami azt az érzést kelti mintha az ágy haladna.[5] in [6], and [7]
A fő hátrány ezzel az, hogy az egyszerű kromatográfiával ellentétben a mintát csak két komponensre tudja szétválasztani.
A módszernek egyre több az alkalmazási területe. Aminosavak egyedi szétválasztására a Google kereső említ egy magyar eredetű angol nyelvű cikket is [8]
Ipari léptékű megvalósítása az izocukor (glükóz-fruktóz oldat) komponenseinek szétválasztása Ca-ionokkal telített kationcserélő gyantán. A fruktóz tartalom 42%/összcukor tartalomról 90-95%-ra növelhető. Köbméteres nagyságrendű oszlopokkal tonnás tételben gyártják a fruktózt.
Simulated Moving-Bed Chromatography[szerkesztés]
Sablon:Details Sablon:Expand-section
Pirolízissel kapcsolt kromatográfia[szerkesztés]
Gyors protein folyadékkromatográfia[szerkesztés]
Ellenáramú kromatográfia[szerkesztés]
Királis kromatográfia[szerkesztés]
Pyrolysis gas chromatography[szerkesztés]
Fast protein liquid chromatography[szerkesztés]
Sablon:Details Fast protein liquid chromatography (FPLC) is a term applied to several chromatography techniques which are used to purify proteins. Many of these techniques are identical to those carried out under high performance liquid chromatography, however use of FPLC techniques are typically for preparing large scale batches of a purified product.
Countercurrent chromatography[szerkesztés]
Sablon:Details Countercurrent chromatography (CCC) is a type of liquid-liquid chromatography, where both the stationary and mobile phases are liquids. It involves mixing a solution of liquids, allowing them to settle into layers and then separating the layers.
Chiral chromatography[szerkesztés]
Chiral chromatography involves the separation of stereoisomers. In the case of enantiomers, these have no chemical or physical differences apart from being three dimensional mirror images. Conventional chromatography or other separation processes are incapable of separating them. To enable chiral separations to take place, either the mobile phase or the stationary phase must themselves be made chiral, giving differing affinities between the analytes. Chiral chromatography HPLC columns (with a chiral stationary phase) in both normal and reversed phase are commercially available.
Hívatkozások[szerkesztés]
- ↑ IUPAC Nomenclature for Chromatography IUPAC Recommendations 1993, Pure & Appl. Chem., Vol. 65, No. 4, pp.819-872, 1993.
- ↑ Still, W. C.; Kahn, M.; Mitra, A. J. Org. Chem. 1978, 43(14), 2923-2925. (doi:10.1021/jo00408a041)
- ↑ Fair, J. D.; Kormos, C. M. J. Chromatogr. A 2008, 1211(1-2), 49-54. (doi:10.1016/j.chroma.2008.09.085)
- ↑ Pascal Bailon, George K. Ehrlich, Wen-Jian Fung and Wolfgang Berthold, An Overview of Affinity Chromatography, Humana Press, 2000. ISBN 978-0-89603-694-9, ISBN 978-1-60327-261-2.
- ↑ Bailly, M. and Nicoud, R.-M. (LSGC-ENSIC, 1, rue Grandville, 54001 Nancy and SEPAREX, 5, rue Monod, 54250, Champigneulle, France): The simulated moving bed: a powerful process for purification
- ↑ Rivat, C. and Stoltz, J.F. (Institut national de la santé et de la recherche médicale (France)). Biotechnology of Blood Proteins — Purification, Clinical and Biological Applications. John Libbey Eurotext. ISBN 2742000070 (1993)
- ↑ [www.arifractal.com/What%20is%20SMB%20chromatography.pdf What is simulated moving bed chromatography (SMB chromatography)?]. (Hozzáférés: 2008. július 5.)
- ↑ Cite web-hiba: az url paramétert mindenképpen meg kell adni![[(1)University of Veszprem, Department of Chemical Engineering, P.O. Box 158 8201 Veszprem, Hongrie, and (2) Gedeon Richter Pharmaceutical Works, P.O. Box 1475 Budapest, Hongrie|Molnár(1), Zoltán]]; Nagy, M. Aranyi(2), A. Hanak, L. Argyelán, J. Pencz, I. Szanya, T.: (Revue). Journal of Chromatography, ISSN: 0021-9673, CODEN: JOCRAM. Elsevier, Amsterdam, Pays-Bas, 1958 (Hozzáférés: 2008. július 5.)
Forrás[szerkesztés]
Ez a szócikk részben vagy egészben a Chromatography című angol Wikipédia-szócikk fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Külső hivatkozások[szerkesztés]
további információk találhatók
- IUPAC Nomenclature for Chromatography
- ChromediaOn line database and community for chromatography practitioners
- "Expanded-bed adsorption", at Modern Drug Discovery
- Reversed phase chromatography article (dutch)
- Library 4 Science: Chrom-Ed Series
- Overlapping Peaks Program - Learning by Simulations
- Chromatography Videos - MIT OCW - Digital Lab Techniques Manual
- Chromatography Equations Calculators - MicroSolv Technology Corporation