Kálium-szuperoxid
| kálium-szuperoxid | |||
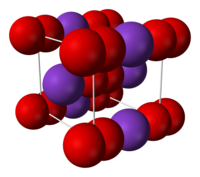 a kálium-szuperoxid elemi cellája | |||
| IUPAC-név | kálium-dioxid | ||
| Más nevek | kálium-szuperoxid | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 12030-88-5 | ||
| PubChem | 61541 | ||
| EINECS-szám | 234-746-5 | ||
| RTECS szám | TT6053000 | ||
| |||
| |||
| InChIKey | CLSKHAYBTFRDOV-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | KO2 | ||
| Moláris tömeg | 71,0971 g/mol | ||
| Megjelenés | sárga szilárd anyag | ||
| Sűrűség | 2,14 g/cm³, szilárd | ||
| Olvadáspont | 560 °C bomlik | ||
| Oldhatóság (vízben) | bomlik | ||
| Kristályszerkezet | |||
| Kristályszerkezet | tércentrált köbös (O2−) | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH |
−283 kJ·mol−1[1] | ||
| Standard moláris entrópia S |
117 J·mol−1·K−1[1] | ||
| Veszélyek | |||
| Főbb veszélyek | korrozív, oxidálószer | ||
| NFPA 704 | |||
| R mondatok | 8-14-34 | ||
| S mondatok | 17-27-36/37/39 | ||
| Rokon vegyületek | |||
| Azonos kation | kálium-oxid kálium-peroxid | ||
| Azonos anion | nátrium-szuperoxid | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A kálium-szuperoxid szervetlen vegyület, a kálium egyik oxidja, képlete KO2. Sárga színű, paramágneses anyag, nedves levegő hatására elbomlik. Egyik ritka példája a szuperoxidion stabil sóinak. Szén-dioxid- és vízmegkötőszerként, illetve oxigéngenerátorként használják lélegeztetőkészülékekben, űreszközökben, tengeralattjárókon és az űrruhák életfenntartó rendszerében.
Előállítása és reakciói[szerkesztés]
Olvadt kálium tiszta oxigénben történő égetésével állítják elő.[2]
- K + O2 → KO2
A sóban K+ és O2− ionok találhatók, melyeket ionos kötés tart össze. Az O−O kötéstávolság 128 nm.[3]
Reakciókészsége[szerkesztés]
Hidrolízise során oxigén és bázis keletkezik:
- 4 KO2 + 2 H2O → 4 KOH + 3 O2
Szén-dioxiddal karbonátok keletkezése közben bomlik:
- 4 KOH + 2 CO2 → 2 K2CO3 + 2 H2O
A fenti két reakció kombinációja is előfordul:
- 4 KO2 + 2 CO2 → 2 K2CO3 + 3 O2
- 4 KO2 + 4 CO2 + 2 H2O → 4 KHCO3 + 3 O2
Laboratóriumi reagensként csak ritkán használják. Mivel vízzel reagál, többnyire szerves oldószerekben vizsgálják. Mivel a só apoláris oldószerekben rosszul oldódik, jellemzően koronaétereket használnak. A tetraetilammónium só is ismert. Ezen sók jellegzetes reakciói a szuperoxid nukleofilként történő alkalmazása, például alkil-bromidok alkoholokká és savkloridok diacil-peroxidokká történő alakításához.[4]
Felhasználása[szerkesztés]
Az orosz űrhajózás sikeresen alkalmazta a kálium-szuperoxidot az űrruhák és a Szojuz űrhajók kémiai oxigéngenerátoraiban. Tűzoltók és bányászok lélegeztető készülékeiben is használják a KO2-t, vízzel történő heves reakciójának veszélye miatt azonban a búváreszközökben csak korlátozottan alkalmazzák. Egy kg KO2 elméletileg 0,618 kg CO2-t képes megkötni, miközben 0,380 kg O2 szabadul fel belőle. Egy KO2 molekula egy molekula CO2-vel reagál, de csak 0,75 oxigénmolekula keletkezik. Az emberi test azonban kevesebb CO2 molekulát termel, mint amennyi oxigénmolekulára szüksége van, mivel a táplálék oxidációja ahhoz is oxigént igényel, hogy azt vízzé és karbamiddá alakítsa.
Veszélyei[szerkesztés]
Erélyes oxidálószer, számos anyaggal, például vízzel, savakkal, szerves anyagokkal vagy porított grafittal keverve robbanásszerű hevességgel reagálhat. Még száraz állapotban is ütésre érzékeny robbanókeveréket képezhet szerves olajokkal, például petróleummal keverve.[5] 1999-ben az Oak Ridge National Laboratory területén a NaK fémötvözet szivárgása nyomán keletkezett kálium-oxidok feltakarítása közben robbanás történt, melyet az okozott, hogy az ásványi olajjal telítődött anyagból ütésérzékeny robbanókeverék keletkezett.[6]
Jegyzetek[szerkesztés]
- ↑ a b Zumdahl, Steven S.. Chemical Principles 6th Ed.. Houghton Mifflin Company, A22. o. (2009). ISBN 0-618-94690-X
- ↑ Harald Jakob, Stefan Leininger, Thomas Lehmann, Sylvia Jacobi, Sven Gutewort “Peroxo Compounds, Inorganic” Ullmann's Encyclopedia of Industrial Chemistry, 2007, Wiley-VCH, Weinheim. doi:10.1002/14356007.a19_177.pub2
- ↑ Abrahams, S. C.; Kalnajs, J. "The Crystal Structure of α-Potassium Superoxide" Acta Crystallographica (1955) volume 8, pages 503-506. doi:10.1107/S0365110X55001540.
- ↑ Roy A. Johnson, Javier Adrio, María Ribagorda "Potassium Superoxide" e-EROS Encyclopedia of Reagents for Organic Synthesis, 2001 John Wiley & Sons. doi:10.1002/047084289X.rp250.pub2
- ↑ Aerojet Nuclear Company. An Explosives Hazards Analysis of the Eutectic Solution of NaK and KO2. Idaho National Engineering Laboratory (1975)
- ↑ Y-12 NaK Accident Investigation. U.S. Department of Energy, 2000. február 1. [2010. május 28-i dátummal az eredetiből archiválva].
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Potassium superoxide című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.

