Etindiol
| etindiol | |||
Az etindiol szerkezeti képlete | |||
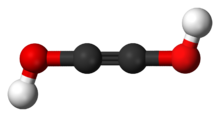 Az etindiol pálcikamodellje | |||
| IUPAC-név | etin-1,2-diol | ||
| Más nevek | acetiléndiol, dihidroxiacetilén | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| PubChem | 9942115 | ||
| ChemSpider | 8117727 | ||
| |||
| |||
| InChIKey | ZUQAPLKKNAQJAU-UHFFFAOYSA-N | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C2H2O2 | ||
| Moláris tömeg | 58,07 g/mol | ||
| Forráspont | Bomlik | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Az etindiol vagy acetiléndiol az acetilén diolja, szerkezeti képlete HO−C≡C−OH. Kondenzált fázisban instabil vegyület. Tautomerje – a glioxál (H(C=O)2H) – jól ismert.
Származékai[szerkesztés]
Bár az etindiol bomlékony, az etindiolát (acetiléndiolát) dianion (O−C≡C−O)2− sói jól ismertek. Ezek a fémorganikus vegyületek formálisan az etindiolból vezethetők le két proton leadásával, de általában nem így keletkeznek.
Ezeket a sókat jellemzően szén-monoxid redukciójával állítják elő. Kálium-etindiolátot (K2C2O2 ) elsőként Liebig állított elő 1834-ben: szén-monoxidot reagáltatott fémkáliummal;[1] de a terméket sokáig „kálium-karbonilnak” (KCO) tartották. A következő 130 év során leírták a nátrium (Johannis, 1893), bárium (Gunz and Mentrel, 1903), stroncium (Roederer, 1906) és a lítium, rubídium és cézium (Pearson, 1933) „karboniljait” is.[2] Végül kimutatták, hogy a reakció termékeként kálium-etindiolát K2C2O2 és kálium-benzolhexolát K6C6O6 keveréke keletkezik.[3]
E sók tényleges szerkezetét csak 1963-ban tisztázta Werner Büchner és E. Weiss.[4][5]
Etindiolátok előállíthatók CO és a megfelelő fém ammóniás oldatának alacsony hőmérsékleten végzett gyors reakciója révén is.[2] A kálium-etindiolát halványsárga szilárd anyag. Robbanásszerűen reagál levegővel, halogénekkel, halogénezett szénhidrogénekkel, alkoholokkal, vízzel és bármely egyéb, savas hidrogént tartalmazó anyaggal.[6]
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben az Acetylenediol című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások[szerkesztés]
- ↑ Justus Liebig (1834), Annalen der Chemie und Pharmacie, volume 11, p. 182. Cited by Raymond N. Vrtis et al (1988), JACS p. 7564.
- ↑ a b T. G. Pearson (1933), Carbonyls of Lithium, Rubidium and Caesium. Nature, volume 131, pp. 166–167 (04 February 1933). doi:10.1038/131166b0
- ↑ Werner Büchner, E. Weiss (1964) Zur Kenntnis der sogenannten «Alkalicarbonyle» IV[1] Über die Reaktion von geschmolzenem Kalium mit Kohlenmonoxid. Helvetica Chimica Acta, Volume 47 Issue 6, Pages 1415–1423.doi:10.1002/hlca.19640470604
- ↑ Werner Büchner, E. Weiss (1963) Zur Kenntnis der sogenannten «Alkalicarbonyle» I Die Kristallstruktur des Kalium-acetylendiolats, KOC≡COK. Helvetica Chimica Acta, Volume 46 Issue 4, Pages 1121–1127. doi:10.1002/hlca.19630460404
- ↑ E. Weiss, Werner Büchner (1963), Zur Kenntnis der sogenannten Alkalicarbonyle. II. Die Kristallstrukturen des Rubidium- und Caesium-acetylendiolats, RbOC≡CORb und CsOC≡COCs. Zeitschrift für anorganische und allgemeine Chemie, Volume 330 Issue 5-6, Pages 251–258. doi:10.1002/zaac.19643300504
- ↑ Charles Kenneth Taylor (1982), The Chemical Behavior of the Alkali Metal Acetylenediolates. Thesis, Pennsylvania State University; also Technical Memo A642321, Penn State University Park Applied Research Lab. 227 pages.
