„Rubídium-oxalát” változatai közötti eltérés
Új oldal, tartalma: „{{Vegyület infobox | név = rubídium-oxalát | kép = Rubidiumion.svg | képméret = 60px | képaláírás = rubídiumion | kép2 = Oxalation.svg | képméret2 = 100p…” Címke: HTML-sortörés |
(Nincs különbség)
|
A lap 2013. november 17., 16:40-kori változata
| rubídium-oxalát | |

| |
| rubídiumion | |
| |
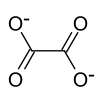
| oxalátion | |
| Kémiai azonosítók | |
| CAS-szám | 7243-75-6 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | Rb2C2O4 |
| Moláris tömeg | * 258.97 g·mol−1 (vízmentes)
|
| Megjelenés | színtelen, fakó kristályok |
| Sűrűség | 2,76 g·cm−3[1](monohidrát) |
| Olvadáspont | bomlik |
| Oldhatóság (vízben) | oldódik |
| Veszélyek | |
| Főbb veszélyek | nincs adat |
| Rokon vegyületek | |
| Azonos kation | rubídium-oxid rubídium-hidroxid |
| Az infoboxban SI-mértékegységek szerepelnek. Ahol lehetséges, az adatok standardállapotra (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. Az ezektől való eltérést egyértelműen jelezzük. | |
A rubídium-oxalát az oxálsav rubídiumsója képlete Rb2C2O4.
Előállítása
Rubídium-karbonát és oxálsav reakciójával állítható elő:[2]
Hevítés hatására rubídium-formiátra és hidrogénre bomlik:
Tulajdonságai
A rubídium-oxalát monohidrátként kristályosodik, kristályszerkezete monoklin,[1] és izomorf a kálium-oxalát monohidráttal.[3] Szobahőmérsékleten vízmentesen két különböző változata van: az egyik monoklin és izotipikus a cézium-oxaláttal, a másik ortorombos és izotipikus a kálium-oxaláttal.[4] A frissen előállítot rubídium-oxalát főként monoklin fázisú, de utána lassan, visszafordíthatatlanul ortorombos lesz.[5] 2004-ben két másik rubídium-oxalát fázist fedeztek fel amelyek magas hőmérsékleten léteznek.[6]
A rubídium-oxalát különböző kristályszerkezeteinek adatai:
| Fázis | Kristályszerkezet | Tércsoport | a in Å | b in Å | c in Å | β | Z |
|---|---|---|---|---|---|---|---|
| Alfa[4] | monoklin | P21/c | 6,328 | 10,455 | 8,217 | 98,016° | 4 |
| Béta[4] | ortorombos | Pbam | 11,288 | 6,295 | 3,622 | — | 2 |
| Monohidrát[7] | monoklin | C2/c | 9,617 | 6,353 | 11,010 | 109,46° | 4 |
A kristályos rubídium-oxalát standart entalpiája 1325,0 ± 8,1 kJ/mol.[8]
Termikus bomlásakor előbb szén-monoxidra és rubídium-karbonátra bomlik, majd szén-dioxidra és rubídium-oxidra majd 507 - 527 °C között rubídiumra és oxigénre:[5][9]
A rubídium-hidrogénoxalát RbH(COO)2 izomorf a vele analóg kálium vegyülettel,[10] és a kristályszerkezete monoklin.[11] A rubídium-tetraoxalát RbH3(COO)2 savas és dihidrátként kristályosodik, sűrűsége 18 °C-on 2,125 g/cm−3, oldhatósága vízben 21 °C-on 21 g/l.[12]
Hidrogén-peroxiddal rubídium-oxalát monoperhidrátot alkot (COO)2Rb2·H2O2, aminek a kristályszerkezete monoklin és viszonylag stabil a levegőn.[13]
Hidrogén-fluoriddal reagálva komplexet alkot:[14]
Források
- ↑ a b Jean D'Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-5406-0035-0, S. 686f. (korlátozott előnézet a Google Könyvekben)
- ↑ E. Giglio, S. Loreti, N. V. Pavel: "EXAFS: A New Approach to the Structure of Micellar Aggregates" in J. Phys. Chem., 1988, 92, S. 2858-2862. doi:10.1021/j100321a032
- ↑ Björn Pedersen: "The Equilibrium Hydrogen-Hydrogen Distances in the Water Molecules in Potassium and Rubidium Oxalate Monohydrates" in Acta Cryst., 1966, 20, S. 412ff. doi:10.1107/S0365110X66000951
- ↑ a b c R. E. Dinnebier, S. Vensky, M. Panthöfer, M. Jansen: "Crystal and molecular structures of alkali oxalates: first proof of a staggered oxalate anion in the solid state." in Inorg. Chem, 2003, 42(5), S. 1499-1507. PMID 12611516.
- ↑ a b Dissertation: "Konformationsaufklärung anorganischer Oxoanionen des Kohlenstoffs", Sascha Vensky, Universität Stuttgart, 2004. S. 117ff. PDF
- ↑ Sablon:Literatur
- ↑ Sablon:Literatur
- ↑ Y. Masuda, H. Miyamoto, Y. Kaneko, K. Hirosawa: "The standard molar enthalpies of formation of crystalline rubidium and cesium oxalates" in J. Chem. Thermodynamics, 1985, 17(2), S. 159-164. doi:10.1016/0021-9614(85)90068-0
- ↑ T. Meisel, Z. Halmos, K. Seybold, E. Pungor: "The thermal decomposition of alkali metal formates" in Journal of Thermal Analysis and Calorimetry 1975, 7(1). S. 73-80. doi:10.1007/BF01911627
- ↑ J. Piccard: "Beitrag zur Kenntniss der Rubidiumverbindungen" in Journal für Praktische Chemie 1862, 86(1), S. 449-460. doi:10.1002/prac.18620860163 Volltext
- ↑ H. Watts: "A dictionary of chemistry and the allied branches of other sciences", Band 4, Verlag Longmans, Green and Co., 1866, S. 264. (korlátozott előnézet a Google Könyvekben)
- ↑ R. Abegg, F. Auerbach: "Handbuch der anorganischen Chemie". Verlag S. Hirzel, Bd. 2, 1908. S. 435. Volltext
- ↑ B. F. Pedersen: "The Crystal Structure of Potassium and Rubidium Oxalate Monoperhydrates, K2C2O4.H2O2 and Rb2C2O4.H2O2" in Acta Chem. Scand. 1967, 21, S. 779-790. doi:10.3891/acta.chem.scand.21-0779
- ↑ R. F. Weinland, W. Stille: "Ueber die Anlagerung von Krystallfluorwasserstoff an Oxalate und an Ammoniumtartrat" in Justus Liebigs Annalen der Chemie 1903, 328(2), S. 149-153. doi:10.1002/jlac.19033280205
Ez a szócikk részben vagy egészben a Rubidiumoxalat című német Wikipédia-szócikk fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.






