„Karbonil-szulfid” változatai közötti eltérés
| [ellenőrzött változat] | [ellenőrzött változat] |
a r2.7.3) (Bot: következő módosítása: pl:Siarczek karbonylu; kozmetikai változtatások |
a r2.7.3) (Bot: következő módosítása: hi:प्रांगारल गन्धेय |
||
| 77. sor: | 77. sor: | ||
[[fi:Karbonyylisulfidi]] |
[[fi:Karbonyylisulfidi]] |
||
[[fr:Oxysulfure de carbone]] |
[[fr:Oxysulfure de carbone]] |
||
[[hi:प्रांगारल गन्धेय]] |
|||
[[hi:कार्बोनिल सल्फाइड]] |
|||
[[it:Solfuro di carbonile]] |
[[it:Solfuro di carbonile]] |
||
[[ja:硫化カルボニル]] |
[[ja:硫化カルボニル]] |
||
A lap 2012. szeptember 28., 13:38-kori változata
| Karbonil-szulfid | |||
 Karbonil-szulfid | |||
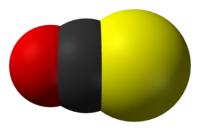 A karbonil-szulfid molekula modellje | |||
| IUPAC-név | Karbonil-szulfid | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 463-58-1 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | COS | ||
| Moláris tömeg | 60,08 g mol−1[1] | ||
| Megjelenés | Színtelen gáz | ||
| Sűrűség | 2,721 kg/m3 (gáz, normálállapotban)[1] 1,178 kg/l (folyadékfázis, forrásponton)[1] | ||
| Olvadáspont | −138,81 °C[1] | ||
| Forráspont | −50,2 °C[1] | ||
| Oldhatóság (vízben) | 1447 mg/l[1] | ||
| Veszélyek | |||
| EU osztályozás | Nagyon gyúlékony (F+), Mérgező (T)[1] | ||
| NFPA 704 | |||
| R mondatok | R12, R23[1] | ||
| S mondatok | S9, S16, S33, S36, S45[1] | ||
| Rokon vegyületek | |||
| Rokon vegyületek | Szén-dioxid Szén-diszulfid | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A karbonil-szulfid vagy szén-oxid-szulfid egy kémiai vegyület, a szén-dioxid monotioszármazékának (egy kénatomot tartalmazó származékának) tekinthető. A képlete COS. Az oxid-szulfidok közé tartozik. (Oxid-szulfidoknak nevezik azokat a vegyületeket, amelyben egy központi atomhoz nemcsak kénligandumok, hanem oxigénligandumok is kapcsolódnak.) Jellegzetes szagú gáz. Lineáris molekulákat alkot. Vízben oldható. A vegyületet Than Károly magyar kémikus fedezte fel 1867-ben.
Kémiai tulajdonságai
A karbonil-szulfid meggyújtható, égésekor szén-dioxid és kén-dioxid képződik. Könnyen bomlik szén-dioxidra és szén-diszulfidra a következő egyenlet szerint:
Vizes oldata hidrolizál, a hidrolízis során szén-dioxid és kén-hidrogén képződik. Lúgok hatására bomlik, a reakcióban karbonátok és szulfidok képződnek.
Előfordulása
A karbonil-szulfid a természetben megtalálható egyes ásványvizekben oldott állapotban, például a parádi és a harkányi ásványvizekben. A vegyület hidrolízisekor képződő szén-dioxid és kén-hidrogén adja ezeknek az ásványvizeknek a jellegzetes ízét.
Kimutatták a Vénusz légkörében is. Egyes elméletek szerint a jelenléte a bolygó légkörében ott élő mikroorganizmusokkal magyarázható.[2]
Előállítása
Karbonil-szulfid képződik szén-monoxidból és kéngőzökből magas hőmérsékleten.
Laboratóriumban előállítható kálium-tiocianátból kénsavval. Az így nyert gáz melléktermékeket tartalmaz, ezért tisztítást igényel.
Források
- Bodor Endre: Szervetlen kémia I.
- Nyilasi János: Szervetlen kémia
- Bruckner Győző: Szerves kémia, I/1-es kötet.





