Fenilacetilén
| fenilacetilén | |||
 fenilacetilén | |||

| |||
| IUPAC-név | etinilbenzol | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 536-74-3 | ||
| PubChem | 10821 | ||
| ChemSpider | 10364 | ||
| |||
| |||
| InChIKey | UEXCJVNBTNXOEH-UHFFFAOYSA-N | ||
| ChEMBL | 234833 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C8H6 | ||
| Moláris tömeg | 102,133 g/mol | ||
| Sűrűség | 0,93 g/cm³ | ||
| Olvadáspont | −45 °C | ||
| Forráspont | 142–144 °C | ||
| Savasság (pKa) | 28,7 (DMSO),[1] 23,2 (víz, extrapolált)[2] | ||
| Mágneses szuszceptibilitás | −72,01·10−6 cm³/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A fenilacetilén a szénhidrogének közé tartozó vegyület, molekulájában alkin és fenilcsoportot is található. Színtelen, viszkózus folyadék. A laboratóriumban néha az acetilén analógjaként használják, mivel folyadékként könnyebben kezelhető, mint a gáz halmazállapotú acetilén.
Előállítása[szerkesztés]
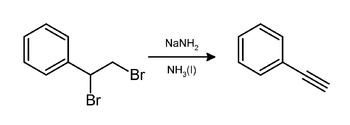
Laboratóriuma előállítása sztirol-dibromidból történhet ammóniában oldott nátrium-amid hatására végbemenő hidrogén-bromid-eliminációval:[3]
Brómsztirolból olvadt kálium-hidroxid hatására végbemenő hidrogén-bromid-eliminációval is előállítható.[4]
Reakciói[szerkesztés]
- Lindlar-katalizátor mellett hidrogénnel sztirollá redukálható (hidrogénezhető)
- fémkatalizált trimerizációs reakcióban 1,2,4- (97%) és 1,3,5-trifenilbenzollá alakul:[5]
- ródium katalizátor mellett ciklotrimerizáció megy végbe, melynek során mind 1,2,4-, mind 1,3,5-izomer keletkezik, jelentős mennyiségű aciklusos enin dimer termék mellett:[6]
- arany(III) vagy higany(II) katalizátorral acetofenonná hidratálható.
Jegyzetek[szerkesztés]
- ↑ Bordwell, F.G. Acc. Chem. Res. 1988, 21, 456-463.
- ↑ Streitwieser, A.,Jr.; Ruben, D.M.E; J. Am. Chem. Soc. 971., 93, 1794-1795.
- ↑ Kenneth N. Campbell and Barbara K. Campbell (1963). „Phenylacetylene”. Org. Synth.. ; Coll. Vol. 4: 763
- ↑ John C. Hessler (1941). „Phenylacetylene”. Org. Synth.. ; Coll. Vol. 1: 438
- ↑ (2005) „A simple cobalt catalyst system for the efficient and regioselective cyclotrimerisation of alkynes”. Chemical Communications 2005 (11), 1474–1475. o. DOI:10.1039/b417832g. PMID 15756340.
- ↑ (2003) „Oligomerization and Polymerization of Alkynes Catalyzed by Rhodium(I) Pyrazolate Complexes”. Journal of Molecular Catalysis A: Chemical 204–205, 333–340. o. DOI:10.1016/S1381-1169(03)00315-7.
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben a Phenylacetylene című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.