L-forma baktérium

- Az „L-forma” szócikk ide irányít át. A cukrok és aminosavak L-konfigurációjáról az Optikai izoméria szócikk ír.
Az L-forma baktérium (baktériumok L-formája), az angol nyelvű szakirodalomban még: L-phase bacteria, L-phase variants vagy cell wall deficient (CWD) bacteria kifejezés olyan baktériumtörzsre utal, aminek hiányzik a sejtfala.[1] Emmy Klieneberger-Nobel német származású mikrobiológus izolálta őket elsőként 1935-ben, és adta nekik az „L-forms” (L-formák) nevet, munkahelye, a londoni Lister Institute után.[2]
Két fajtáját különböztetik meg: az instabil L-formák vagy szferoplasztok osztódásra képesek, de képesek visszaalakulni sejtfallal rendelkező formára, és a stabil L-formák, amik visszaalakulásra nem képesek.
Egyes parazita életmódú baktériumokból, mint a fitoplazma vagy a mikoplazma szintén hiányzik a sejtfal,[3] de ezeket nem tekintik L-formáknak, mivel nem egyébként sejtfallal rendelkező baktériumok különleges alakváltozatai.[4]
Megjelenés, sejtosztódás[szerkesztés]
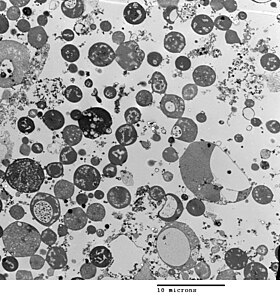
A baktériumok morfológiáját a sejtfal határozza meg. Mivel az L-formák nem rendelkeznek sejtfallal, alakjuk eltér a baktériumtörzsétől, amelyből erednek, tipikusan gömb vagy szferoid. Például a pálcika alakú Bacillus subtilis fáziskontraszt-mikroszkóp vagy transzmissziós elektronmikroszkóp alatt kerek formájúnak látszik.[5]
Bár L-formák Gram-pozitív és Gram-negatív baktériumokból egyaránt kialakulhatnak, a Gram-festés során az L-formák mindig Gram-negatív eredményt adnak a sejtfal hiánya miatt.
A sejtfalnak fontos szerepe van a sejtosztódásban is, ami a legtöbb baktérium esetében kettéosztódással (bináris hasadás) történik. Az L-formák esetén a sejtfal hiánya miatt a sejtosztódás szervezetlen, így az osztódás során a nagyon aprótól a nagyon nagyig különböző méretű sejtek jönnek létre.

A bakteriális sejtosztódás általában megköveteli a sejtfal, és a bakteriális sejtváz minden komponensének (mint pl. az FtsZ) jelenlétét. Az L-forma baktériumok képessége, hogy ezek nélkül is növekedjenek és osztódjanak merőben szokatlan, és talán egy az élet fejlődésének korábbi szakaszaiban működő sejtosztódási formát képvisel.[1] Ennek a sejtosztódási formának sajátossága, hogy vékony kitüremkedések alakulnak ki a sejt felületén, amik aztán leválnak, hogy új sejteket alkossanak.
Létrehozás kultúrában[szerkesztés]
L-formákat laboratóriumi körülmények között is létre lehet hozni egyébként sejtfallal rendelkező fajokból, mint a Bacillus subtilis vagy az Escherichia coli. Ez történhet a peptidoglikán-szintézis antibiotikummal való gátlásával, vagy a sejtfalat emésztő lizozim enzimmel való kezelés útján. Az L-formákat olyan tápközegben kell nevelni, aminek az ozmolalitása megegyező a baktérium citoszoljáéval (sejtfolyadék), azaz izotonikus oldat. Ez megakadályozza az ozmotikus sokk kialakulását.[2] A L-formák törzsei instabilak is lehetnek, azaz visszanöveszthetik a sejtfalukat. Ez megakadályozható, ha hosszú ideig azonos körülmények között tartják a baktériumkultúrát.[6]
Egyes kutatóknak sikerült az L-formák létrejöttekor történő mutációkat azonosítani.[1][2] Az egyik ilyen pontmutáció a lipidanyagcsere mevalonát-anyagcsereútjának egy enzimével kapcsolatos, és az L-formák létrejöttének gyakoriságát mintegy ezerszeresére növelte.[1] Ennek hatásmechanizmusa nem ismert, de köze lehet az enzim szerepéhez egy a peptidoglikán-szintézisben fontos lipid előállításában.
Egy másik módszer a nanotechnológia felhasználása. Mikrofluidikai eszközöket építve a peptidoglikán szintézisét a rendelkezésre álló tér korlátozásával akadályozni lehet. Egy szomszédos mikroélőhelyfoltokat és bakteriális metapopulációkat összekötő, szűk (nagyságrendileg mikrométeresnél kisebb) biológiai folyosón („vadátjárón”) keresztül történő szétszóródás után az L-formához hasonló sejtek nyerhetők.[7]
Jelentőségük, alkalmazásaik[szerkesztés]
Az L-forma baktériumok kutatása hasznos lehet az élet ősi formáinak kutatásában és a biotechnológiában.
A laboratóriumban létrehozott L-forma baktériumtörzsek létezését a természetben nem sikerült igazolni. Egyes publikációk humánpatogén L-forma baktériumok létezése mellett érveltek, de a betegség és ezen életformák közötti kapcsolat töredékes és gyakran ellentmondásos, ezért az elmélet vitatott maradt.[8][9]
A kérdésben a két végletes álláspont szerint az L-forma baktériumok vagy mindössze laboratóriumi látványosságok, vagy betegségek fontos, fel nem ismert okozói.[4] Az L-forma baktériumok kutatása folytatódik, például L-forma szervezeteket figyeltek meg egerek tüdejében, miután egy kísérletben Nocardia caviae-vel oltották be őket,[10][11] és egy tanulmány szerint az L-formák megfertőzhetnek olyan immunszupresszív gyógyszerekkel kezelt pácienseket, akik csontvelő-átültetésen estek át.[12] A sejtfal nélküli baktériumtörzsek kialakulása fontos lépés lehet a gyógyszerrezisztens baktériumok kialakulásában is.[13]
Vizsgálják az L-forma baktériumok biotechnológiai felhasználásának lehetőségét a fehérjetermelés eszközeiként.[14] Itt a sejtfal hiánya kimondottan előnyös, mivel nagy mennyiségű fehérje termelését teszi lehetővé, amik egyébként a sejthártya és a külső membrán közötti periplazmatikus térben gyűlnének fel.[15][16] A periplazmatikus térben toxikus mennyiségben felgyűlhetnek a fehérjék, ami csökkentheti a kiválasztott fehérjék hozamát.
Lásd még[szerkesztés]
Ajánlott irodalom[szerkesztés]
- Domingue, Gerald J.. Cell wall-deficient bacteria: basic principles and clinical significance. Reading, Mass: Addison-Wesley Pub. Co (1982). ISBN 0-201-10162-9
- Mattman, Lida H.. Cell wall deficient forms: stealth pathogens. Boca Raton: CRC (2001). ISBN 0-8493-8767-1
Jegyzetek[szerkesztés]
- ↑ a b c d Leaver M, Domínguez-Cuevas P, Coxhead JM, Daniel RA, Errington J (2009. February). „Life without a wall or division machine in Bacillus subtilis”. Nature 457 (7231), 849–53. o. DOI:10.1038/nature07742. PMID 19212404.
- ↑ a b c Joseleau-Petit D, Liébart JC, Ayala JA, D'Ari R (2007. September). „Unstable Escherichia coli L forms revisited: growth requires peptidoglycan synthesis”. J. Bacteriol. 189 (18), 6512–20. o. DOI:10.1128/JB.00273-07. PMID 17586646.
- ↑ Razin S, Yogev D, Naot Y (1998. December). „Molecular biology and pathogenicity of mycoplasmas”. Microbiol. Mol. Biol. Rev. 62 (4), 1094–156. o. PMID 9841667.
- ↑ a b Domingue GJ, Woody HB (1997. April). „Bacterial persistence and expression of disease”. Clin. Microbiol. Rev. 10 (2), 320–44. o. PMID 9105757. Full PDF
- ↑ Gilpin RW, Young FE, Chatterjee AN (1973. January). „Characterization of a stable L-form of Bacillus subtilis 168”. J. Bacteriol. 113 (1), 486–99. o. PMID 4631836.
- ↑ Allan EJ (1991. April). „Induction and cultivation of a stable L-form of Bacillus subtilis”. J. Appl. Bacteriol. 70 (4), 339–43. o. PMID 1905284.
- ↑ Männik J., R. Driessen, P. Galajda, J.E. Keymer, C. Dekker (2009. September). „Bacterial growth and motility in sub-micron constrictions”. PNAS 106 (35), 14861–14866. o. DOI:10.1073/pnas.0907542106. PMID 19706420.
- ↑ Onwuamaegbu ME, Belcher RA, Soare C (2005). „Cell wall-deficient bacteria as a cause of infections: a review of the clinical significance”. J. Int. Med. Res. 33 (1), 1–20. o. [2009. augusztus 24-i dátummal az eredetiből archiválva]. PMID 15651712. (Hozzáférés: 2009. március 16.)
- ↑ Casadesús J (2007. December). „Bacterial L-forms require peptidoglycan synthesis for cell division”. Bioessays 29 (12), 1189–91. o. DOI:10.1002/bies.20680. PMID 18008373.
- ↑ Beaman BL (1980. July). „Induction of L-phase variants of Nocardia caviae within intact murine lungs”. Infect. Immun. 29 (1), 244–51. o. PMID 7399704.
- ↑ Beaman BL, Scates SM (1981. September). „Role of L-forms of Nocardia caviae in the development of chronic mycetomas in normal and immunodeficient murine models”. Infect. Immun. 33 (3), 893–907. o. PMID 7287189.
- ↑ Woo PC, Wong SS, Lum PN, Hui WT, Yuen KY (2001. March). „Cell-wall-deficient bacteria and culture-negative febrile episodes in bone-marrow-transplant recipients”. Lancet 357 (9257), 675–9. o. DOI:10.1016/S0140-6736(00)04131-3. PMID 11247551.
- ↑ Fuller E, Elmer C, Nattress F, et al (2005. December). „Beta-lactam resistance in Staphylococcus aureus cells that do not require a cell wall for integrity”. Antimicrob. Agents Chemother. 49 (12), 5075–80. o. [2009. május 29-i dátummal az eredetiből archiválva]. DOI:10.1128/AAC.49.12.5075-5080.2005. PMID 16304175. (Hozzáférés: 2010. augusztus 15.)
- ↑ Gumpert J, Hoischen C (1998. October). „Use of cell wall-less bacteria (L-forms) for efficient expression and secretion of heterologous gene products”. Curr. Opin. Biotechnol. 9 (5), 506–9. o. DOI:10.1016/S0958-1669(98)80037-2. PMID 9821280.
- ↑ Rippmann JF, Klein M, Hoischen C, et al (1998. december 1.). „Procaryotic expression of single-chain variable-fragment (scFv) antibodies: secretion in L-form cells of Proteus mirabilis leads to active product and overcomes the limitations of periplasmic expression in Escherichia coli”. Appl. Environ. Microbiol. 64 (12), 4862–9. o. PMID 9835575.
- ↑ Choi JH, Lee SY (2004. June). „Secretory and extracellular production of recombinant proteins using Escherichia coli”. Appl. Microbiol. Biotechnol. 64 (5), 625–35. o. DOI:10.1007/s00253-004-1559-9. PMID 14966662.
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben az L-form bacteria című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
