Interkalkogének
|
|
Ez a szócikk vagy szakasz lektorálásra, tartalmi javításokra szorul. |
A kalkogének (oxigéncsoport elemei) egymás közötti reakciójában interkalkogének keletkeznek.[1]
A kalkogének elektronegativitása között nagy különbségek vannak: az oxigéné 3,44, a polóniumé 2,0. A csoportban lefelé haladva az elemek fémes jellege növekszik. Az oxigén nemfém és gáz, a polónium ezüstös színű másodfajú fém.[* 1] Emiatt az interkalkogénekben sokféle kötéstípus előfordul: ionos, kovalens, fémes és félfémes kötés is lehetséges.[1]
Ismert interkalkogének[szerkesztés]
| O | S | Se | Te | Po | |
|---|---|---|---|---|---|
| O | |||||
| S | |||||
| Se | |||||
| Te | |||||
| Po |
Az interkalkogének kötései[szerkesztés]
A fenti táblázatban lefelé haladva átmenet van a kovalens kötésből (diszkrét molekulák) az ionos kötés felé. A táblázatban balról jobbra haladva átmenet van az ionos kötésből a fémes kötés felé. Kovalens kötés két nagy elektronegativitású elem között fordul elő; ionos kötés két nagyon különböző – az egyik kicsi, a másik nagy – elektronegativitású elem között fordul elő; fémes kötés két kis elektronegativitású elem között fordul elő.) Például, a táblázat bal szélén (oxigének közti kötések), az O2 és a O3 tisztán kovalens, a SO2 és a SO3 poláris molekulák, a SeO2 molekulák egydimenziós láncot alkotnak, a TeO2 rétegzett polimert képez (az atomok két dimenzióban kapcsolódnak egymáshoz), a PoO2 ionvegyület és fluorit szerkezetű térrácsot alkot. A táblázat alján (a polónium kötései) a PoO2 és a PoS ionvegyület, a PoxSey és a PoxTey félfém, a Po∞ fém.[1]
Az ismert interkalkogének összefoglalása[szerkesztés]
A kén kalkogenidjei[szerkesztés]

- kén-oxidok, SxOy, ahol az X:Y aránya kisebb, mint 1:2
- dikén-monoxid, S2O
- dikén-dioxid, S2O2
- kén-monoxid, SO
- kén-dioxid, SO2
- kén-trioxid, SO3
- kén-oxidok, SOx, ahol x>3
A szelén kalkogenidjei[szerkesztés]

- szelén-dioxid, SeO2
- szelén-trioxid, SeO3
- Különböző vegyületek, ahol a szelén és a kén különböző koncentrációban félfémes kötéssel kapcsolódnak egymáshoz SexSy
- szelén-monoszulfid, SeS
- szelén-diszulfid, SeS2, valójában gyűrűs Se3S5 és Se2S6 2:1 arányú keveréke
- szelén-hexaszulfid, Se2S6
A tellúr kalkogénei[szerkesztés]
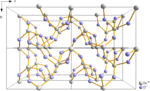
- tellúr-monoxid, TeO (instabil átmeneti állapot)
- tellúr-dioxid, TeO2
- tellúr-trioxid, TeO3
- ditellúr-pentoxid, Te2O5[2]
- Különböző vegyületek, ahol a tellúr és a kén különböző koncentrációban félfémes kötéssel kapcsolódnak, TexSy
- Különböző vegyületek, ahol a tellúr és a szelén különböző koncentrációban félfémes kötéssel kapcsolódnak, TexSey
A polónium kalkogénei[szerkesztés]
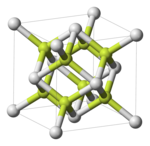
- polónium-monoxid, PoO
- polónium-dioxid, PoO2
- polónium-trioxid, PoO3
- polónium-monoszulfid, PoS
- Különböző vegyületek, ahol a polónium és a szelén különböző koncentrációban félfémes kötéssel kapcsolódnak egymáshoz PoxSey
- Különböző vegyületek, ahol a polónium és a tellúr különböző koncentrációban félfémes kötéssel kapcsolódnak egymáshoz PoxTey
Megjegyzések[szerkesztés]
- ↑ Nem egyértelmű, hogy félfém vagy másodfajú fém.
Hivatkozások[szerkesztés]
- ↑ a b c Holleman, Arnold Frederik; Wiberg, Egon (2001), Wiberg, Nils (szerk.), Inorganic Chemistry, fordította Eagleson, Mary; Brewer, William, San Diego/Berlin: Academic Press/De Gruyter, pp. 585–586, ISBN 0-12-352651-5
- ↑ http://scripts.iucr.org/cgi-bin/paper?S0567740873003092
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben az Interchalcogen című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
