„Kálium-hidroxid” változatai közötti eltérés
| [ellenőrzött változat] | [ellenőrzött változat] |
embed {{Nemzetközi katalógusok}} with Wikidata information |
|||
| 28. sor: | 28. sor: | ||
| LogP = <!--oktanol/víz--> |
| LogP = <!--oktanol/víz--> |
||
}} |
}} |
||
| CrystalStruct = monoklin |
| CrystalStruct = monoklin<ref>{{cite journal | title = Structure of Potassium Hydroxide: An X-Ray and Infrared Study | author = James A. Ibers, Junji Kumamoto, and Robert G. Snyder | journal = J. Chem. Phys. | year = 1960 | volume = 33 | issue = 4 | pages = 1164-1170 | doi = 10.1063/1.1731351}}</ref> |
||
| Section10 = {{Chembox_Hazards |
| Section10 = {{Chembox_Hazards |
||
| EUClass = maró hatású ('''C''') [[Fájl:Hazard C.svg|15px]] |
| EUClass = maró hatású ('''C''') [[Fájl:Hazard C.svg|15px]] |
||
A lap 2015. november 1., 13:46-kori változata
| Kálium-hidroxid | |

| |
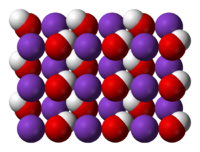
| |
| IUPAC-név | kálium-hidroxid |
| Más nevek | marókáli |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 1310-58-3 |
| EINECS-szám | 215-181-3 |
| RTECS szám | TT2100000 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | KOH |
| Moláris tömeg | 56,11 g/mol |
| Megjelenés | higroszkópos, fehér rögök |
| Halmazállapot | szilárd |
| Sűrűség | 2,04 g/cm3 (20 °C) |
| Olvadáspont | 406 °C |
| Forráspont | 1379 °C |
| Oldhatóság (vízben) | 1130 g/l (20 °C) |
| Kristályszerkezet | |
| Kristályszerkezet | monoklin[1] |
| Veszélyek | |
| EU osztályozás | maró hatású (C) |
| EU Index | 019-002-00-8 |
| R mondatok | R22, R35 |
| S mondatok | (S1/2), S26, S36/37/39, S45 |
| Lobbanáspont | nem gyúlékony |
| Rokon vegyületek | |
| Azonos kation | a kálium vegyületei |
| Azonos anion | hidroxidok |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
A kálium-hidroxid vagy marókáli egy szervetlen vegyület, amelynek képlete KOH. Színtelen kristályokat alkot, erősen higroszkópos. Erős bázis.
Története
Jellemzői
A kálium-hidroxid szobahőmérsékleten szilárd halmazállapotú, erősen nedvszívó (higroszkópos) kristályos anyag. Levegőn gyorsan elfolyósodik, és a levegő szén-dioxid tartalmával reagálva kálium-karbonáttá alakul. Vízben és alkoholban jól oldódó, a nátrium-hidroxidnál erősebb bázis, vizes oldata a kálilúg. Vizes oldatban teljesen disszociál, oldata erősen maró, lúgos kémhatású. Olvadt állapotban a szilikátokat így az üveget is feloldja.
- Kálium-hidroxid és szén-dioxid reakciója kálium-karbonát és víz keletkezése közben.
Előfordulása, előállítása
Előállítható kálium-klorid oldat elektrolízisével vagy kálium-karbonát és kalcium-hidroxid reakciója révén. Vizes oldatban végezve az utóbbi kísérletet a vízben oldhatatlan kalcium-karbonát kicsapódik, mely ezáltal eltávolítható az oldat tetejéről.
- Kálium-karbonát és kalcium-hidroxid reakciója kálium-hidroxid és kalcium-karbonát keletkezése közben.
Felhasználása
Felhasználják a laboratóriumokban vegyszerként, lúgos akkumulátorokban elektrolitként, valamint káliszappan és más káliumvegyületek előállítására.
- A VIII. Magyar Gyógyszerkönyvben Kalii hydroxidum néven hivatalos.
- Az élelmiszeriparban széles körben alkalmazzák, például a gyümölcsök héjának kémiai úton történő eltávolítására, csokoládé és kakaó készítése során, karamellel történő színezésnél, olajbogyó tartósításánál, valamint egyes pékárukban is előfordulhat, valamint az annatto (E160b) használata estén is. Élelmiszer-adalékanyagként, E525 néven alkalmazzák. Napi maximum beviteli mennyisége nincs meghatározva, valamint élelmiszerek esetén nincs ismert mellékhatása, mert rendkívül erős lúgossága miatt csak nagyon kis mennyiségben alkalmazható.[2]
Élettani tulajdonságok
Az anyag maró hatású a bőrre, a szemre és lenyelve. Maradandó égési sérüléseket okoz!
Óvintézkedések
Nagyon fontos a megfelelő védőeszköz. Gumikesztyű, védőszemüveg vagy arcvédő légzésvédelemmel kombinálva. A levegő nedvességtartalmával érintkezve elpattanhatnak a kristályok, így akár a szembe is kerülhetnek.
Források
- ↑ James A. Ibers, Junji Kumamoto, and Robert G. Snyder (1960). „Structure of Potassium Hydroxide: An X-Ray and Infrared Study”. J. Chem. Phys. 33 (4), 1164-1170. o. DOI:10.1063/1.1731351.
- ↑ Food-Info.net : E-numbers : E525 : Potassium hydroxide


