„Izobutanol” változatai közötti eltérés
| [ellenőrzött változat] | [ellenőrzött változat] |
a r2.7.1) (Bot: következő hozzáadása: fa:ایزوبوتانول |
a r2.7.1) (Bot: következő hozzáadása: sr:Izobutanol |
||
| 82. sor: | 82. sor: | ||
[[no:Isobutanol]] |
[[no:Isobutanol]] |
||
[[pt:Isobutanol]] |
[[pt:Isobutanol]] |
||
[[sr:Izobutanol]] |
|||
[[sv:Isobutanol]] |
[[sv:Isobutanol]] |
||
[[zh:异丁醇]] |
[[zh:异丁醇]] |
||
A lap 2012. október 18., 09:28-kori változata
| Izobutanol | |||
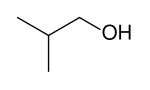 Isobutanol |
 Izobutanol | ||
| IUPAC-név | 2-metilpropán-1-ol, 2-metil-1-propanol | ||
| Más nevek | izobutil-alkohol | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 78-83-1 | ||
| RTECS szám | NP9625000 | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C4H10O | ||
| Moláris tömeg | 74,12 g/mol | ||
| Megjelenés | Színtelen folyadék | ||
| Sűrűség | 0,80 g/cm³[1] | ||
| Olvadáspont | -107,8 °C[1] | ||
| Forráspont | 108 °C[1] | ||
| Oldhatóság (vízben) | 95 g/l, 20 °C[1] | ||
| Viszkozitás | 3,95 centipoise 20°C-on | ||
| Gőznyomás | 11,8 mbar (20 °C), 73,4 mbar (50 °C)[1] | ||
| Veszélyek | |||
| EU osztályozás | Irritatív (Xi)[2] | ||
| NFPA 704 | |||
| R mondatok | R10, R37/38, R41, R67[2] | ||
| S mondatok | (S2), S7/9, S13, S26, S37/39, S46[2] | ||
| Lobbanáspont | 27 °C[1] | ||
| Öngyulladási hőmérséklet | 430 °C[1] | ||
| LD50 | 2460 mg/kg (patkány, szájon át)[1] | ||
| Rokon vegyületek | |||
| Rokon alkoholok | izopropil-alkohol, etanol, 2-butanol | ||
| Rokon vegyületek | aceton, propilén, diizopropil-éter | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Az izobutanol (vagy izobutil-alkohol, 2-metil-1-propanol, 2-metilpropán-2-ol) egy szerves vegyület, az alkoholok közé tartozik. Primer alkohol (a hidroxilcsoportja láncvégi szénatomhoz kapcsolódik). Három szerkezeti izomerje van ezek az n-butanol, a 2-butanol és a terc-butanol. Színtelen, jellegzetes szagú folyadék. Feloldódik vízben, etanolban és dietil-éterben.
Kémiai tulajdonságai
Gyúlékony vegyület, a lobbanáspontja körülbelül 27 °C. Az alkoholok általános reakcióit mutatja: karbonsavakkal észtereket képez, illetve dehidrogénezéssel aldehiddé alakul.
Előfordulása a természetben
A természetben észterei alakjában található meg, ezek az észterek gyümölcsök ízanyagai.
Előállítása
A keményítő alkoholos erjedésekor keletkező úgynevezett kozmás olajok alkotórésze. Ezekből frakcionált desztillációval nyerhető ki. Előállítható a szintézisgázból is katalizátor jelenlétében, a metanol ipari előállításához hasonló módon.
Felhasználása
Az izobutanol kiindulási anyagként szolgál szerves kémiai szintéziseknél, például észterek és lágyítók előállítására használják.[1] Oldószerként is alkalmazzák, főként a lakkiparban.
Források
- Bruckner Győző: Szerves kémia, I/1-es kötet
- Erdey-Grúz Tibor: Vegyszerismeret
Hivatkozások
Lásd még
- Butanol – A vegyület izomerjei táblázatban

