Polyomaviridae
| Polyomaviridae | ||||
|---|---|---|---|---|
 Egér-poliómavírus modellje
| ||||
| Vírusbesorolás | ||||
| ||||
| Nemek | ||||
| ||||
| Hivatkozások | ||||
A Wikifajok tartalmaz Polyomaviridae témájú rendszertani információt. A Wikimédia Commons tartalmaz Polyomaviridae témájú kategóriát. |
A Polyomaviridae a vírusok egy családja, amelybe kettős szálú DNS-genommal rendelkező, lipidburok nélküli fajok, az ún. poliómavírusok tartoznak. Elsősorban emlősöket és madarakat fertőznek. 2015-ben a családba 76 ismert faj tartozott, amelyből 73-at négy nembe osztottak be, három pedig egyelőre osztályozatlan.[1] Közülük 13 képes az embert is megfertőzni;[2][3] többségük azonban, bár meglehetősen elterjedtek (mint a BK-vírus vagy a JC-vírus), csak immunhiányos betegekben okoznak klinikai tüneteket.[4][5] A BK-vírus veseátültetett páciensek vesekárosodásában,[6][7] a JC-vírus progresszív multifokális leukoencefalopátiában,[8] a Merkel-sejtes vírus pedig a Merkel-sejtes karcinómában játszhat szerepet.[9]
A család egyes tagjai (egér-poliómavírus, SV40) onkovírusok, vagyis daganatot képesek indukálni; gazdaszervezetükben többnyire nem okoznak szimptómákat, de agresszívak lehetnek ha annak immunrendszere károsodik vagy más fajba kerülnek át. A család elnevezése, a polióma arra utal, hogy tagjai többféle tumort képesek okozni.
Szerkezetük[szerkesztés]
A poliómavírusok 40-50 nm átmérőjű, T7 ikozaéder-szimmetriájú kapsziddal rendelkeznek. Genomjuk kör alakú (cirkuláris) és kettős szálú DNS-ből áll; hossza kb. 5000 bázispár.[10] A kapszidot 72 alegység építi fel; az alegységek a VP1 kapszidfehérje pentamerjei (öt fehérje alkot egy alegységet). Az alegységek spontán képesek ikozaéder formájú vírusburokká összeállni.[11] Minden egyes VP1 a burok belső oldalán egy-egy másik burokfehérjéhez, a VP2-höz és VP3-hoz kapcsolódik.[12]

A poliómavírusoknak többnyire 5-9 génjük van amelyek vagy a fertőzés korai vagy a késői szakaszában aktiválódó régióban találhatóak. A teljes régiót a gazdasejt RNS-polimeráz II enzimje írja át egyetlen hosszú mRNS-sé. A korai régió többnyire két gént tartalmaz, a kis és nagy tumorantigént, amelyek végleges mRNS-e alternatív splicing által jön létre. A késői régióban a három kapszidprotein génje található. Egyes vírusok további fehérjéket is kódolhatnak. A rágcsálók poliómavírusai esetében a korai régióban egy harmadik fehérje, a közepes tumorantigén is előfordulhat, amely különösen hatékonyak alakítja át a gazdasejtet tumorsejtté. Az SV40-nek vagy egy negyedik burokfehérjéje (VP4) is. A genom egy nem-kódoló szakaszt is tartalmaz, amely a korai és késői régiókat kifejeződését szabályozza, valamint a másolást megindító replikációs origó is itt helyezkedik el.[10][12]
Életciklusuk[szerkesztés]
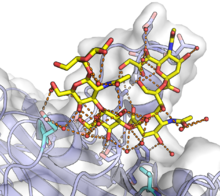
A fertőzés első lépéseként a vírusnak kapcsolódnia kell a sejt felszínéhez. A poliómavírusok receptora a glikoproteinek vagy glikolipidek (főlkeg gangliozidok) sziálsav része. A sziálsavat a VP1 köti meg,[13] majd a vírusrészecske endocitózissal a sejt belsejébe kerül. A kapszid szétesése után a vírus-DNS a citoplazmából ismeretlen mechanizmussal a sejtmagba vándorol.
A poliómavírusok a sejtmagban szaporodnak. Replikációjuk négy szakaszból áll:
- korai gének aktivációja
- DNS-másolás,
- kései gének aktivációja
- összeszerelés.
A vírus-DNS másolását és a gének transzkripcióját teljes egészében a sejt enzimjei végzik, ezért a korai vírusfehérjék más vírusoktól (amelyek saját enzimmel végzik a genom másolását) eltérően szabályozó proteinek.
Első lépésként a vírusgenom aktivátor régióinak hatására a sejt saját RNS-polimeráza létrehozza az ún. T-antigén mRNS-ét, majd erről fehérje íródik át. A T-antigén serkenti a saját termelődését, így igen hamar nagy mennyiség készül belőle. Ezenkívül stimulálja a vírusgenom átírását és a sejt osztódását; valamint gátolja a tumorellenes p53 sejtfehérje működését. Amikor koncentrációja elér egy bizonyos mértéket, átírása gátlás alá kerül és megkezdődik a fertőzés kései szakasza.
Eközben a sejtmagban található DNS-másoló mechanizmus elkezdi lemásolni a sejt saját kromoszómáihoz hasonlító, kettős szálú vírus-DNS-t. A kromoszómákhoz hasonlóan a vírusgenom is a nukleoszóma-szerűen becsomagolódik, egyfajta minikromoszómaként.
A kései szakaszban a struktúrproteinek, gyakorlatilag a burokfehérjék készülnek nagy mennyiségben. Ez a folyamat részben párhuzamosan zajlik a genom replikációjával. A kései proteinek egy része alternatív splicinggel jön létre.
Valamennyi vírusfehérjén nukleáris lokalizációs jel található, vagyis a gazdasejt a sejtmagba szállítja őket, ahol hamarosan nagy mennyiségben gyűlnek össze és megkezdődik a kapszidok, majd a kész vírusrészecskék (virionok) összeszerelődése.[14]
Mindezen folyamatok közben a sejt olyan mértékben károsodik, hogy elpusztul, szétesik, a vírusrészecskék pedig kiszabadulnak a külvilágba. Kisebb mértékben úgy is kikerülhetnek a még élő sejtből, hogy citoplazmatikus vakuólumok szállítják őket a sejthártyához és bimbózással szabadulnak ki.
A poliómavírusok jellemzően a gazdaszervezet (emlős, madár) légzőszerveinek, veséjének vagy agyának szöveteit fertőzik meg és az ürülék közvetítésével kerülnek át másik állatba (vagy az emberbe).
Osztályozásuk[szerkesztés]
A poliómavírusok a Baltimore-rendszerben az I. csoportba, a kettős szálú DNS-vírusokhoz tartoznak. Korábban, amíg DNS-szekvenciájuk nem volt ismert, a hasonló szerkezetű papillómavírusokkal együtt a Papovaviridae csoportba sorolták őket.[15]
A jelenleg érvényes ICTV szerinti osztályozásuk szerint a családba 76 faj tartozik, amelyből 73 négy nembe sorolható, 3 pedig egyelőre besorolatlan:[1][2]
- Alphapolyomavirus (típusfaj az egér-poliómavírus)
- Betapolyomavirus (típusfaj a rhesusmajom-poliómavírus 1, azaz SV40))
- Gammapolyomavirus (típusfaj a madár-poliómavírus 1)
- Deltapolyomavirus (típusfaj a humán poliómavírus 6)
Humán poliómavírusok[szerkesztés]
Az ismert poliómavírusok közül 13 képes megfertőzni az embert.[2] Legtöbbjük általánosan elterjedt a népesség körében és nem okoz tüneteket.[4][5] Egyes fajok azonban különböző betegségekkel asszociálhatóak, különösen immungyenge betegek esetében. A Merkel-sejtes poliómavírus nagyon eltér a többi emberben is megtalálható fajtól és leginkább az egerek vírusaival rokon.
| Formális név | Nem | Triviális név | Rövidítés | Genomszekvencia | Felfedezés éve | Kórkép | Forrás |
|---|---|---|---|---|---|---|---|
| Humán poliómavírus 5 | Alpha | Merkel-sejtes poliómavírus | MCPyV | NC_010277 | 2008 | Merkel-sejtes karcinóma[12] | [16][17][18] |
| Humán poliómavírus 8 | Alpha | Trichodysplasia spinulosa-poliómavírus | TSPyV | NC_014361 | 2010 | Trichodysplasia spinulosa[12] | [19][20] |
| Humán poliómavírus 9 | Alpha | Humán poliómavírus 9 | HPyV9 | NC_015150 | 2011 | nem ismert | [21] |
| Humán poliómavírus 12 | Alpha | Humán poliómavírus 12 | HPyV12 | NC_020890 | 2013 | nem ismert | [22] |
| Humán poliómavírus 13 | Alpha | New Jersey-poliómavírus | NJPyV | NC_024118 | 2014 | nem ismert | [23] |
| Humán poliómavírus 1 | Beta | BK-poliómavírus | BKPyV | NC_001538 | 1971 | poliómavírus-asszociált nefropátia; hemorrágiás cisztitisz[12] | [24] |
| Humán poliómavírus 2 | Beta | JC-poliómavírus | JCPyV | NC_001699 | 1971 | progresszív multifokális leukoencefalopátia[12] | [25] |
| Humán poliómavírus 3 | Beta | KI-poliómavírus | KIPyV | NC_009238 | 2007 | nem ismert | [26] |
| Humán poliómavírus 4 | Beta | WU-poliómavírus | WUPyV | NC_009539 | 2007 | nem ismert | [27] |
| Humán poliómavírus 6 | Delta | Humán poliómavírus 6 | HPyV6 | NC_014406 | 2010 | nem ismert | [28] |
| Humán poliómavírus 7 | Delta | Humán poliómavírus 7 | HPyV7 | NC_014407 | 2010 | HPyV7-asszociált keratózis[29] | [28] |
| Humán poliómavírus 10 | Delta | MW-poliómavírus | MWPyV | NC_018102 | 2012 | nem ismert | [30][31][32] |
| Humán poliómavírus 11 | Delta | STL-poliómavírus | SLTPyV | NC_020106 | 2013 | nem ismert | [33] |
A Deltapolyomavirus nembe csak a fenti négy embert megfertőző faj tartozik. Az Alpha és Beta nemek fajai más emlősökben is megtalálhatóak. A Gamma csoportba csak madárvírusok tartoznak.[2]
Felfedezésük[szerkesztés]
A család első tagját, az egér-poliómavírust 1953-ban izolálta leukémiasejtek extraktumából a lengyel-amerikai Ludwik Gross és azt is felismerte, hogy a vírus a nyálmirigyekben tumort képes indukálni.[34] A kórokozó vírusmivoltát Sarah Stewart és Bernice Eddy fedezte fel; az ő nevük rövidítéséből egy ideig SE-poliómának nevezték.[35][36][37] A polióma arra utalt, hogy a fertőző ágens többfajta tumort is képes volt okozni.
2016-ig több tucatnyi poliómavírust azonosítottak és genomjukat meg is szekvenálták. Többnyire emlősöket és madarakat fertőznek, de két faj is ismert, amelynek hal a gazdaállata: a fekete-tengeri sügér (Centropristis striata) és az aranydurbincs (Sparus aurata).[38][39]
Jegyzetek[szerkesztés]
- ↑ a b Virus Taxonomy: 2015 Release. [2016. augusztus 12-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. július 26.)
- ↑ a b c d (2016. február 29.) „A taxonomy update for the family Polyomaviridae.”. Archives of Virology 161, 1739–50. o. DOI:10.1007/s00705-016-2794-y. PMID 26923930.
- ↑ (2013) „A cornucopia of human polyomaviruses”. Nat. Rev. Microbiol. 11, 264–76. o. DOI:10.1038/nrmicro2992. PMID 23474680.
- ↑ a b (2016. január 1.) „Seroepidemiology of Human Polyomaviruses in a US Population.”. American Journal of Epidemiology 183 (1), 61–9. o. DOI:10.1093/aje/kwv155. PMID 26667254.
- ↑ a b (2009. március 1.) „Seroepidemiology of human polyomaviruses.”. PLOS Pathogens 5 (3), e1000363. o. DOI:10.1371/journal.ppat.1000363. PMID 19325891.
- ↑ (2016. január 18.) „BK virus nephropathy in renal transplant recipients.”. Nephrology (Carlton, Vic.) 21, 647–54. o. DOI:10.1111/nep.12728. PMID 26780694.
- ↑ (2016. április 1.) „BK polyoma virus infection and renal disease in non-renal solid organ transplantation.”. Clinical kidney journal 9 (2), 310–8. o. DOI:10.1093/ckj/sfv143. PMID 26985385.
- ↑ (2015. május 5.) „Progressive Multifocal Leukoencephalopathy.”. F1000Research 4. DOI:10.12688/f1000research.7071.1. PMID 26918152.
- ↑ (2008) „Clonal Integration of a Polyomavirus in Human Merkel Cell Carcinoma”. Science 319 (5866), 1096–100. o. DOI:10.1126/science.1152586. PMID 18202256.
- ↑ a b Viral Zone. ExPASy. (Hozzáférés: 2015. június 15.)
- ↑ (1986. szeptember 12.) „Self-assembly of purified polyomavirus capsid protein VP1.”. Cell 46 (6), 895–904. o. DOI:10.1016/0092-8674(86)90071-1. PMID 3019556.
- ↑ a b c d e f (2013. április 1.) „A cornucopia of human polyomaviruses.”. Nature reviews. Microbiology 11 (4), 264–76. o. DOI:10.1038/nrmicro2992. PMID 23474680.
- ↑ (2015. október 1.) „Structural and Functional Analysis of Murine Polyomavirus Capsid Proteins Establish the Determinants of Ligand Recognition and Pathogenicity.”. PLOS Pathogens 11 (10), e1005104. o. DOI:10.1371/journal.ppat.1005104. PMID 26474293.
- ↑ (2012) „Trichodysplasia spinulosa is characterized by active polyomavirus infection”. Journal of Clinical Virology 53 (3), 225–30. o. DOI:10.1016/j.jcv.2011.11.007. PMID 22196870.
- ↑ (2013. május 5.) „IARC Working Group on the Evaluation of Carcinogenic Risk to Humans. Malaria and Some Polyomaviruses (SV40, BK, JC, and Merkel Cell Viruses).”. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 104.
- ↑ Altman, Lawreence K.. „Virus Is Linked to a Powerful Skin Cancer”, The New York Times, 2008. január 18. (Hozzáférés: 2008. január 18.)
- ↑ (2008) „Clonal Integration of a Polyomavirus in Human Merkel Cell Carcinoma”. Science 319 (5866), 1096–100. o. DOI:10.1126/science.1152586. PMID 18202256.
- ↑ (2009) „Human Merkel cell polyomavirus infection I. MCV T antigen expression in Merkel cell carcinoma, lymphoid tissues and lymphoid tumors”. International Journal of Cancer 125 (6), 1243–9. o. DOI:10.1002/ijc.24510. PMID 19499546.
- ↑ (2010) „Discovery of a New Human Polyomavirus Associated with Trichodysplasia Spinulosa in an Immunocompromized Patient”. PLoS Pathogens 6 (7), e1001024. o. DOI:10.1371/journal.ppat.1001024. PMID 20686659.
- ↑ (2013. augusztus 1.) „The trichodysplasia spinulosa-associated polyomavirus: virological background and clinical implications.”. APMIS : acta pathologica, microbiologica, et immunologica Scandinavica 121 (8), 770–82. o. DOI:10.1111/apm.12092. PMID 23593936.
- ↑ (2011. május 1.) „A novel human polyomavirus closely related to the african green monkey-derived lymphotropic polyomavirus.”. Journal of Virology 85 (9), 4586–90. o. DOI:10.1128/jvi.02602-10. PMID 21307194.
- ↑ (2013) „Identification of a Novel Human Polyomavirus in Organs of the Gastrointestinal Tract”. PLoS ONE 8 (3), e58021. o. DOI:10.1371/journal.pone.0058021. PMID 23516426.
- ↑ (2014. november 15.) „Identification of a novel polyomavirus in a pancreatic transplant recipient with retinal blindness and vasculitic myopathy.”. The Journal of Infectious Diseases 210 (10), 1595–9. o. DOI:10.1093/infdis/jiu250. PMID 24795478.
- ↑ (1971. június 19.) „New human papovavirus (B.K.) isolated from urine after renal transplantation.”. Lancet (London, England) 1 (7712), 1253–7. o. PMID 4104714.
- ↑ (1971. június 19.) „Cultivation of papova-like virus from human brain with progressive multifocal leucoencephalopathy.”. Lancet (London, England) 1 (7712), 1257–60. o. PMID 4104715.
- ↑ (2007) „Identification of a Third Human Polyomavirus”. Journal of Virology 81 (8), 4130–6. o. DOI:10.1128/JVI.00028-07. PMID 17287263.
- ↑ (2007) „Identification of a Novel Polyomavirus from Patients with Acute Respiratory Tract Infections”. PLoS Pathogens 3 (5), e64. o. DOI:10.1371/journal.ppat.0030064. PMID 17480120.
- ↑ a b (2010) „Merkel Cell Polyomavirus and Two Previously Unknown Polyomaviruses Are Chronically Shed from Human Skin”. Cell Host & Microbe 7 (6), 509–15. o. DOI:10.1016/j.chom.2010.05.006. PMID 20542254.
- ↑ (2015. május 15.) „Human polyomavirus 7-associated pruritic rash and viremia in transplant recipients.”. The Journal of Infectious Diseases 211 (10), 1560–5. o. DOI:10.1093/infdis/jiu524. PMID 25231015.
- ↑ (2012) „Identification of MW Polyomavirus, a Novel Polyomavirus in Human Stool”. Journal of Virology 86 (19), 10321–6. o. DOI:10.1128/JVI.01210-12. PMID 22740408.
- ↑ (2012) „Complete Genome Sequence of a Tenth Human Polyomavirus”. Journal of Virology 86 (19), 10887. o. DOI:10.1128/JVI.01690-12. PMID 22966183.
- ↑ (2012) „Discovery of a Novel Polyomavirus in Acute Diarrheal Samples from Children”. PLoS ONE 7 (11), e49449. o. DOI:10.1371/journal.pone.0049449. PMID 23166671.
- ↑ (2013) „Discovery of STL polyomavirus, a polyomavirus of ancestral recombinant origin that encodes a unique T antigen by alternative splicing”. Virology 436 (2), 295–303. o. DOI:10.1016/j.virol.2012.12.005. PMID 23276405.
- ↑ (1953) „A Filterable Agent, Recovered from Ak Leukemic Extracts, Causing Salivary Gland Carcinomas in C3H Mice”. Experimental Biology and Medicine 83 (2), 414–21. o. DOI:10.3181/00379727-83-20376. PMID 13064287.
- ↑ (1958. június 1.) „Neoplasms in mice inoculated with a tumor agent carried in tissue culture.”. Journal of the National Cancer Institute 20 (6), 1223–43. o. PMID 13549981.
- ↑ (1959. november 1.) „Characteristics of the SE Polyoma Virus”. American Journal of Public Health and the Nations Health 49 (11), 1486–1492. o. DOI:10.2105/AJPH.49.11.1486.
- ↑ Polyoma Virus Infection, Pathology of Laboratory Rodents and Rabbits, 3rd, John Wiley & Sons (2013. május 5.). ISBN 1118704630
- ↑ (2015. január 29.) „Genome Sequence of a Fish-Associated Polyomavirus, Black Sea Bass (Centropristis striata) Polyomavirus 1.”. Genome announcements 3 (1). DOI:10.1128/genomeA.01476-14. PMID 25635011.
- ↑ (2016. július 20.) „Concurrence of iridovirus, polyomavirus and a unique member of a new group of fish papillomaviruses in lymphocystis disease affected gilthead seabream.”. Journal of Virology. DOI:10.1128/JVI.01369-16. PMID 27440877.
Források[szerkesztés]
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben a Polyomaviridae című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.


