Parciális nyomás
A gázkeverékekben minden gáz saját parciális nyomással rendelkezik, ez az az elméleti nyomás, amelyet a gáz akkor fejtene ki, ha ugyanazon a hőmérsékleten egyedül töltené ki a teljes térfogatot.[1] A komponensek parciális nyomásának összege adja a rendszer össznyomását (Dalton-törvény).
Egy gáz parciális nyomása a gázmolekulák termodinamikai aktivitásának mértéke. A gázok nem a gázkeverékben vagy folyadékokban vett koncentrációjuknak, hanem a parciális nyomásuknak megfelelő mértékben oldódnak, diffundálnak és lépnek reakcióba. A gázoknak ez az általános tulajdonsága érvényes a gázok biológiai folyamatokban végbemenő kémiai reakcióiban is. Azt, hogy az oxigén mennyisége elegendő-e az emberi légzéshez, vagy már mérgező, egyedül az oxigén parciális nyomása határozza meg. Ez nagyon széles koncentrációtartományban, különböző gázkeverékekben vagy vérben oldott oxigénre is érvényes.[pontosabban?][2] Az oxigén és a szén-dioxid parciális nyomása fontos paraméter az artériás vérgázvizsgálatban, de ezek az értékek például az agy-gerincvelői folyadékban is meghatározhatók.
Jelölés[szerkesztés]
A nyomás jele többnyire P vagy p, alsó indexben szerepelhet a gáz minősége vagy egyéb azonosító. Ha ezekből több is van, az alsó indexelés rekurzívan alkalmazandó.[3][4]
például:
- or = nyomás az 1. időpontban
- or = a hidrogén parciális nyomása
- or = az oxigén vénás parciális nyomása
Dalton-törvény[szerkesztés]
Dalton törvénye kimondja, hogy egy gázelegy össznyomása egyenlő a gázelegyet alkotó egyes gázok parciális nyomásának összegével.[5] Ez az egyenlőség abból fakad, hogy az ideális gáz molekulái olyan távol vannak egymástól, hogy nem hatnak egymásra. A valóságban a gázok többsége nagyon jól megközelíti ezt az idealizált állapotot. Nitrogén (N2), hidrogén (H2) és ammónia (NH3) ideális gázelegyében például:
| ahol: | |
| = a gázelegy teljes nyomása | |
| = a nitrogén (N2) parciális nyomása | |
| = a hidrogén (H2) parciális nyomása | |
| = az ammónia (NH3) parciális nyomása |

Ideális gázelegyek[szerkesztés]
Ideális esetben a parciális nyomások aránya megegyezik a molekulák számarányával, azaz az ideális gázoknál az egyes gázkomponensek móltörtje kifejezhető a komponens parciális nyomásával vagy anyagmennyiségével:
és ideális gázban egy egyedi komponens parciális nyomása az alábbi kifejezéssel kapható meg:
| ahol: | |
| = a gázkomponens móltörtje a gázelegyben | |
| = a gázkomponens parciális nyomása a gázelegyben | |
| = a gázkomponens anyagmennyisége (mólban) a gázelegyben | |
| = a gázelegy teljes anyagmennyisége (mólban) | |
| = a gázelegy teljes nyomása |
Egy gázkeverékben az egyes komponensek móltörtje egyenlő a komponensek a gázkeverékbeli térfogattörtjével.[6]
A parciális nyomások aránya az alábbi izoterm összefüggésen alapszik:
-
- Vx bármely egyedi (x) gáz komponens parciális térfogata
- Vtot a gázelegy teljes térfogata
- px az x gáz parciális nyomása
- ptot a gázelegy teljes nyomása
- nx a(z x) gáz anyagmennyisége
- ntot a gázelegy teljes anyagmennyisége
Parciális térfogat (Amagat-szabály)[szerkesztés]
Egy adott gáz parciális térfogata egy gázelegyben az adott gáznak a térfogata az elegyben. Ez a fogalom gázkeverékek, például a levegő esetében hasznos, ha csak az egyik komponenst, például az oxigén áll a középpontban.
A parciális térfogat mind a parciális nyomás, mint a móltört segítségével közelíthető:[7]
-
- Vx az x komponens parciális térfogata az elegyben
- Vtot a gázelegy teljes térfogata
- px az x komponens parciális nyomása
- ptot a gázelegy teljes nyomása
- nx az x komponens anyagmennyisége
- ntot a gázelegyben a komponensek összes anyagmennyisége
Gőznyomás[szerkesztés]
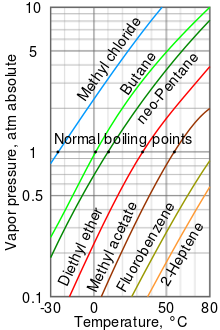
A gőznyomás egy, a kondenzált (azaz folyadék vagy szilárd) fázissal egyensúlyban levő gőz nyomása, többnyire a folyadékok párolgásra való hajlamának jellemzésére használják. A gőznyomás a molekulák és atomok folyadék vagy szilárd halmazállapotból történő szökésének mértéke. A folyadékok légköri nyomáson mért forráshőmérséklete megegyezik azzal a hőmérséklettel, amelyen a gőznyomása egyenlő a környező légnyomással, ezt forráspontnak vagy normál forráspontnak nevezzük.
Adott hőmérsékleten minél nagyobb egy folyadék gőznyomása, annál alacsonyabb a normál forráspontja.
A gőznyomásdiagramok különböző folyadékok gőznyomását ábrázolják a hőmérséklet függvényében.[8] Ahogy az ábrán is látható, a legnagyobb gőznyomású folyadékoknak van a legalacsonyabb normális forráspontja.
Az ábrán feltüntetett folyadékok közül a metil-klorid gőznyomása a legnagyobb bármely hőmérsékleten. A normális forráspontja – ahol a metil-klorid gőznyomásgörbéje (kék vonal) metszi az egy atmoszféra (atm) nyomás vízszintes vonalát – is ennek az anyagnak a legkisebb, −24,2 °C. Megjegyzendő, hogy nagyobb tengerszint feletti magasságon a légköri nyomás kisebb, mint tengerszinten, ezért a folyadékok forráspontja lecsökken. A Csomolungma tetején a légnyomás közelítőleg 0,333 atm, így az ábráról leolvasva a dietil-éter forráspontja kb. 7,5 °C-nak adódik, a tengerszinten (1 atm) mért 34,6 °C-hoz képest.
Gázkeverékek reakcióinak egyensúlyi állandója[szerkesztés]
Gázkeverékben zajló kémiai reakció egyensúlyi állandóját meg lehet határozni az egyes komponensek parciális nyomásának és a reakcióegyenletnek az ismeretében. Gázállapotú reaktánsok és termékek alábbi módon felírható megfordítható reakciójában:
az egyensúlyi állandó:
| ahol: | |
| = a reakció egyensúlyi állandója | |
| = az reaktáns sztöchiometriai együtthatója | |
| = a reaktáns sztöchiometriai együtthatója | |
| = a termék sztöchiometriai együtthatója | |
| = a termék sztöchiometriai együtthatója | |
| = a parciális nyomása a -edik hatványon | |
| = a parciális nyomása a -edik hatványon | |
| = az parciális nyomása az -adik hatványon | |
| = a parciális nyomása a -edik hatványon |
Megfordítható reakciók esetén az össznyomás, a hőmérséklet vagy a reaktánsok koncentrációjának változása a tömeghatás törvényének (Le Chatelier-elv) megfelelően az egyenlet bal vagy jobb oldala felé tolja el az egyensúlyt.
A Henry-törvény és a gázok oldhatósága[szerkesztés]
A gázoknak egy folyadékban való oldhatóságát az oldott és nem oldott gáz közötti egyensúly határozza meg.[9] Ennek az egyensúlyi állandója:
- (1)
ahol: = a szolvatációs folyamat egyensúlyi állandója = az gáz parciális nyomása egyensúlyban = az gáz koncentrációja az oldatban
Az egyensúlyi állandó kifejezéséből látható, hogy egy oldott gáz oldatbeli koncentrációja egyenesen arányos ennek a gáznak az oldat feletti parciális nyomásával. Ezt nevezik Henry törvényének, a egyensúlyi állandót pedig Henry-állandónak.[9][10][11]
A Henry-törvény az alábbi alakban is felírható:[12]
- (2)
ahol -t is Henry-állandónak nevezik.[12] Ahogy az (1) és (2) egyenletek összehasonlításából látható, nem más, mint reciproka. Mivel bármelyiket hívhatják Henry-állandónak, az olvasónak figyelmesnek kell lennie, hogy adott esetben éppen melyik változattal találkozik.
A Henry-törvény csak közelítés, híg, ideális oldatokra érvényes, ha nincs kémiai reakció az oldószer és az oldott gáz között.
Az orvostudományban[szerkesztés]
Különösen az oxigén és a szén-dioxid parciális nyomása (, illetve ) fontos paraméter az artériás vérgázvizsgálatban, de ezek az értékek például az agy-gerincvelői folyadékban is meghatározhatók.[pontosabban?]
| Egység | artériás vérgáz | vénás vérgáz | agy-gerincvelői folyadék | alveoláris nyomás | |
|---|---|---|---|---|---|
| kPa | 11–13[13] | 4,0–5,3[13] | 5,3–5,9[13] | 14,2 | |
| Hgmm | 75–100[14] | 30–40[15] | 40–44[16] | 107 | |
| kPa | 4,7–6,0[13] | 5,5–6,8[13] | 5,9–6,7[13] | 4,8 | |
| mmHg | 35–45[14] | 41–51[15] | 44–50[16] | 36 |
Jegyzetek[szerkesztés]
- ↑ Charles Henrickson. Chemistry. Cliffs Notes (2005). ISBN 0-7645-7419-1
- ↑ Gas Pressure and Respiration. Lumen Learning
- ↑ Symbols and Units. Respiratory Physiology & Neurobiology : Guide for Authors . Elsevier. (Hozzáférés: 2017. június 3.) „All symbols referring to gas species are in subscript,”
- ↑ IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Compiled by A. D. McNaught and A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). XML on-line corrected version: http://goldbook.iupac.org (2006-) created by M. Nic, J. Jirat, B. Kosata; updates compiled by A. Jenkins. ISBN 0-9678550-9-8. https://doi.org/10.1351/goldbook. Last update: 2014-02-24; version: 2.3.3. DOI of this term: https://doi.org/10.1351/goldbook.P04819.
- ↑ Dalton's Law of Partial Pressures. [2017. február 1-i dátummal az eredetiből archiválva]. (Hozzáférés: 2019. március 15.)
- ↑ Frostberg State University's "General Chemistry Online"
- ↑ Page 200 in: Medical biophysics. Flemming Cornelius. 6th Edition, 2008.
- ↑ Perry, R.H. and Green, D.W. (Editors). Perry's Chemical Engineers' Handbook, 7th, McGraw-Hill (1997). ISBN 0-07-049841-5
- ↑ a b An extensive list of Henry's law constants, and a conversion tool
- ↑ (2007. szeptember 1.) „Avoid Common Pitfalls When Using Henry's Law”. CEP (Chemical Engineering Progress). ISSN 0360-7275.
- ↑ Introductory University Chemistry, Henry's Law and the Solubility of Gases Archiválva 2012. május 4-i dátummal a Wayback Machine-ben.
- ↑ a b University of Arizona chemistry class notes. [2012. március 7-i dátummal az eredetiből archiválva]. (Hozzáférés: 2019. március 15.)
- ↑ a b c d e f a Hgmm-ben kifejezett értékből számítva a 0,133322 kPa/mmHg átváltási tényezővel
- ↑ a b Normal Reference Range Table Archiválva 2011. december 25-i dátummal a Wayback Machine-ben. from The University of Texas Southwestern Medical Center at Dallas. Used in Interactive Case Study Companion to Pathologic basis of disease.
- ↑ a b The Medical Education Division of the Brookside Associates--> ABG (Arterial Blood Gas) Retrieved on Dec 6, 2009
- ↑ a b PATHOLOGY 425 CEREBROSPINAL FLUID [CSF] Archiválva 2012. február 22-i dátummal a Wayback Machine-ben. at the Department of Pathology and Laboratory Medicine at the University of British Columbia. By Dr. G.P. Bondy. Retrieved November 2011
Fordítás[szerkesztés]
Ez a szócikk részben vagy egészben a Partial pressure című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.












































