Korrin
| Korrin | |||
| |||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 262-76-0 | ||
| PubChem | 6438343 | ||
| ChemSpider | 16736705 | ||
| ChEBI | 33221 | ||
| |||
| |||
| InChIKey | WUPRCGRRQUZFAB-DEGKJRJSSA-N | ||
| UNII | 288E04GRMT | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | H22N4 | ||
| Moláris tömeg | 78,20 g/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
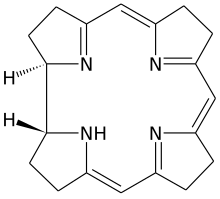
A korrin tetrapirrol. Bár nem ismert önmagában, érdeklődés van iránta, mivel a B12-vitamin kofaktorához és kromoforjához kapcsolódó alapmakrociklus. Neve arra utal, hogy B12-vitamin (kobalaminok)„magja”. Az ilyen magvú vegyületek a korrinok.[1]
Két természetes vegyületekben, például kobalaminban azonos sztereokémiájú sztereoközpontja van.
Koordinációs kémia[szerkesztés]
Deprotonálás után a korrinoid gyűrű képes kobalt kötésére. A B12-vitaminban az így keletkező komplex benzimidazol-származék ligandumot is tartalmaz, az oktaéder 6. helye katalitikus központ.
A korringyűrű a porfiringyűrűkre hasonlít.[2] Mindkettő 4 pirrolszerű alegységet tartalmaz gyűrűbe rendezve. A korrinok központja C11N4-, a porfirinok C12N4-gyűrű. A 4 nitrogénatom konjugált rendszerben kapcsolódik váltakozó kettős és egyes kötésekkel. A porfirinokkal ellentétben a korrinok a pirrolszerű egységeket teljesen konjugálttá tevő egyik szénatommal nem rendelkeznek. Mivel konjugált rendszerük csak a gyűrű háromnegyedéig ér, és nem tartalmazza a külső szénatomokat, a korrinokban több nem konjugált sp3-szénatom van, így rugalmasabbak a porfirinoknál és nem olyan laposak. Egy harmadik hasonló biológiai szerkezet, a klorofillban található kloringyűrű a porfirin és a korrin átmenete, a porfirinokhoz hasonlóan 20 szénatom van, konjugált rendszere körbeér, de csak 6 szélső szénatom vesz részt.
A korrolok (oktadehidrokorrinok) a korrinok teljesen aromás származékai.
Bioszintézis[szerkesztés]
A Propionibacterium nemzetség különböző korrinoidokat állít elő 5-aminolevulinsavból. Ezek porfobilinogénné dimerizálódnak, majd 4 porfobilinogén-egység uroporfirinogénekké alakul, melyeket az uroporfirinogén III-metiltranszferáz metilál. Ezután egy mintegy 30 reakcióból álló sorozat után jönnek létre biológiailag aktív korrinoidok, például a kobalamin.[3]
Jegyzetek[szerkesztés]
- ↑ Nelson DL, Cox MM. Lehninger, Principlex of Biochemistry, 3., New York: Worth Publishing (2000). ISBN 1-57259-153-6
- ↑ Brown, Kenneth L. (2005). „Chemistry and Enzymology of Vitamin B12”. Chemical Reviews 105 (6), 2075–2150. o. DOI:10.1021/cr030720z. PMID 15941210.
- ↑ Lena I. Vorobjeva. Propionibacteria. Springer, 160–161. o. (1999). ISBN 0-7923-5884-8
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben a Corrin című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
- Ez a szócikk részben vagy egészben a Corrin című német Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Források[szerkesztés]
- (2019. július 29.) „The Hydrogenobyric Acid Structure Reveals the Corrin Ligand as an Entatic State Module Empowering B 12 Cofactors for Catalysis”. Angewandte Chemie International Edition 58 (31), 10756–10760. o. DOI:10.1002/anie.201904713. PMID 31115943.
