Klorit
| Klorit | |||
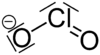 Klorition | |||
 Klorition | |||
| IUPAC-név | Klorit | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 14998-27-7 | ||
| PubChem | 197148 | ||
| ChemSpider | 170734 | ||
| EINECS-szám | 215-285-9 | ||
| |||
| InChIKey | QBWCMBCROVPCKQ-UHFFFAOYSA-M | ||
| UNII | Z63H374SB6 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | ClO−2 | ||
| Moláris tömeg | 67.452 | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A klorition halogenit, képlete OClO−. A klorit ilyen csoportot tartalmazó vegyület, ahol a klór oxidációs száma +3. A kloritok a klórossav sói és észterei.
Vegyületek
[szerkesztés]A szabad sav, a klórossav (HOClO) a legkevésbé stabil klór-oxosav, és csak kis koncentrációjú vizes oldatban észlelték. Mivel nem koncentrálható, nem forgalmazzák. Az alkálifém- és alkáliföldfémsók színtelenek vagy halványsárgák, csak a nátrium-klorit (NaOClO) kapható nagyobb mennyiségben. A nehézfém- (Ag+, Hg+, Tl+, Pb2+, Cu2+) és ammónium-kloritok instabilak, és hő vagy ütés hatásra robbanásszerűen bomlanak.[1]
A nátrium-kloritot nátrium-klorátból nyerik. Először a robbanékony klór-dioxid keletkezik nátrium-klorát megfelelő redukálószerrel (például metanol, hidrogén-peroxid, sósav vagy kén-dioxid) való redukálásakor.
Szerkezete, tulajdonságai
[szerkesztés]A klorition V alakú a klóron lévő nem kötő párok miatt, az O–Cl–O kötésszög 111°, a Cl–O kötéshossz 156 pm.[1] A klór-oxoanionok közt a klorit a legerősebb oxidálószer standard félcella-potenciálok alapján.[2]
| Ion | Savas reakció | E° (V) | Semleges/lúgos reakció | E° (V) |
|---|---|---|---|---|
| Hipoklorit | 1,63 | 0,89 | ||
| Klorit | 1,64 | 0,78 | ||
| Klorát | 1,47 | 0,63 | ||
| Perklorát | 1,42 | 0,56 |
Használat
[szerkesztés]A legfontosabb klorit a nátrium-klorit (NaOClO), melyet textilek, papír és pép fehérítésére használnak. Ezt, bár erős oxidálószer, gyakran nem közvetlenül használják, hanem klór-dioxid előállítására, általában HCl-dal való reakcióban:
Egészségi kockázatok
[szerkesztés]2009-ben a Kaliforniai Környezeti Egészségügyi Vizsgálati Hivatal (OEHHA) 50 ppb-os határértéket írt elő a kloritkoncentrációra az ivóvízben,[3] miután kutatók kiderítették, hogy nagyobb mennyiségű klorit befolyásolja a sperma- és a pajzsmirigyfunkciót, gyomorfekélyt és vörösvérsejt-károsodást okoz laboratóriumi állatokban.[4] Egyes tanulmányok szerint bizonyos mennyiségű klorit karcinogén is lehet.[5]
Az Amerikai Egyesült Államokban az országosan megengedett maximális kloritkoncentráció a kaliforniai egészségügyi határérték 20-szorosa, 1000 ppb.[6]
Kloritot használó élőlények
[szerkesztés]A klorit-dizmutáz a klorátlégzést használó egysejtűek kloritból kloridot és oxigént előállító enzime.[7] Ez jellemzően perklorát- vagy klorát-reduktázzal együtt van jelen a baktériumokban.
Egyéb oxoanionok
[szerkesztés]4 klór-oxoanion van, ahol a klór oxidációs száma +1, +3, +5 vagy +7 a megfelelő ClO−, ClO−2, ClO−3 vagy ClO−4 (hipoklorit, klorit, klorát és perklorát) ionokban. Ezek a klór-oxidok közé tartoznak.
| oxidációs szám | +1 | +3 | +5 | +7 |
|---|---|---|---|---|
| anion neve | hipoklorit | klorit | klorát | perklorát |
| képlet | ClO− | ClO−2 | ClO−3 | ClO−4 |
| szerkezet | 
|

|
Jegyzetek
[szerkesztés]- ↑ a b Chemistry of the elements, 2nd, Oxford: Butterworth-Heinemann, 861. o. (2006. november 3.). ISBN 0750633654
- ↑ Sablon:Cotton&Wilkinson5th
- ↑ Final Public Health Goal for Chlorite. oehha.ca.gov . (Hozzáférés: 2023. augusztus 8.)
- ↑ EWG's Tap Water Database: Contaminants in Your Water (angol nyelven). www.ewg.org . Environmental Working Group. (Hozzáférés: 2023. augusztus 8.)
- ↑ Public Health Goal for Chlorite in Drinking Water. oehha.ca.gov . (Hozzáférés: 2023. augusztus 8.)
- ↑ Stage 1 and Stage 2 Disinfectants and Disinfection Byproducts Rules (angol nyelven). www.epa.gov . OW US EPA, 2015. október 13. (Hozzáférés: 2023. augusztus 8.)
- ↑ J. L. DuBois, S. Ojha.szerk.: P. M. Kroneck, M. E. Torres: Chapter 3: Production of Dioxygen in the Dark: Dismutases of Oxyanions, Sustaining Life on Planet Earth: Metalloenzymes Mastering Dioxygen and Other Chewy Gases, Metal Ions in Life Sciences. Springer, 45–87. o.. DOI: 10.1007/978-3-319-12415-5_3 (2015)
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Chlorite című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Források
[szerkesztés]- Kirk-Othmer Concise Encyclopedia of Chemistry, Martin Grayson, Editor, John Wiley & Sons, Inc., 1985









