Folyadék

A folyadék (ideális folyadéknak tekintve) az anyagnak azon halmazállapota, amelyben az anyag felveszi a tárolásra szolgáló edény alakját, megtartja a térfogatát és nem képes csavaróerők továbbítására. Gyakorlatilag összenyomhatatlan, részecskéi állandóan, tetszőleges módon helyet változtatnak. A részecskék – sok szilárd anyagtól eltérően – rendezetlenül helyezkednek el, eltekintve egyfajta enyhe fokú, laza rendezettségtől. Az amorf anyagokat (pl. üveg, teflon, gumi) tekinthetjük akár nagyon nagy viszkozitású folyadékoknak is, az ezek közötti határ számos esetben nem egyértelmű.
Statikai és dinamikai tulajdonságai[szerkesztés]
Míg a szilárd anyagok szilárdsága alaktartó, a folyadékok szilárdsága térfogattartó.
A nyomás a folyadékelem normálisának megfelelő irányba mutat. A Pascal-elv értelmében a súlytalan folyadék belsejében a nyomás irányfüggetlen, ezért vektori irány nem rendelhető hozzá.
Reális folyadék[szerkesztés]
Az általános felfogás szerint az ideális folyadék részecskéi között súrlódóerők nem adódhatnak át. Eszerint a súrlódásos folyadékokat kell reális folyadéknak neveznünk. Valójában a reális folyadék más módon is eltérhet az ideális folyadéktól. Összenyomható lehet, felléphetnek benne elektrosztatikus erők, kohéziós erők, a van der Waals-erők, a felületi feszültségből származó erő is.
A vízmolekula például V alakú; a hidrogén- és az oxigénatom irányultsága[pontosabban?] miatt elektromos vagy mágneses térben rendezettséget mutat, (diamágneses), igen nagy a permittivitása.
Termodinamikai tulajdonságai[szerkesztés]
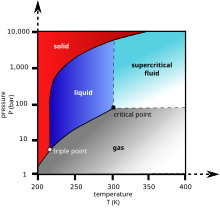
Liquid = folyadék
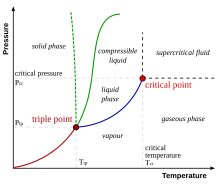
Compressible liquid = sűríthető folyadék
A folyadék halmazállapot alsó határa a hármaspont. Ez alatt az anyag vagy szilárd, vagy légnemű. A folyadék határállapot felső határa a kritikus pont. Felette az anyag vagy szuperkritikus folyadék, vagy gáz.
A hármaspont és a kritikus pont hőmérsékleti és nyomási adattal határozható meg, és az adott anyagra jellemző állandó. A szén-dioxid példája esetén a hármaspont nyomása 0,517 Ma (5,17 bar), hőmérséklete 217 K (-56 °C). Ennél kisebb értékeknél nem lehet folyékony; állapota vagy szilárd, vagy légnemű. Kritikus pontja 7,38 MPa nyomású és 304 K (+31,1 °C). Folyadék állapotban csak akkor lehet, ha a hőmérséklete ennél alacsonyabb; korlátozva ez is az igen magas nyomások tartományával (kb. 6000 bar).
Abban az esetben, ha a nyomása is és a hőmérséklete is magasabb a kritikus állapothoz tartozó értéknél, akkor szuperkritikus állapotba kerül. Ilyenkor áramlása például hasonló a gázokéhoz, de oldószerként működnek, akár a folyadékok.
Folyadékoknak palackban történő szállításához igen nagy nyomást alkalmaznak, ám az anyag ekkor is folyadékállapotban van. Ennek az állapotnak (compressible liquid) az alsó határa a kritikus nyomás értéke. Leginkább hidrogént vagy metánt tárolnak ilyen állapotban (helytelen kifejezéssel: Compressed or Liquified Gas, ezek ugyanis csak szobahőmérsékleten lennének gázállapotban; a palackban részben folyadékállapotban vannak).
Túlhűtött folyadék[szerkesztés]
A legtöbb folyadék kismértékben lehűthető a fagyáspontja alá. Ez instabil állapot, a legkisebb zavarás, vagy egy kristályosodási mag bejuttatása átviszi a folyadékot stabil állapotába, azaz megfagy. Ennek leginkább ismert példája a jégeső.
A víz átlagos körülmények között -6 °C-ig lehűthető; laboratóriumi körülmények között -20 °C-ig is.
Néhány folyadék[szerkesztés]
Minden anyagnak van folyadék halmazállapota. Ezt bizonyos jelenségek korlátozhatják, például magas hőmérsékleten kémiai bomlásnak indulhatnak; igen alacsony hőmérsékleten szuperfolyékony állapotba kerülnek (a hélium például 2,17 K hőmérsékleten és 5 kPa nyomáson átmegy szuperfolyékony Helium-II állapotba; ez a Lambda pont). A hétköznapi nyelv azokat az anyagokat nevezi folyadéknak, amelyek normál környezeti állapotban folyadékok, mint a víz, higany, bróm, kénsav, dietil-éter, alkohol, benzol, kloroform, gallium (29 °C-tól), cézium (28,44 °C-tól), dimetil-szulfoxid.
Lásd még[szerkesztés]
Források[szerkesztés]
- Cambridge enciklopédia. Szerk. David Crystal. A magyar kiadást szerk. Szelle Béla. Ford. Acsády Judit et al. Budapest: Maecenas. 1992. ISBN 963-7425-65-9
- Budó Ágoston–Pócza Jenő: Kísérleti Fizika I. Tankönyvkiadó
- Károly, Nagy. Elméleti Mechanika, 5. kiadás, Nemzeti Tankönyvkiadó (2002). ISBN 963-19-3955-3
