„Keton” változatai közötti eltérés
| [ellenőrzött változat] | [ellenőrzött változat] |
Nincs szerkesztési összefoglaló |
embed {{Nemzetközi katalógusok}} with Wikidata information |
||
| 21. sor: | 21. sor: | ||
{{Oxigéntartalmú szerves vegyületek}} |
{{Oxigéntartalmú szerves vegyületek}} |
||
{{Nemzetközi katalógusok}} |
|||
[[Kategória:Ketonok| ]] |
[[Kategória:Ketonok| ]] |
||
A lap 2015. augusztus 27., 14:14-kori változata

A ketonok oxocsoportot (═O) tartalmazó oxigéntartalmú szerves vegyületek, melyeknél a funkciós csoport egy láncközi vagy gyűrűs C atomhoz kapcsolódik. Általános képletük: R1-CO-R2. A képletben szereplő R1, R2 láncokat a keton oldalláncainak nevezzük.
Szabályos nevüket a megfelelő szénhidrogénlánc nevének végéhez illesztett -on végződéssel jelöljük. Az -on végződés előtt feltüntetjük annak a szénatomnak a számát, amelyhez az oxocsoport kapcsolódik. Így az aceton (CH3-CO-CH3) szabályos, genfi nómenklatúra szerinti neve propán-2-on. Egyes ketonok régies neve is használatos.
A ketonok legegyszerűbb képviselője az aceton.
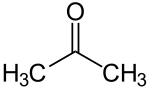
Fizikai tulajdonságok
A kisebb- és közepes szénatomszámú ketonok jellegzetes, az éterekéhez hasonló szagú folyadékok. Forráspontjuk az alkoholokénál és a karbonsavakénál alacsonyabb, mivel nem képesek hidrogén-híd kialakítására, viszont a szénhidrogénekénél magasabb, mivel a poláris molekulák dipól-dipól kölcsönhatásba léphetnek egymással. A kis szénatomszámú ketonok jól oldódnak vízben, a szénatomszám növekedésével az oldhatóság egyre csökken, az ötös szénatomszámú ketonok már vízben gyakorlatilag nem oldódnak. Az összes keton jól oldódik alkoholban és éterben.
Kémiai tulajdonságok
A ketonok oldalláncai jellegük szerint szubsztitúciós, addíciós, vagy egyéb reakciókban vehetnek részt.
A ketonok az aldehidekkel ellentétben enyhe oxidációs hatásra nem oxidálódnak, így nem adják sem az ezüsttükör-, sem a Fehling-próbát. Megfelelően erős oxidációs hatásra (pl. HNO3) azonban lánchasadás mellett oxidálhatók, ekkor különféle szénatomszámú karbonsavak keletkeznek.
Előállításuk
A ketonok előállítása a nekik megfelelő szekunder alkohol oxidációjával történhet. Előállíthatók továbbá a megfelelő karbonsavak kalciumsóinak hevítésével is.
