„Karbonsavészter” változatai közötti eltérés
| [ellenőrzött változat] | [nem ellenőrzött változat] |
Nincs szerkesztési összefoglaló Címkék: Mobilról szerkesztett Mobil web szerkesztés |
→Kémiai tulajdonságok: Képlet javítása Címkék: Mobilról szerkesztett Mobil web szerkesztés |
||
| 20. sor: | 20. sor: | ||
== Kémiai tulajdonságok == |
== Kémiai tulajdonságok == |
||
* Kondenzációval, alkoholból és karbonsav észterből, észter keletkezik (egyensúlyra vezető reakció) → <chem>R-OH +HOOC-R'<=> ROCOR' +H2O</chem>. |
* Kondenzációval, alkoholból és karbonsav észterből, észter keletkezik (egyensúlyra vezető reakció) → <chem>R-OH +HOOC-R'<=> ROCOR' +H2O</chem>. |
||
* Lúgos közegben való hidrolízise az észternek, a kondenzáció ellentettje, a folyamat neve pedig szappanosítás → <chem>R-COOH +NaOH <=>R- |
* Lúgos közegben való hidrolízise az észternek, a kondenzáció ellentettje, a folyamat neve pedig szappanosítás → <chem>R-COOH +NaOH <=>R-COO- Na +H2O </chem>. |
||
== Fontosabb észterek == |
== Fontosabb észterek == |
||
A lap 2019. október 6., 17:53-kori változata
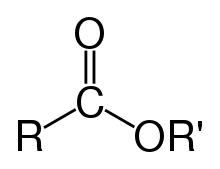
A karbonsavészterek, más néven alkil- alkanoátok, alkoholok és karbonsavak reakciója során keletkeznek vízkilépéssel. Az észterek egyik csoportját alkotják. Jellemző funkciós csoportjuk az észtercsoport (R−COO−R’). Az észtercsoport karbonil- és étercsoportból álló összetett funkciós csoport. Az elnevezés első tagja a karbonsavat, a második az alkohol szénhidrogéncsoportját, a harmadik pedig a funkciós csoportot jelöli.
Vannak gyümölcsészterek, amelyek megtalálhatóak a gyümölcsökben, mint aromaanyag. Ezeket is elő lehet állítani mesterséges úton kis szénatomszámú alkoholból és kis szénatomszámú karbonsavból. Vízben jól oldódnak a kicsi szénatomszám miatt. Kellemes szagú folyadékok.
A karbonsavészterekhez tartoznak a viaszok is. Nagy és páros szénatomszámú telített karbonsavak és ugyanilyen típusú alkoholok észterei. Szilárd halmazállapotuk van és nem oldódnak vízben.
Fizikai tulajdonságok
- A karbonilcsoportban a kötés poláris, ezért a molekula is poláris.
- Halmazban pedig dipol- dipol kötés alakul ki (az éterekhez képest itt erősebb a kötés).
- Olvadáspont és a forráspont is magasabb mint az étereké.
- H- kötés nem alakulhat ki szemben az alkoholokkal és a karbonsavakkal. (Az alkohol csak hidrogéndonor, a karbonsav hidrogén donor és akceptor is.)
- folyékony halmazállapotúak, illékonyak és kellemes illatúak (ezek a gyümölcsök aromái).
- felett szilárdak.
- A vízben való oldódásuk jobb mint az étereké de gyengébb mint az alkoholoké.
Kémiai tulajdonságok
- Kondenzációval, alkoholból és karbonsav észterből, észter keletkezik (egyensúlyra vezető reakció) → .
- Lúgos közegben való hidrolízise az észternek, a kondenzáció ellentettje, a folyamat neve pedig szappanosítás → .
Fontosabb észterek
- Kis C- atomszámúak: (kis C- atomszámú alkoholból és kis C- atomszámú karbonsavból jönnek létre)
- gyümölcsészterek
- gyógyhatású észter pl.: aszpirin (acetil-szalicilsav)
- Nagy C- atomszámúak:
- viaszok (legnagyobb nem polimer molekulák)
- zsírok, olajok (glicerin /3 értékű alkohol/ és zsírsavak észterei)
Előállítás
Például ecetsav-etil-észter (etil-acetát) előállítása
A karbonsavészterek képződése megfordítható folyamat.





