Ammónium-acetát
Megjelenés
| Ammónium-acetát | |
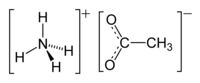 Ammónium-acetát | |
| IUPAC-név | Ammónium-acetát |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 631-61-8 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | CH3COONH4 |
| Moláris tömeg | 77,0825 g/mol |
| Megjelenés | fehér por, vagy színtelen átlátszó kristályok |
| Sűrűség | 1,07 g/cm³, szilárd |
| Olvadáspont | 112 °C |
| Forráspont | elbomlik |
| Oldhatóság (vízben) | 148 g/100 ml (4 °C) |
| Kristályszerkezet | |
| Kristályszerkezet | rombos |
| Veszélyek | |
| EU osztályozás | nincsenek veszélyességi szimbólumok[1] |
| R mondatok | (nincs)[1] |
| S mondatok | (nincs)[1] |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
Az ammónium-acetát az ecetsav és az ammónia reakciójából keletkező fehér só. Széles körben alkalmazzák, mert tisztaságától függően olcsón is beszerezhető.
Képlete: NH4C2H3O2.
Felhasználása[szerkesztés]

Mivel gyenge sav és gyenge bázis alkotja, széles körben alkalmazzák:
- a NH4C2H3O2-t alkalmanként felületek jég-, és síkosságmentesítésére
- ecetsavval együtt ún. pufferoldatként
- szerves vegyületek szintetizálása során a Knoevenagel-kondenzáció folyamán hasznos adalékanyag
- ritka tulajdonsága, hogy sóként relatív alacsony hőmérsékleten olvad
- desztillált vízben elősegíti a fehérjék kicsapódását
Tulajdonságok[szerkesztés]
A NH4C2H3O2 erősen higroszkópos, magas hőmérsékleten könnyen acetamiddé alakul:
- NH4C2H3O2 → CH3C(O)NH2 + H2O
Más anyagok esetében ehhez hasonló reakció igen ritka alacsony hőmérsékleten
Források[szerkesztés]
- ↑ a b c Az ammónium-acetát vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2011. január 1. (JavaScript szükséges) (angolul)
- G. Jones, Organic Reactions, 1967, volume 15, 204ff (the Knoevenagel Reaction)
